某学习小组用如图所示装置测定铝镁合金(不含其他杂质)中铝的质量分数和铝的相对原子质量。
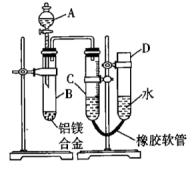
(1)A中试剂为____ 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____ 。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;
②将B中剩余固体过滤,洗涤,干燥,称重;
③待B中不再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂;
上述操作的顺序是_____ (填序号);记录C的液面位置时,除视线平视外,还应____ 。
(4)B中发生反应的化学反应方程式_____ 。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将___ (填“偏大”、“偏小”或“不受影响”)。

(1)A中试剂为
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;
②将B中剩余固体过滤,洗涤,干燥,称重;
③待B中不再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂;
上述操作的顺序是
(4)B中发生反应的化学反应方程式
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
更新时间:2021-06-24 17:38:08
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上可以利用含铝、铁、铜合金的废料获得的绿矾(FeSO4·7H2O)、胆矾等,甲同学设计的实验方案如下:

请回答:
(1)操作①、操作②所用的玻璃仪器是___________ ;沉淀C的化学式为________ 。
(2)为了检测滤液D中含有的金属离子,可设计实验方案为(试剂自选)__________ 。
(3)在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,其原因是________________ 。
(4)若考虑绿色化学工艺,在滤渣E中加入稀硫酸和H2O2制胆矾晶体,则反应④的离子化学方程式为________________________________ ;若不考虑绿色化学工艺,所选试剂Y为1mol/L HNO3,欲使3mol Cu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则需该硝酸的体积_________ L。

请回答:
(1)操作①、操作②所用的玻璃仪器是
(2)为了检测滤液D中含有的金属离子,可设计实验方案为(试剂自选)
(3)在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,其原因是
(4)若考虑绿色化学工艺,在滤渣E中加入稀硫酸和H2O2制胆矾晶体,则反应④的离子化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铝镁合金已成为轮船制造、化工生产等行业的重要材料。某研究性学习小组的三位同学为测定某含镁 的铝镁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白:
的铝镁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白:
探究一
实验方案:铝镁合金 测定剩余固体质量。
测定剩余固体质量。
(1)实验中发生反应的化学方程式是_______ 。
实验步骤:
(2)称取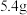 铝镁合金粉末样品,投入体积为V、浓度为
铝镁合金粉末样品,投入体积为V、浓度为 的
的 溶液中,充分反应。为保证合金充分反应,
溶液中,充分反应。为保证合金充分反应, 溶液的体积
溶液的体积
_______ 。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将_______ (填“偏大”或“偏小”)。
探究二
实验方案:铝镁合金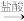 测定生成气体的体积(实验装置如图所示)。
测定生成气体的体积(实验装置如图所示)。

(4)某同学提出该实验装置不够完善,应在A、B之间添加一个除酸雾的装置。你的意见是_______ (填“需要”或“不需要”)。
(5)为使测定结果尽可能精确,实验中应注意的问题有(写出两点):①_______ ,②_______ 。
 的铝镁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白:
的铝镁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白:探究一
实验方案:铝镁合金
 测定剩余固体质量。
测定剩余固体质量。(1)实验中发生反应的化学方程式是
实验步骤:
(2)称取
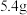 铝镁合金粉末样品,投入体积为V、浓度为
铝镁合金粉末样品,投入体积为V、浓度为 的
的 溶液中,充分反应。为保证合金充分反应,
溶液中,充分反应。为保证合金充分反应, 溶液的体积
溶液的体积
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
探究二
实验方案:铝镁合金
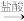 测定生成气体的体积(实验装置如图所示)。
测定生成气体的体积(实验装置如图所示)。
(4)某同学提出该实验装置不够完善,应在A、B之间添加一个除酸雾的装置。你的意见是
(5)为使测定结果尽可能精确,实验中应注意的问题有(写出两点):①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某铁的氧化物粉末可能含有FeO、 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
(已知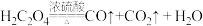 )
)

(1)装置甲的作用是______________________________ 。
(2)装置丁中的实验现象是______________________________________ 。
(3)若丙中铁的氧化物的化学式为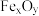 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为________ 。若丙中铁的氧化物质量为 3. 92 g,且完全反应,丁中生成沉淀的质量为13. 79 g,试确定该氧化物中x:y=_________ 。
(4)实验评价:该装置存在缺点__________ ,改进的方法________ 。
 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:(已知
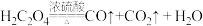 )
)
(1)装置甲的作用是
(2)装置丁中的实验现象是
(3)若丙中铁的氧化物的化学式为
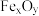 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为(4)实验评价:该装置存在缺点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】 是翠绿色晶体,见光易分解,是制备活性铁催化剂的主要原料。实验室制备该晶体并测定
是翠绿色晶体,见光易分解,是制备活性铁催化剂的主要原料。实验室制备该晶体并测定 含量的主要步骤如下。
含量的主要步骤如下。
Ⅰ.制备
取一定浓度的 溶液,恒温80℃、磁力搅拌下加入过量的6%
溶液,恒温80℃、磁力搅拌下加入过量的6% 溶液,再加入适量
溶液,再加入适量 的氨水,充分反应后过滤、洗涤。
的氨水,充分反应后过滤、洗涤。
Ⅱ.制备 晶体
晶体
80℃下,将 溶液缓慢滴入
溶液缓慢滴入 中,不断搅拌至固体完全溶解,将溶液蒸发浓缩、冷却,加入适量95%乙醇,置于暗处结晶,减压抽滤、洗涤、重结晶得翠绿色晶体。
中,不断搅拌至固体完全溶解,将溶液蒸发浓缩、冷却,加入适量95%乙醇,置于暗处结晶,减压抽滤、洗涤、重结晶得翠绿色晶体。
Ⅲ.测定晶体中 含量
含量
称量 样品于锥形瓶中,溶解后加稀硫酸酸化,用
样品于锥形瓶中,溶解后加稀硫酸酸化,用
 溶液滴定至终点,重复滴定两次,平均消耗
溶液滴定至终点,重复滴定两次,平均消耗 溶液
溶液 。
。
回答下列问题:
(1)由 晶体配制I中的
晶体配制I中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是___________ (填仪器名称)。

(2)Ⅰ中需控制温度80℃左右主要原因是___________ ,合适的加热方式是___________ 。
(3)Ⅰ中总反应的离子方程式为___________ 。
(4)Ⅱ中加入95%乙醇的作用是___________ ,该步骤中需控制“暗处结晶”的原因是___________ 。
(5)氧化还原滴定是常用的定量分析方法之一。
①实验Ⅲ中判断到达滴定终点的实验现象是___________ 。
②产品中 的质量分数为
的质量分数为___________ (用字母m、c和V的代数式表示)。若滴定前滴定管尖嘴内无气泡终点读数时有气泡,会使测定结果___________ (填“偏大”“偏小”或“无影响”)。
 是翠绿色晶体,见光易分解,是制备活性铁催化剂的主要原料。实验室制备该晶体并测定
是翠绿色晶体,见光易分解,是制备活性铁催化剂的主要原料。实验室制备该晶体并测定 含量的主要步骤如下。
含量的主要步骤如下。Ⅰ.制备

取一定浓度的
 溶液,恒温80℃、磁力搅拌下加入过量的6%
溶液,恒温80℃、磁力搅拌下加入过量的6% 溶液,再加入适量
溶液,再加入适量 的氨水,充分反应后过滤、洗涤。
的氨水,充分反应后过滤、洗涤。Ⅱ.制备
 晶体
晶体80℃下,将
 溶液缓慢滴入
溶液缓慢滴入 中,不断搅拌至固体完全溶解,将溶液蒸发浓缩、冷却,加入适量95%乙醇,置于暗处结晶,减压抽滤、洗涤、重结晶得翠绿色晶体。
中,不断搅拌至固体完全溶解,将溶液蒸发浓缩、冷却,加入适量95%乙醇,置于暗处结晶,减压抽滤、洗涤、重结晶得翠绿色晶体。Ⅲ.测定晶体中
 含量
含量称量
 样品于锥形瓶中,溶解后加稀硫酸酸化,用
样品于锥形瓶中,溶解后加稀硫酸酸化,用
 溶液滴定至终点,重复滴定两次,平均消耗
溶液滴定至终点,重复滴定两次,平均消耗 溶液
溶液 。
。回答下列问题:
(1)由
 晶体配制I中的
晶体配制I中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是
(2)Ⅰ中需控制温度80℃左右主要原因是
(3)Ⅰ中总反应的离子方程式为
(4)Ⅱ中加入95%乙醇的作用是
(5)氧化还原滴定是常用的定量分析方法之一。
①实验Ⅲ中判断到达滴定终点的实验现象是
②产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:

已知某些氢氧化物沉淀的pH如下表所示:
(1)MgO的电子式为__________ 。
(2)滤渣2的主要成分是__________ ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为__________ 。
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为__________ 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为______ 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为__________ (用含有a、b的代数式表示)。

已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 Al(OH)3 | 2.7 3.7 | 3.7 4.7 |
(2)滤渣2的主要成分是
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】【改编题】当你走进化学实验室时,首先要认真阅读并遵守《实验室安全守则》。以下实验室中的学生行为不符合实验室安全规范的是(回答两条即可):

(1)_____________________________________________________
(2)_____________________________________________________

(1)
(2)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】图1、图2分别是甲同学和乙同学设计的制溴苯的装置。已知制备溴苯的反应是放热反应。
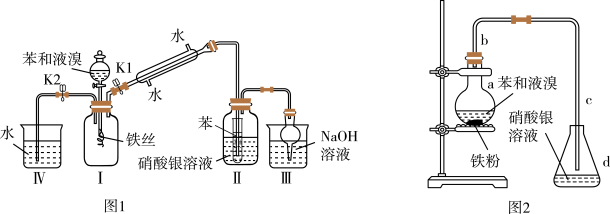
通过分析回答下列问题:
(1)实验室制溴苯的化学反应方程式为:________________________________ 。
(2)实验时,图1中看到的现象有:
①______________________________________________________ 。
②______________________________________________________ 。
(3)图2的操作和现象:
①中先关闭K2,开启K1和漏斗活塞滴加苯和液溴的混合液反应开始,观察到:____________________________________ 。
②关闭K1和漏斗活塞,开启K2发现___________________________________ 。
(4)比较两装置,图2优于图1有(答出主要的三点):
①______________________________________________________ 。
②______________________________________________________ 。
③______________________________________________________ 。

通过分析回答下列问题:
(1)实验室制溴苯的化学反应方程式为:
(2)实验时,图1中看到的现象有:
①
②
(3)图2的操作和现象:
①中先关闭K2,开启K1和漏斗活塞滴加苯和液溴的混合液反应开始,观察到:
②关闭K1和漏斗活塞,开启K2发现
(4)比较两装置,图2优于图1有(答出主要的三点):
①
②
③
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氨基甲酸铵(NH2COONH4)是一种白色固体,易分解,易水解,可用作肥料、灭火剂、洗涤剂等。实验室制备氨基甲酸铵的反应如下:2NH3(g)+CO2(g)  NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:

步骤1:按图连接好实验装置,____________________ 。
步骤2:在相应仪器中装入药品,其中1在三颈烧瓶中加入足量的氢氧化钠固体,在恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品。
……
请回答下列问题:
(1)将步骤1补充完整:________________________
(2)干燥管中盛放的药品是___________________________
(3)对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有____________________ (写出一种即可)。
(4)三颈烧瓶中产生氨气的原理是________________________________ 。
(5)反应后期随着产生CO2气流减慢,导致反应物比例不当,可采取的措施是________________ 。
(6)尾气处理装置中双通玻璃管的作用是_________________ (用文字叙述),浓硫酸的作用是_______________ 、______________ 。
(7)取部分变质(混有碳酸氢铵的氨基甲酸铵)样品1.173g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。则样品中氨基甲酸铵的物质的量分数为___________ 。
 NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
步骤1:按图连接好实验装置,
步骤2:在相应仪器中装入药品,其中1在三颈烧瓶中加入足量的氢氧化钠固体,在恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品。
……
请回答下列问题:
(1)将步骤1补充完整:
(2)干燥管中盛放的药品是
(3)对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有
(4)三颈烧瓶中产生氨气的原理是
(5)反应后期随着产生CO2气流减慢,导致反应物比例不当,可采取的措施是
(6)尾气处理装置中双通玻璃管的作用是
(7)取部分变质(混有碳酸氢铵的氨基甲酸铵)样品1.173g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。则样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】立方晶系二元合金
有一立方晶系二元合金,单胞参数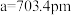 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体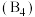 ,已知晶胞中
,已知晶胞中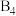 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
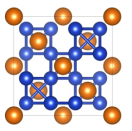
(1)写出二元合金的化学式_______ 。
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度_______ 。
(3)晶胞的单位点阵型式_______ 。
(4)实际上,大部分该类结构二元合金的原子半径比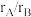 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和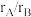 值
值_______ 、_______ 。
有一立方晶系二元合金,单胞参数
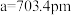 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体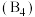 ,已知晶胞中
,已知晶胞中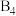 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
(1)写出二元合金的化学式
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度
(3)晶胞的单位点阵型式
(4)实际上,大部分该类结构二元合金的原子半径比
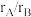 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和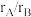 值
值
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】合金A由四种单质组成,已知:①合金A中不含K、Ca、Na;②气体B可燃;③气体G为人体新陈代谢的主要产物之一,请据图回答以下问题:

(1)合金A由哪些单质组成(用化学式表示):_____ 、_______ 、________ 、________ ;
(2)写出反应①的化学方程式:______________ ;
(3)写出反应②的化学方程式:__________________ 。

(1)合金A由哪些单质组成(用化学式表示):
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)在700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2 > t1):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2 > t1):
①反应在t1min内的平均速率:v(H2)=____ mol·L-1·min-1。
②t2时刻,该反应的正反应速率___ 逆反应速率(填“大于”、“小于”或“等于”)。
(2)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。
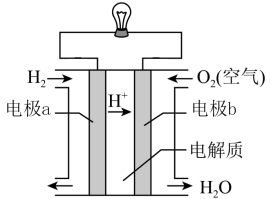
①该电池供电时,____ 能转化为____ 能。
②写出该电池供电时的总反应方程式________ 。
③电极b上发生______ 反应(“氧化”或“还原”)。
④在外电路中,电子流动的方向为________ 。
(3)镁铝合金(Mg17Al10)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al10+17H2=17MgH2+10Al。得到的混合物Y(17MgH2+10Al)在一定条件下可释放出氢气。
①镁铝合金的熔点比金属镁的熔点______ 。(填“高”或“低”)
②在6.0 mol·L-1 HCl溶液中,混合物Y能完全释放出H2。1 mol Mg17Al10完全吸氢后得到的混合物Y与足量上述盐酸完全反应,释放出H2的物质的量为______ 。
(1)在700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)
 CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2 > t1):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2 > t1):| 反应时间/min | 0 | t1 | t2 |
| n(CO)/mol | 1.20 | 0.80 | 0.80 |
②t2时刻,该反应的正反应速率
(2)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。

①该电池供电时,
②写出该电池供电时的总反应方程式
③电极b上发生
④在外电路中,电子流动的方向为
(3)镁铝合金(Mg17Al10)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al10+17H2=17MgH2+10Al。得到的混合物Y(17MgH2+10Al)在一定条件下可释放出氢气。
①镁铝合金的熔点比金属镁的熔点
②在6.0 mol·L-1 HCl溶液中,混合物Y能完全释放出H2。1 mol Mg17Al10完全吸氢后得到的混合物Y与足量上述盐酸完全反应,释放出H2的物质的量为
您最近一年使用:0次



