水合氧化铁[FeO(OH)]是一种重要的化工原料,用作磁性材料、颜料铁黄等.一种以硫铁矿烧渣(含Fe、FeO、SiO2和少量CuO)为原料生产FeO(OH)的工艺流程如下:
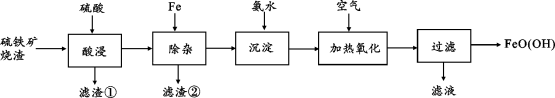
回答下列问题:
(1)“酸浸”时CuO与硫酸发生反应的离子方程式为_______
(2)“除杂”时滤渣②的成分有Fe和_______
(3)常温时,当“沉淀”后溶液中的Fe2+浓度为8.0×10-6mol·L-1时,溶液的pH=_______ {Ksp[Fe(OH)2]=8.0×10-16}。
(4)“加热氧化”的化学方程式为_______ 。
(5)“过滤”后需洗涤FeO(OH)沉淀,请设计实验检验FeO(OH)沉淀是否洗涤干净_______ 。

回答下列问题:
(1)“酸浸”时CuO与硫酸发生反应的离子方程式为
(2)“除杂”时滤渣②的成分有Fe和
(3)常温时,当“沉淀”后溶液中的Fe2+浓度为8.0×10-6mol·L-1时,溶液的pH=
(4)“加热氧化”的化学方程式为
(5)“过滤”后需洗涤FeO(OH)沉淀,请设计实验检验FeO(OH)沉淀是否洗涤干净
更新时间:2021-07-15 10:01:44
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】以黄铁矿(主要成分为FeS2)为原料制备绿矾晶体(FeSO4·7H2O)的工艺流程如下:

回答下列问题;
(1)焙烧时黄铁矿要粉碎,其目的是___________ 。焙烧后得到的固体主要成分为Fe2O3,写出焙烧过程主要反应的化学方程式___________ 。
(2)试剂X是___________ (填化学式)。
(3)SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式___________ 。
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4·7H2O)的操作:___________ 、___________ 、过滤、洗涤、干燥。
(5)绿帆晶体在空气中易被氧化。取m g样品加水完全溶解,该样品溶液恰好可以与VmLc mol/L的酸性KMnO4溶液反应。则该样品溶液与酸性KMnO4溶液反应的离子方程式为:___________ ,硫酸亚铁晶体纯度的计算式为:___________ (写出计算式即可,无需化简)。(FeSO4·7H2O摩尔质量为278 g/mol)

回答下列问题;
(1)焙烧时黄铁矿要粉碎,其目的是
(2)试剂X是
(3)SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4·7H2O)的操作:
(5)绿帆晶体在空气中易被氧化。取m g样品加水完全溶解,该样品溶液恰好可以与VmLc mol/L的酸性KMnO4溶液反应。则该样品溶液与酸性KMnO4溶液反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】利用炼铝厂的废料—铝灰(含 、
、 及少量
及少量 和
和 、
、 )回收少量铝。有关工艺流程如下:
)回收少量铝。有关工艺流程如下:
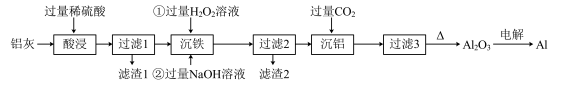
已知: 是酸性氧化物;
是酸性氧化物; 具有粘合性;
具有粘合性;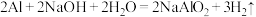
回答下列问题:
(1)“酸浸”操作后溶液中含有的阳离子为___________ (填离子符号)。
(2)滤渣1的主要成分是___________ (填化学式)。
(3)“沉铁”时加入过量 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为___________ 。
(4)“沉铁”时加入过量NaOH溶液的主要目的是沉淀铁,有同学提出在“酸浸”时将稀硫酸替换成为NaOH溶液,这样就无需进行“沉铁”操作,你认为先进行“酸浸”再进行“沉铁”的原因为___________ 。
(5)“沉铝”时发生反应的化学方程式为___________ 。
(6)工业通过电解的方法得到铝,通常在电解时会加入冰晶石,加入冰晶石的目的是___________ ;若回收1tAl,在电解 生产过程中Al的损失率为10%,则消耗的
生产过程中Al的损失率为10%,则消耗的 的质量为
的质量为___________ t(结果保留2位有效数字)。
 、
、 及少量
及少量 和
和 、
、 )回收少量铝。有关工艺流程如下:
)回收少量铝。有关工艺流程如下:
已知:
 是酸性氧化物;
是酸性氧化物; 具有粘合性;
具有粘合性;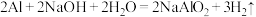
回答下列问题:
(1)“酸浸”操作后溶液中含有的阳离子为
(2)滤渣1的主要成分是
(3)“沉铁”时加入过量
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)“沉铁”时加入过量NaOH溶液的主要目的是沉淀铁,有同学提出在“酸浸”时将稀硫酸替换成为NaOH溶液,这样就无需进行“沉铁”操作,你认为先进行“酸浸”再进行“沉铁”的原因为
(5)“沉铝”时发生反应的化学方程式为
(6)工业通过电解的方法得到铝,通常在电解时会加入冰晶石,加入冰晶石的目的是
 生产过程中Al的损失率为10%,则消耗的
生产过程中Al的损失率为10%,则消耗的 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
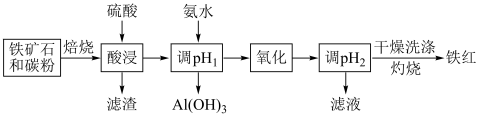
【推荐1】一种以赤铁矿(主要含有Fe2O3,含少量Al2O3、CaO等)为原料制备高纯度铁红的流程如下:
(1)“酸浸”时,Al2O3发生反应的离子方程式是___________ 。
(2)“酸浸”后的实验操作名称是___________ ,滤渣的主要成分是___________ 。
(3)“调pH1”不能用氢氧化钠溶液代替氨水的原因是___________ 。
(4)“氧化”时可选用多种氧化剂,若选择氯水,反应的离子方程式为___________ 。
(5)“氧化”后如何检验氧化产物,操作步骤是___________ 。
(6)灼烧时发生反应的化学方程式为___________ 。
(7)写出铁红在生产生活中的一种用途___________ 。
(1)“酸浸”时,Al2O3发生反应的离子方程式是
(2)“酸浸”后的实验操作名称是
(3)“调pH1”不能用氢氧化钠溶液代替氨水的原因是
(4)“氧化”时可选用多种氧化剂,若选择氯水,反应的离子方程式为
(5)“氧化”后如何检验氧化产物,操作步骤是
(6)灼烧时发生反应的化学方程式为
(7)写出铁红在生产生活中的一种用途
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NaHCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。

如果此方案正确,那么:
(1)操作④为________ ,操作①、④、⑤都用到的玻璃仪器有____________ 。
(2)操作②为什么不用硝酸钡溶液,其理由是___________________________________ 。
(3)进行操作②后,如何判断SO42-已除尽,方法是_____________________________________ 。
(4)操作③的目的是____________ ,为什么不先过滤后加碳酸钠溶液?理由是____________ 。
(5)操作⑤的目的是_______________________________________________________ 。

如果此方案正确,那么:
(1)操作④为
(2)操作②为什么不用硝酸钡溶液,其理由是
(3)进行操作②后,如何判断SO42-已除尽,方法是
(4)操作③的目的是
(5)操作⑤的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】3-苯基乳酸是一些重要的化学合成物的前体,并广泛应用于医药、化工、生物合成等领域,可作为日常食品的防腐剂。实验室通过苯丙氨酸的重氮化及水解反应制取3-苯基乳酸,方法如下:
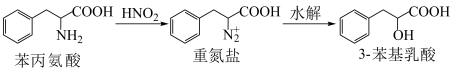
已知:HNO2(M=47)为弱酸,不稳定,遇热即分解,水溶液无色;苯丙氨酸(M=165)为白色固体,溶于水,熔点283℃;3−苯基乳酸(M=166)为白色晶体,微溶于水,易溶于有机溶剂,熔点121~126℃。
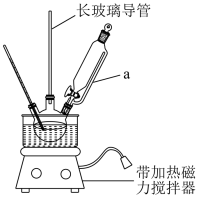
实验步骤:
①三颈烧瓶中加入6.0g苯丙氨酸,再加入70mL稀硫酸,冷却至5℃,边搅拌边滴加60mLNaNO2溶液(0.1g·mL-1),维持温度搅拌50min,然后改成35℃热水浴再搅拌10min。
②往烧瓶中加入25mL乙酸乙酯,搅拌后将混合液中的水分离,进一步提纯得到粗产品5.0g。
③取粗产品0.5g于锥形瓶中,加入1mL95%的乙醇,溶解后再加入25mL蒸馏水、2滴酚酞试剂,用0.1mol·L-1NaOH标准溶液滴定至终点,重复3次实验,平均消耗V(NaOH)=28.10mL。
(1)仪器a的名称为___________ ,配制60mL0.1g·mL-1NaNO2溶液需要的玻璃仪器有___________ 、胶头滴管、玻璃棒、烧杯。
(2)加入稀硫酸的作用是___________ ,生成重氮盐之前涉及反应的化学方程式为___________ 。
(3)步骤①中先在5℃下搅拌50min,采用较低温度较长时间反应的原因是___________ 。
(4)步骤②中乙酸乙酯的作用是___________ ,后续提纯粗产品的方法是___________ 。
(5)判断滴定终点的现象是___________ 粗产品的纯度是___________ (保留3位有效数字)。

已知:HNO2(M=47)为弱酸,不稳定,遇热即分解,水溶液无色;苯丙氨酸(M=165)为白色固体,溶于水,熔点283℃;3−苯基乳酸(M=166)为白色晶体,微溶于水,易溶于有机溶剂,熔点121~126℃。

实验步骤:
①三颈烧瓶中加入6.0g苯丙氨酸,再加入70mL稀硫酸,冷却至5℃,边搅拌边滴加60mLNaNO2溶液(0.1g·mL-1),维持温度搅拌50min,然后改成35℃热水浴再搅拌10min。
②往烧瓶中加入25mL乙酸乙酯,搅拌后将混合液中的水分离,进一步提纯得到粗产品5.0g。
③取粗产品0.5g于锥形瓶中,加入1mL95%的乙醇,溶解后再加入25mL蒸馏水、2滴酚酞试剂,用0.1mol·L-1NaOH标准溶液滴定至终点,重复3次实验,平均消耗V(NaOH)=28.10mL。
(1)仪器a的名称为
(2)加入稀硫酸的作用是
(3)步骤①中先在5℃下搅拌50min,采用较低温度较长时间反应的原因是
(4)步骤②中乙酸乙酯的作用是
(5)判断滴定终点的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】I.回答下列问题
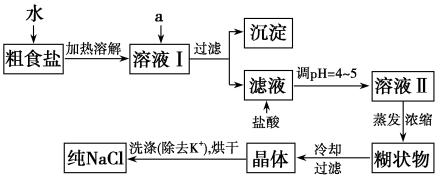
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO ,选出a所代表的试剂,按滴加顺序依次为
,选出a所代表的试剂,按滴加顺序依次为___________ (只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为___________ 。
Ⅱ.工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如图:
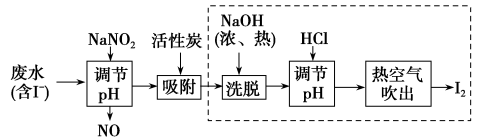
(2)向废水中加入NaNO2并调节pH<4,写出此反应的离子方程式:___________ 。
(3)写出该流程加入HCl调节pH发生的反应的离子方程式:___________ 。
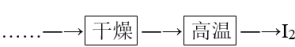
(4)工业上虚线框内流程还可用下图操作代替,试评价图中替代流程的优点:___________ (写出一条即可)。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO
 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO
 ,选出a所代表的试剂,按滴加顺序依次为
,选出a所代表的试剂,按滴加顺序依次为②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
Ⅱ.工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如图:

(2)向废水中加入NaNO2并调节pH<4,写出此反应的离子方程式:
(3)写出该流程加入HCl调节pH发生的反应的离子方程式:
(4)工业上虚线框内流程还可用下图操作代替,试评价图中替代流程的优点:

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】纯碱是一种非常重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A 的方法是_______ ,得到的NaHCO3晶体中可能含有少量NaCl、NH4Cl等杂质,检验该晶体中是否含有氯离子杂质的操作方法是_______ 。
②该工艺流程中可回收再利用的物质是_______ 。
(2)若称取10.5 g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02 g。如果把剩余的固体全部加入到100 mL 2 mol·L-1的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度(设溶液的体积变化及盐酸的挥发忽略不计)(写出计算过程)。_______
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A 的方法是
②该工艺流程中可回收再利用的物质是
(2)若称取10.5 g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02 g。如果把剩余的固体全部加入到100 mL 2 mol·L-1的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度(设溶液的体积变化及盐酸的挥发忽略不计)(写出计算过程)。
您最近一年使用:0次
【推荐3】氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
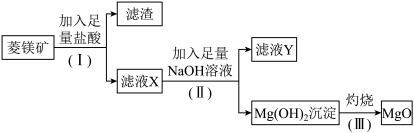
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是_________ ,所使用的玻璃仪器有__________ 烧杯、玻璃棒。
(2)步骤(Ⅰ)中分离出的滤渣主要含有___________ ,它属于_________ (填“酸性”或“碱性”)氧化物。
(3)滤液Y中的阴离子除了含 、
、 外还有
外还有_________ (填离子符号);若步骤(Ⅱ)中加入的NaOH溶液不足量,则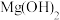 沉淀中混有的杂质是
沉淀中混有的杂质是_________ (填化学式)。
(4)写出步骤(Ⅲ)中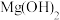 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式_____________ 。
 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(Ⅰ)中分离出的滤渣主要含有
(3)滤液Y中的阴离子除了含
 、
、 外还有
外还有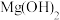 沉淀中混有的杂质是
沉淀中混有的杂质是(4)写出步骤(Ⅲ)中
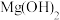 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】实验室合成三苯基膦(C6H5)3P,并从反应后的废渣中获取MgCl2∙6H2O。
I.合成三苯基膦(C6H5)3P
反应装置如图所示(夹持仪器已略去)。先向三颈烧瓶中加入氯苯和溶剂(四氢呋喃),然后加入镁屑,反应制得C6H5MgCl;再从滴液漏斗中缓慢加入PCl3,控制反应温度在40~50℃。
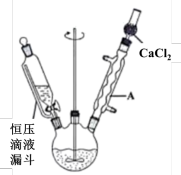
相关物质的部分性质如下表:
(1)装置中仪器A的名称为________ 。与普通分液漏斗比较,使用恒压滴液漏斗的优点是:使漏斗内液体顺利滴下、__________ 。
(2)实验宜使用的加热方法为_________ 。
II.获取MgCl2∙6H2O
提取(C6H5)3P后的废渣中含MgCl2、四氢呋喃、(C6H5)3P等。以该废渣为原料,获取MgCl2∙6H2O的主要实验流程如下:

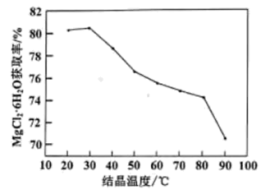
(3)其他条件相同时,水浸相同时间,水浸温度与MgCl2∙6H2O获取率关系如下图所示,分析曲线在不同温度段趋势变化的原因:A→B段_______ ;D→E段______ 。

(4)过滤后得到的滤液中主要含MgCl2、四氢呋喃。结晶温度与MgCl2∙6H2O回收率的关系如下图所示。补充完整获取MgCl2∙6H2O的实验方案:取酸浸后滤液,_____ 。
I.合成三苯基膦(C6H5)3P
反应装置如图所示(夹持仪器已略去)。先向三颈烧瓶中加入氯苯和溶剂(四氢呋喃),然后加入镁屑,反应制得C6H5MgCl;再从滴液漏斗中缓慢加入PCl3,控制反应温度在40~50℃。

相关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 部分性质 |
三苯基膦 | 78.5 | 377 | 与水剧烈反应 |
四氢呋喃 | −108.5 | 65.4 | 对环境有污染 |
三氯化磷 | −111.8 | 76 | 与水剧烈反应 |
(2)实验宜使用的加热方法为
II.获取MgCl2∙6H2O
提取(C6H5)3P后的废渣中含MgCl2、四氢呋喃、(C6H5)3P等。以该废渣为原料,获取MgCl2∙6H2O的主要实验流程如下:

(3)其他条件相同时,水浸相同时间,水浸温度与MgCl2∙6H2O获取率关系如下图所示,分析曲线在不同温度段趋势变化的原因:A→B段

(4)过滤后得到的滤液中主要含MgCl2、四氢呋喃。结晶温度与MgCl2∙6H2O回收率的关系如下图所示。补充完整获取MgCl2∙6H2O的实验方案:取酸浸后滤液,

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】过氧化钙晶体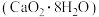 为白色固体,难溶于水,可做分析试剂、消毒剂等。制备
为白色固体,难溶于水,可做分析试剂、消毒剂等。制备 晶体的装置如下图所示。回答相关问题:
晶体的装置如下图所示。回答相关问题:___________ 。
(2)B中反应需在0℃~3℃的温度下进行,B可采用的降温方式为___________ 。B中发生的离子反应方程式为___________ 。
(3)C管起到平衡气压的作用,加水液封的目的是___________ 。
(4)该实验装置还需要在AB之间增加一个装置,其作用是___________ 。
(5)碘量法测定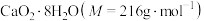 的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用
的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用 的
的 溶液滴定至终点,终点溶液颜色变化为
溶液滴定至终点,终点溶液颜色变化为___________ ,重复操作2次,三次平均消耗 溶液体积为15.00mL,则
溶液体积为15.00mL,则 的质量分数为
的质量分数为___________ %。
已知: ;
; 。
。
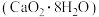 为白色固体,难溶于水,可做分析试剂、消毒剂等。制备
为白色固体,难溶于水,可做分析试剂、消毒剂等。制备 晶体的装置如下图所示。回答相关问题:
晶体的装置如下图所示。回答相关问题: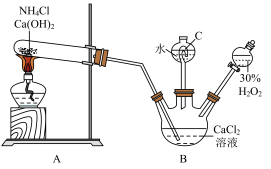
(2)B中反应需在0℃~3℃的温度下进行,B可采用的降温方式为
(3)C管起到平衡气压的作用,加水液封的目的是
(4)该实验装置还需要在AB之间增加一个装置,其作用是
(5)碘量法测定
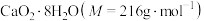 的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用
的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用 的
的 溶液滴定至终点,终点溶液颜色变化为
溶液滴定至终点,终点溶液颜色变化为 溶液体积为15.00mL,则
溶液体积为15.00mL,则 的质量分数为
的质量分数为已知:
 ;
; 。
。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】碘化钠可用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等。某探究小组利用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
[实验一]制备NaClO溶液
实验装置如图所示:

(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有__ (填序号)。
A.烧杯 B.容量瓶 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是___ 。
[实验二]制取水合肼。
制备原理:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
实验装置如图所示:
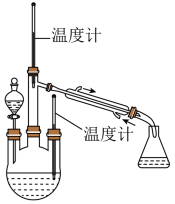
控制反应温度,将分液漏斗中的溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108℃~114℃馏分。
(3)分液漏斗中的溶液是__ (填序号)。选择的理由是__ 。
A.NaOH和NaClO混合溶液
B.CO(NH2)2溶液
[实验三]制备碘化钠
探究小组用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。其步骤如下:
(4)步骤一:向三颈烧瓶中加入过量的NaOH及水,搅拌、冷却,再加入碘单质,打开恒温磁力搅拌器,保持60℃~70℃至反应完全;观察到的现象是___ 。
(5)步骤二:继续加入稍过量的N2H4•H2O,还原NaIO和NaIO3,得NaI溶液粗品;向上述反应液中加入活性炭,煮沸半小时,然后将溶液与活性炭分离,分离的方法是___ 。
(6)步骤三:将步骤二中分离出的溶液__ 、__ 、过滤、洗涤、干燥,得产品。
(7)某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉溶液后再滴加适量稀硫酸,片刻后溶液变蓝,由此得出NaI中含有NaIO3杂质。请评价该实验结论的合理性:___ (填“合理”或“不合理”)。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
[实验一]制备NaClO溶液
实验装置如图所示:

(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有
A.烧杯 B.容量瓶 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是
[实验二]制取水合肼。
制备原理:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
实验装置如图所示:

控制反应温度,将分液漏斗中的溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108℃~114℃馏分。
(3)分液漏斗中的溶液是
A.NaOH和NaClO混合溶液
B.CO(NH2)2溶液
[实验三]制备碘化钠
探究小组用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。其步骤如下:
(4)步骤一:向三颈烧瓶中加入过量的NaOH及水,搅拌、冷却,再加入碘单质,打开恒温磁力搅拌器,保持60℃~70℃至反应完全;观察到的现象是
(5)步骤二:继续加入稍过量的N2H4•H2O,还原NaIO和NaIO3,得NaI溶液粗品;向上述反应液中加入活性炭,煮沸半小时,然后将溶液与活性炭分离,分离的方法是
(6)步骤三:将步骤二中分离出的溶液
(7)某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉溶液后再滴加适量稀硫酸,片刻后溶液变蓝,由此得出NaI中含有NaIO3杂质。请评价该实验结论的合理性:
您最近一年使用:0次

 ·
· 晶体。具体的流程如下:
晶体。具体的流程如下:
 、
、

