工业制硫酸的反应之一为:2SO2(g)+O2(g) 2SO3(g),在2 L恒温恒容密闭容器中投入2 mol SO2和1mol O2在一定条件下充分反应,下图是SO2和SO3随时间的变化曲线。
2SO3(g),在2 L恒温恒容密闭容器中投入2 mol SO2和1mol O2在一定条件下充分反应,下图是SO2和SO3随时间的变化曲线。

(1)前10min SO3的平均反应速率为___________ ;平衡时,SO2转化率为___________ 。
(2)下列叙述不能判断该反应达到平衡状态的是___________ ;
①容器中压强不再改变;
②容器中气体密度不再改变;
③SO3的质量不再改变;
④O2的物质的量浓度不再改变;
⑤容器内气体原子总数不再发生变化;
(3)以下操作会引起化学反应速率变快的是__ 。
A.向容器中通入氦气
B.升高温度
C.扩大容器的体积
D.向容器中通入O2
E.使用正催化剂
(4)反应达平衡时,体系的压强与开始时的压强之比为____ ;容器内混合气体的平均相对分子质量和起始投料时相比____ (填“增大”“减小”或“不变”)。
 2SO3(g),在2 L恒温恒容密闭容器中投入2 mol SO2和1mol O2在一定条件下充分反应,下图是SO2和SO3随时间的变化曲线。
2SO3(g),在2 L恒温恒容密闭容器中投入2 mol SO2和1mol O2在一定条件下充分反应,下图是SO2和SO3随时间的变化曲线。
(1)前10min SO3的平均反应速率为
(2)下列叙述不能判断该反应达到平衡状态的是
①容器中压强不再改变;
②容器中气体密度不再改变;
③SO3的质量不再改变;
④O2的物质的量浓度不再改变;
⑤容器内气体原子总数不再发生变化;
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气
B.升高温度
C.扩大容器的体积
D.向容器中通入O2
E.使用正催化剂
(4)反应达平衡时,体系的压强与开始时的压强之比为
更新时间:2021-07-17 09:55:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:

(1)反应的化学方程式为_______ 。
(2)反应达到化学平衡的时间内的平均反应速率v(N)=_______ 。
(3)4min时,正、逆反应速率的大小关系为v正_______ v逆(填“>”“<”或“=”);
(4)一定温度下,将一定量的N2和H2充入固定容积催化剂的密闭容器中进行反应:N2(g)+3H2(g)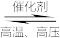 2NH3(g)。下列描述能说明该可逆反应达到化学平衡状态的有
2NH3(g)。下列描述能说明该可逆反应达到化学平衡状态的有_______ (填序号)。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3molH-H键断裂,有6molN-H键形成
D.c(N2)︰c(H2)︰c(NH3)=1︰3︰2
E.NH3的质量分数不再改变
(5)能加快反应速率的措施是_______ (填序号)
①升高温度
②容器容积不变,充入惰性气体Ar
③容器压强不变,充入惰性气体Ar
④使用催化剂

(1)反应的化学方程式为
(2)反应达到化学平衡的时间内的平均反应速率v(N)=
(3)4min时,正、逆反应速率的大小关系为v正
(4)一定温度下,将一定量的N2和H2充入固定容积催化剂的密闭容器中进行反应:N2(g)+3H2(g)
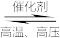 2NH3(g)。下列描述能说明该可逆反应达到化学平衡状态的有
2NH3(g)。下列描述能说明该可逆反应达到化学平衡状态的有A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3molH-H键断裂,有6molN-H键形成
D.c(N2)︰c(H2)︰c(NH3)=1︰3︰2
E.NH3的质量分数不再改变
(5)能加快反应速率的措施是
①升高温度
②容器容积不变,充入惰性气体Ar
③容器压强不变,充入惰性气体Ar
④使用催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下列关于H2S和SO2的说法正确的是______________
A.两气体都可用浓硫酸干燥
B.两气体均可以用NaOH溶液吸收
C.两气体按体积比1:2混合可完全转化为S
D.将两气体通入溴水或酸性KMnO4溶液中,可通过颜色变化鉴别两气体
(2)目前治理汽车尾气是在催化剂条件下发生反应2NO+2CO N2+2CO2,现在实验室模拟上述反应,已知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
N2+2CO2,现在实验室模拟上述反应,已知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
①这段时间内CO的反应速率为_________________ 。
②该反应平衡常数______________ (保留两位有效数字)。
③平衡后再向密闭容器通入0.4molCO和0.4molCO2,平衡将_____________ (填“正向”、“逆向”或“不”)移动。判断理由是_________________ 。
④若升温发现体系气体平均相对分子质量增大,则该反应的△H______ 0(填“>”、“<”或“=”)。
⑤维持条件不变,向平衡后的容器再充入0.2molNO和0.1molCO,达到新平衡,则与原平衡相比NO的转化率____________ (填“增大”、“减小”或“不变”)。
A.两气体都可用浓硫酸干燥
B.两气体均可以用NaOH溶液吸收
C.两气体按体积比1:2混合可完全转化为S
D.将两气体通入溴水或酸性KMnO4溶液中,可通过颜色变化鉴别两气体
(2)目前治理汽车尾气是在催化剂条件下发生反应2NO+2CO
 N2+2CO2,现在实验室模拟上述反应,已知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
N2+2CO2,现在实验室模拟上述反应,已知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:①这段时间内CO的反应速率为
②该反应平衡常数
③平衡后再向密闭容器通入0.4molCO和0.4molCO2,平衡将
④若升温发现体系气体平均相对分子质量增大,则该反应的△H
⑤维持条件不变,向平衡后的容器再充入0.2molNO和0.1molCO,达到新平衡,则与原平衡相比NO的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】油气开采、石油化工等行业废气含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H=+94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)=S2(g)+2H2(g)的∆H4=___________  。
。
(2)较普遍采用的H2S处理方法是克劳斯工艺,即利用反应①和②生成单质硫。另一种方法是利用反应④高温热分解H2S。相比克劳斯工艺,高温热分解方法的优点是___________ ,缺点是___________ 。
(3)在1470K、100Kpa反应条件下,将n(H2S)∶n(Ar)=1:4的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为___________ ,平衡常数Kp=___________ Kpa.(以分压表示,分压=总压×物质的量分数,结果保留两位小数)
(4)在1373K、100Kpa反应条件下,对于n(H2S)∶n(Ar)分别为4:1、1:1、1:4、1:9、1:19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如下图所示。
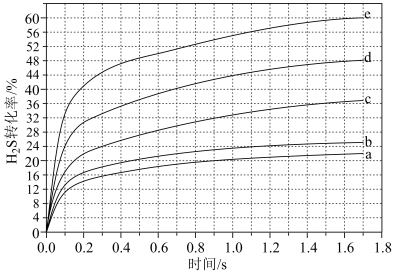
①n(H2S)∶n(Ar)越小,H2S平衡转化率___________ ,理由是___________ 。
②n(H2S)∶n(Ar)=1∶9对应图中曲线d,此时H2S的转化率为24%,则在0―0.1s之间H2S分压的平均变化率为___________ Kpa·s-1。
(1)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H=+94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)=S2(g)+2H2(g)的∆H4=
 。
。(2)较普遍采用的H2S处理方法是克劳斯工艺,即利用反应①和②生成单质硫。另一种方法是利用反应④高温热分解H2S。相比克劳斯工艺,高温热分解方法的优点是
(3)在1470K、100Kpa反应条件下,将n(H2S)∶n(Ar)=1:4的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为
(4)在1373K、100Kpa反应条件下,对于n(H2S)∶n(Ar)分别为4:1、1:1、1:4、1:9、1:19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如下图所示。

①n(H2S)∶n(Ar)越小,H2S平衡转化率
②n(H2S)∶n(Ar)=1∶9对应图中曲线d,此时H2S的转化率为24%,则在0―0.1s之间H2S分压的平均变化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(一)一种工业制硝酸的方法经历下列几个步骤:
 △H1<0
△H1<0
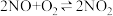 △H2<0
△H2<0
 △H3<0
△H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_______________ 目的;
(2)实验发现,单位时间内NH3的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因________________ 。

(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: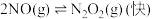 △H1<0
△H1<0

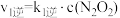
反应Ⅱ: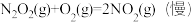 △H2<0
△H2<0
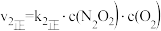
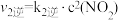
①一定条件下,反应 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=________________ 。(用含k1正、k1逆、k2正、k2逆的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为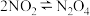 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
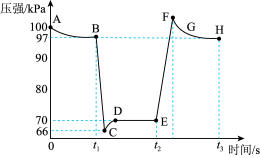
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是_______________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=_______________ (不必化成小数);
(6)图像中C、E两点气体平均摩尔质量最大的点为_______________ (填代号)。
 △H1<0
△H1<0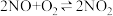 △H2<0
△H2<0 △H3<0
△H3<0已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[
 ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
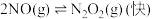 △H1<0
△H1<0 
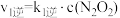
反应Ⅱ:
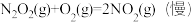 △H2<0
△H2<0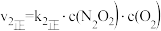
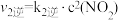
①一定条件下,反应
 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为
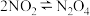 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=
(6)图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为2 mol、B为5 mol,5 min末时达到化学平衡状态,此时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
3C(g)+nD(g),开始时A为2 mol、B为5 mol,5 min末时达到化学平衡状态,此时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
(1)5 min末A的物质的量浓度为______________ 。
(2)前5 min内用B表示的化学反应速率v(B)为______________ 。
(3)化学方程式中n值为______________ 。
(4)平衡时B的转化率为______________ 。
(5)反应开始时与达到平衡后容器中压强之比为______________ 。
 3C(g)+nD(g),开始时A为2 mol、B为5 mol,5 min末时达到化学平衡状态,此时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
3C(g)+nD(g),开始时A为2 mol、B为5 mol,5 min末时达到化学平衡状态,此时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。(1)5 min末A的物质的量浓度为
(2)前5 min内用B表示的化学反应速率v(B)为
(3)化学方程式中n值为
(4)平衡时B的转化率为
(5)反应开始时与达到平衡后容器中压强之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】反应aA(g)+bB(g) cC(g)(△H<0)在恒容条件下进行。改变其它反应条件,在I、II、III阶段中各物质浓度随时间变化的曲线如图所示:
cC(g)(△H<0)在恒容条件下进行。改变其它反应条件,在I、II、III阶段中各物质浓度随时间变化的曲线如图所示:
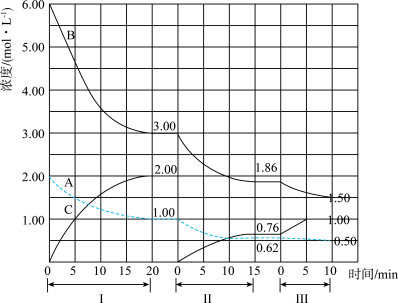
(1)化学方程式中a:b:c=___ 。
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小的排列顺序为___ 。
(3)B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是___ ,其值是___ (保留2位有效数字)。
(4)由第一次平衡到第二次平衡,平衡向___ (填“左”或“右”)移动,采取的措施是___ 。
(5)其他条件不变,只改变温度,则第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低T2___ T3(填“<”“>”或“=”),判断的理由是___ 。
 cC(g)(△H<0)在恒容条件下进行。改变其它反应条件,在I、II、III阶段中各物质浓度随时间变化的曲线如图所示:
cC(g)(△H<0)在恒容条件下进行。改变其它反应条件,在I、II、III阶段中各物质浓度随时间变化的曲线如图所示:
(1)化学方程式中a:b:c=
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小的排列顺序为
(3)B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡向
(5)其他条件不变,只改变温度,则第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低T2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的 NO 和 NH3,在 一定条件下发生反应:6NO(g) + 4NH3(g) 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是___________
a.反应速率 v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内 N2的物质的量分数不再随时间而发生变化
d.容器内 n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
e.12molN-H 键断裂的同时生成 5mol N≡N 键
f.混合气体的总质量不随时间的变化而变化
②某次实验中测得容器内 NO 及 N2的物质的量随时间变化如图所示,图中 b 点 对应的速率关系是v(正)___________ v(逆)(填﹥、﹤或﹦),d 点对应的速率关系是v(正) ___________ v(逆)
(填﹥、﹤或﹦)。

(2)298 K 时,若已知生成标准状况下 2.24LNH3时放出热量为 4.62kJ。写出合成氨反应的热化学方程式___________ 。在该温度下,取 1molN2和 3mol H2 放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于 92.4 kJ, 其原因是___________ 。
(3)一定条件下,在 2L密闭容器内,反应 2NO2(g) N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
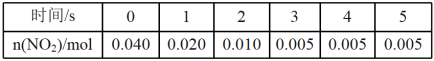
①用 N2O4 表示 0~2 s 内该反应的平均速率为__________ 。在第 5s 时,NO2的转化 率为____________ 。(转化率是指某一反应物转化的百分率。)
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是______________ 。
 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。①能说明该反应已达到平衡状态的标志是
a.反应速率 v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内 N2的物质的量分数不再随时间而发生变化
d.容器内 n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
e.12molN-H 键断裂的同时生成 5mol N≡N 键
f.混合气体的总质量不随时间的变化而变化
②某次实验中测得容器内 NO 及 N2的物质的量随时间变化如图所示,图中 b 点 对应的速率关系是v(正)
(填﹥、﹤或﹦)。

(2)298 K 时,若已知生成标准状况下 2.24LNH3时放出热量为 4.62kJ。写出合成氨反应的热化学方程式
(3)一定条件下,在 2L密闭容器内,反应 2NO2(g)
 N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
①用 N2O4 表示 0~2 s 内该反应的平均速率为
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢气在工业合成中应用广泛,可用反应CO(g)+2H2(g)⇌CH3OH(g) ΔH<0 来制备甲醇,在容积不变的密闭容器中,当c(CO)=1.0mol/L、c(H2)=1.4 mol/L开始反应,结果如图所示,回答下列问题:
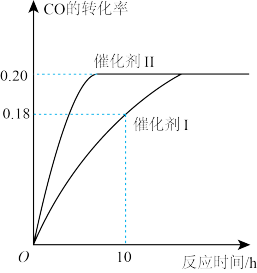
(1)使用催化剂Ⅰ时,在10小时内的平均速率v (H2) =___________ 。
(2)根据图中数据,计算此反应的平衡常数K1 =___________ 。(写出表达式,并代入数据,算出结果)
(3)反应 CO(g)+H2(g)⇌
CO(g)+H2(g)⇌ CH3OH(g)的平衡常数为K2,则K2与K1的关系是
CH3OH(g)的平衡常数为K2,则K2与K1的关系是___________ 。
(4)下列叙述正确的是___________ (填序号) 。
A.充入氩气增大压强有利于提高CO的转化率 B.升高温度有利于提高CO的转化率
C.当容器内气体的密度不再改变时,反应达到平衡D.催化剂Ⅱ的催化效率比催化剂Ⅰ高

(1)使用催化剂Ⅰ时,在10小时内的平均速率v (H2) =
(2)根据图中数据,计算此反应的平衡常数K1 =
(3)反应
 CO(g)+H2(g)⇌
CO(g)+H2(g)⇌ CH3OH(g)的平衡常数为K2,则K2与K1的关系是
CH3OH(g)的平衡常数为K2,则K2与K1的关系是(4)下列叙述正确的是
A.充入氩气增大压强有利于提高CO的转化率 B.升高温度有利于提高CO的转化率
C.当容器内气体的密度不再改变时,反应达到平衡D.催化剂Ⅱ的催化效率比催化剂Ⅰ高
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2L密闭容器内以物质的量比2:3充入CO和H2,400℃时反应:CO(g)+2H2(g) CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
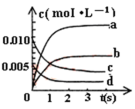
(1)如图表示反应中CH3OH的变化曲线,其中合理的是___________ 。
(2)用CO表示从0~2s内该反应的平均速率v(CO)=___________ 。
(3)能说明该反应已达到平衡状态的是___________ 。
a.v(CH3OH)=2v(H2)
b.容器内压强保持不变
c.断开2molH-H键的同时断开4molC-H键
d.容器内密度保持不变
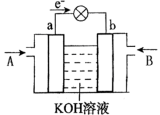
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从___________ (填A或B)通入,a极附近溶液pH将___________ (填升高,降低或不变),b极的电极反应式是___________ 。
 CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(1)如图表示反应中CH3OH的变化曲线,其中合理的是
(2)用CO表示从0~2s内该反应的平均速率v(CO)=
(3)能说明该反应已达到平衡状态的是
a.v(CH3OH)=2v(H2)
b.容器内压强保持不变
c.断开2molH-H键的同时断开4molC-H键
d.容器内密度保持不变
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从

您最近一年使用:0次



