不同温度下水的电离平衡曲线如图所示。下列说法不正确的是
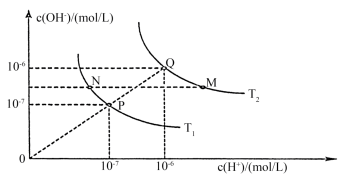

| A.图中,T1<T2,且线段PQ上任一点对应的体系均呈中性 |
| B.要从P点变到N点,可在T1温度下向水中加入适量醋酸 |
| C.点M与点N对应的pOH相等,但水的电离程度不同 |
| D.在T2温度下,将pH=8的Ba(OH)2溶液与pH=5的盐酸混合,要使混合溶液的pH=7,Ba(OH)2和盐酸的体积比应为2:9 |
2018高二·广东·竞赛 查看更多[1]
更新时间:2021-08-01 12:15:15
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】常温下,向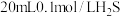 溶液中缓慢加入少量溶于水的
溶液中缓慢加入少量溶于水的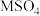 粉末(已知
粉末(已知 难溶,忽略溶液体积变化),溶液中
难溶,忽略溶液体积变化),溶液中 与
与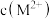 变化如图所示。已知:
变化如图所示。已知: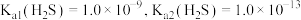 。下列说法错误的是
。下列说法错误的是
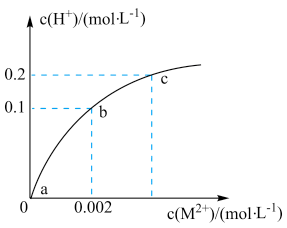
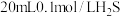 溶液中缓慢加入少量溶于水的
溶液中缓慢加入少量溶于水的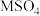 粉末(已知
粉末(已知 难溶,忽略溶液体积变化),溶液中
难溶,忽略溶液体积变化),溶液中 与
与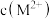 变化如图所示。已知:
变化如图所示。已知: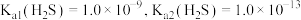 。下列说法错误的是
。下列说法错误的是
A.a点溶液的 约为5 约为5 |
B. 三点溶液中由水电离产生的 三点溶液中由水电离产生的 最大的是 最大的是 点 点 |
C. 点溶液中, 点溶液中, |
D. 点溶液中, 点溶液中,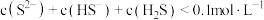 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某温度下,相同pH的氨水和氢氧化钠溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示。据图判断正确的是( )
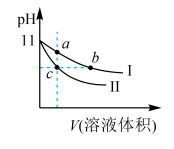

| A.Ⅰ为氨水稀释时的pH值变化曲线 |
| B.a、b、c三点溶液的导电性:c>b=a |
| C.a、b、c三点溶液中水的电离程度:c=b>a |
| D.用相同浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸的体积:Vb=Vc |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】25℃时,用0.10mol•L-1的氨水滴定10.00mL0.05mol•L-1的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中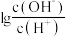 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )
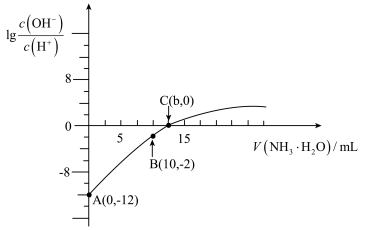
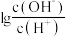 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )
| A.H2A的电离方程式为H2A⇌H++HA- |
| B.B点溶液中,水电离出的氢离子浓度为1.0×10-6mol•L-1 |
| C.C点溶液中,c(NH4+)+c(NH3•H2O)=2c(A2-) |
D.25℃时,氨水的电离平衡常数为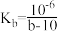 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】室温下,将NaOH溶液滴加到某酒石酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
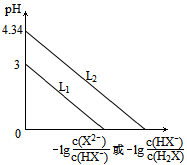

A.L1表示pH与﹣lg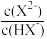 的变化关系 的变化关系 |
| B.NaHX溶液呈酸性 |
| C.L2上每点对应的溶液中水的电离程度都大于L1 |
| D.当c(Na+)﹣c(HX﹣)﹣c(X2﹣)=0时,溶液pH<7 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,用0.010mol•L﹣1NaOH溶液滴定0.010mol•L﹣1的二元酸H2A溶液,H2A、HA﹣、A2﹣的物质的量分数δ(X)随pH变化如图所示:
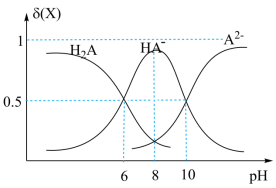
下列说法正确的是

下列说法正确的是
| A.pH=8时有c(HA-)>c(H2A)=c(A2-)>c(H+) |
| B.H2A的第一步电离平衡常数Ka1=1×10﹣6 |
| C.HA﹣的水解常数Kh=1×10﹣10 |
| D.将0.020mol•L﹣1Na2A溶液和0.010mol•L﹣1HCl溶液等体积混合,所得溶液的pH约为8 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】在密闭容器中进行反应: 2SO2(g) +O2(g)⇌2SO3 (g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别是0.2 mol/L、 0.1 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是
| A.SO2为0.4 mol/L,O2为0.2 mol/L |
| B.SO2为0.10 mol/L、SO3为0.30 mol/L |
| C.SO3为0.4 mol/L |
| D.SO2为0.25 mol/L |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速卒和推测反应16 min时反应物的浓度及反应级数,下列说法正确的是
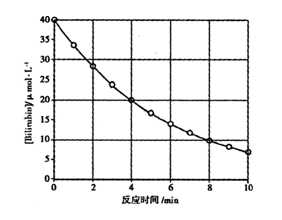

| A.2.5μ mol·L-1·min-1和2.0μ mol·L-1 |
| B.2.5μ mol·L-1·min-1和2.5μ mol·L-1 |
| C.该反应为零级反应 |
| D.该反应为一级反应 |
您最近一年使用:0次

 的
的 溶液中,由水电离的
溶液中,由水电离的
 的
的 溶液和
溶液和 溶液等体积混合,所得溶液
溶液等体积混合,所得溶液
 氨水和
氨水和 溶液等体积混合后所得溶液pH>7,则c(NH
溶液等体积混合后所得溶液pH>7,则c(NH )>c(NH3·H2O)
)>c(NH3·H2O) 的
的 溶液中加入
溶液中加入 溶液反应的离子方程式为:
溶液反应的离子方程式为:


