化合物A是一种烈性炸药。已知A为1:1型的离子化合物,A中只含有三种常见元素,将一定质量的A置于密闭且容积可变的容器中引爆,无固体物质残留。维持体系压强在101.3kPa下分别于120℃及25℃测得爆炸后产生的混合气体的密度分别为0.768g/L和1.20g/L,A的摩尔质量不大于150。
(1)通过计算写出A的化学式_______ 。
(2)写出120℃爆炸的化学方程式________ 。
(1)通过计算写出A的化学式
(2)写出120℃爆炸的化学方程式
2012高二·浙江·竞赛 查看更多[1]
更新时间:2021-08-02 21:59:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填写下列空白:
(1)_____ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(2)将等物质的量的 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为_______ 。
(3)要使 与
与 含相同数目的
含相同数目的 原子,则
原子,则 和
和 的物质的量之比为
的物质的量之比为_______ 。
(4)标准状况下,密度为0.75g•L-1的 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为_______ ,该混合气体对氢气的相对密度为_______ 。
(5)某结晶水合物的化学式为A•nH2O,A的相对分子质量为M。如将ag该结晶水合物加热至结晶水全部失去,剩余的残渣为bg,则
_______ 。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_______ 。
(7)配制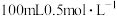 的硫酸铜溶液,所需胆矾的质量是
的硫酸铜溶液,所需胆矾的质量是_______ 。
(1)
(2)将等物质的量的
 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为(3)要使
 与
与 含相同数目的
含相同数目的 原子,则
原子,则 和
和 的物质的量之比为
的物质的量之比为(4)标准状况下,密度为0.75g•L-1的
 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为(5)某结晶水合物的化学式为A•nH2O,A的相对分子质量为M。如将ag该结晶水合物加热至结晶水全部失去,剩余的残渣为bg,则

(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
(7)配制
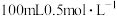 的硫酸铜溶液,所需胆矾的质量是
的硫酸铜溶液,所需胆矾的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答问题:
(1)等质量的CO和CO2,物质的量之比为___________ ,氧原子个数之比为___________ 。
(2)1.5molH2SO4的质量是___________ g,其中含有___________ molH,含有___________ g氧原子。
(3)1.806×1024个氨分子(NH3)的物质的量为___________ mol,含有___________ mol氢原子、___________ mol电子。
(4)有标准状况下的四种气体:①6.72LCH4,②3.01×1023个H2分子,③3.4gH2S,④0.2molNH3,则其体积按从大到小的顺序为:___________ (填序号)。
(5)标准状况下,测得1.92克某气体的体积为672mL,则此气体的相对分子质量为___________ 。
(1)等质量的CO和CO2,物质的量之比为
(2)1.5molH2SO4的质量是
(3)1.806×1024个氨分子(NH3)的物质的量为
(4)有标准状况下的四种气体:①6.72LCH4,②3.01×1023个H2分子,③3.4gH2S,④0.2molNH3,则其体积按从大到小的顺序为:
(5)标准状况下,测得1.92克某气体的体积为672mL,则此气体的相对分子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】计算填空
(1)相同物质的量的SO2和SO3,所含分子的数目之比为___________ ,所含原子数目之比为___________ ,所含氧原子的物质的量之比为___________ 。
(2)同温同压条件下,等质量的CO2与O2的体积比为___________ ,分子数之比为___________ ,原子数之比为___________ ,密度之比为___________ 。
(3)在Al2(SO4)3溶液中,若c( )=0.3mol/L,则c(Al3+)=
)=0.3mol/L,则c(Al3+)=___________ mol/L,c[Al2(SO4)3]=___________ mol/L。
(1)相同物质的量的SO2和SO3,所含分子的数目之比为
(2)同温同压条件下,等质量的CO2与O2的体积比为
(3)在Al2(SO4)3溶液中,若c(
 )=0.3mol/L,则c(Al3+)=
)=0.3mol/L,则c(Al3+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题
(1)下列10种物质:
①水②空气③铁④二氧化碳⑤硫酸⑥熟石灰[Ca(OH)2]⑦胆矾(CuSO4·5H2O)⑧酒精⑨硫酸氢钠溶液⑩熔融状态氯化钠
a.属于电解质的是___________ ;(填序号,下同)
b.属于非电解质的是___________ ;
c.属于弱电解质的是___________ ;
d.能导电的是___________ 。
(2)已知: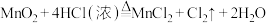 一定质量的二氧化锰溶解在
一定质量的二氧化锰溶解在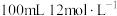 的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
a.反应耗用 的质量
的质量___________ ;
b.反应结束时理论上最后能生成氯气的体积___________ (标准状况下)。
(1)下列10种物质:
①水②空气③铁④二氧化碳⑤硫酸⑥熟石灰[Ca(OH)2]⑦胆矾(CuSO4·5H2O)⑧酒精⑨硫酸氢钠溶液⑩熔融状态氯化钠
a.属于电解质的是
b.属于非电解质的是
c.属于弱电解质的是
d.能导电的是
(2)已知:
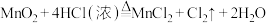 一定质量的二氧化锰溶解在
一定质量的二氧化锰溶解在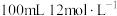 的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:a.反应耗用
 的质量
的质量b.反应结束时理论上最后能生成氯气的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在加热条件下,用MnO2与足量浓盐酸反应,制得氯气1.12L(标况下),已知反应后溶液体积为50mL。试计算:
(1)写出该反应的化学方程式_______ ;
(2)理论上需要消耗MnO2的质量为_______ ;
(3)若将上述反应后的溶液稀释至250mL,则稀释后的溶液中MnCl2的物质的量浓度为_____ 。
(1)写出该反应的化学方程式
(2)理论上需要消耗MnO2的质量为
(3)若将上述反应后的溶液稀释至250mL,则稀释后的溶液中MnCl2的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 、
、 都是大气污染物。请回答下列有关问题:
都是大气污染物。请回答下列有关问题:
(1)碘循环工艺能吸收 ,降低环境污染,同时又能制得氢气,反应过程如下图:
,降低环境污染,同时又能制得氢气,反应过程如下图:_______ ,氧化剂与还原剂的物质的量之比为_______ ,反应温度控制在20~100℃的原因是_______ 。
②若有196g 生成,理论上产生氢气的体积为
生成,理论上产生氢气的体积为_______ L(标准状况)。
(2)工业上用 溶液吸收
溶液吸收 ,生成等物质的量的两种钠盐,其中一种为
,生成等物质的量的两种钠盐,其中一种为 ,同时还有一种气体生成,则该反应的离子方程式为
,同时还有一种气体生成,则该反应的离子方程式为_______ 。
(3)工业上脱出 ,也可以在加热和催化剂作用下用
,也可以在加热和催化剂作用下用 还原生成
还原生成 和
和 ,实验测得温度高于400℃时,
,实验测得温度高于400℃时, 脱出率减小,其原因可能是
脱出率减小,其原因可能是_______ 。
(4)工业上可用 吸收含
吸收含 的烟气得到
的烟气得到 ,将50.7g
,将50.7g 受热分解,分解过程中的热重曲线(固体质量随温度变化的曲线)如图所示。
受热分解,分解过程中的热重曲线(固体质量随温度变化的曲线)如图所示。_______ 。
②1160℃时,所得固体的化学式为_______ 。
 、
、 都是大气污染物。请回答下列有关问题:
都是大气污染物。请回答下列有关问题:(1)碘循环工艺能吸收
 ,降低环境污染,同时又能制得氢气,反应过程如下图:
,降低环境污染,同时又能制得氢气,反应过程如下图: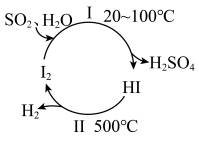
②若有196g
 生成,理论上产生氢气的体积为
生成,理论上产生氢气的体积为(2)工业上用
 溶液吸收
溶液吸收 ,生成等物质的量的两种钠盐,其中一种为
,生成等物质的量的两种钠盐,其中一种为 ,同时还有一种气体生成,则该反应的离子方程式为
,同时还有一种气体生成,则该反应的离子方程式为(3)工业上脱出
 ,也可以在加热和催化剂作用下用
,也可以在加热和催化剂作用下用 还原生成
还原生成 和
和 ,实验测得温度高于400℃时,
,实验测得温度高于400℃时, 脱出率减小,其原因可能是
脱出率减小,其原因可能是(4)工业上可用
 吸收含
吸收含 的烟气得到
的烟气得到 ,将50.7g
,将50.7g 受热分解,分解过程中的热重曲线(固体质量随温度变化的曲线)如图所示。
受热分解,分解过程中的热重曲线(固体质量随温度变化的曲线)如图所示。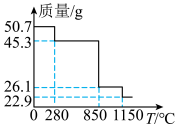
②1160℃时,所得固体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下面是我们熟悉的物质:①O2②金刚石③NaBr ④H2SO4⑤Na2CO3⑥NH4Cl
⑦NaHSO4⑧Ne ⑨Na2O2⑩NaOH
(1)这些物质中,只含有共价键的是______________ ;只含有离子键的是______________ ;不存在化学键的______________ ;
(2)属于共价化合物的是______________ ;
(3)将NaHSO4溶于水,破坏了NaHSO4中的_______ ,写出电离方程式______________ ;NaHSO4熔融状态下电离,破坏了___________ 键,写成电离方程式
______________________ 。
⑦NaHSO4⑧Ne ⑨Na2O2⑩NaOH
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)将NaHSO4溶于水,破坏了NaHSO4中的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下五种物质:①Na②金刚石③NaCl④NH3⑤He⑥NaOH。请用相应序号填空:
(1)熔化时只需要克服分子间作用力的是___________ 。
(2)含有共价键的有_______ 。属于共价化合物的是________ 。含共价键的离子化合物是_______ 。
(3)既能表示物质组成又能表示单质分子的是_________ 。
(4)熔化时能导电的是___________ 。
(5)①、②、④三种物质熔点由高到低的顺序为___________ 。
(1)熔化时只需要克服分子间作用力的是
(2)含有共价键的有
(3)既能表示物质组成又能表示单质分子的是
(4)熔化时能导电的是
(5)①、②、④三种物质熔点由高到低的顺序为
您最近一年使用:0次
【推荐3】生活污水中氮元素是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180 mg/L。
(1)写出NH4Cl的电子式_________ 。
(2)写出与氯同周期,有2个未成对电子的原子的电子排布式:_______ 、________
(3)为除去废水中的NH4+,向103 L该污水中加入0.1 mol/L NaOH溶液,理论上需要NaOH 溶液的体积为_________ L(计算结果保留两位小数)。
(4)若某污水中同时存在NH4+和NO3-时。可用下列方法除去:可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目:___ Fe +___ NO3- +___ H+=___ Fe2+ +___ NH4+ +___ H2O,____________ 。
(1)写出NH4Cl的电子式
(2)写出与氯同周期,有2个未成对电子的原子的电子排布式:
(3)为除去废水中的NH4+,向103 L该污水中加入0.1 mol/L NaOH溶液,理论上需要NaOH 溶液的体积为
(4)若某污水中同时存在NH4+和NO3-时。可用下列方法除去:可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】去年报道,在-55℃令XeF4(A)和C6F5BF2(B)化合,得一离子化合物(C),测得Xe的质量分数为31%,阴离子为四氟硼酸根离子,阳离子结构中有B的苯环。C是首例有机氙(IV)化合物,-20℃以下稳定。C为强氟化剂和强氧化剂,如与碘反应得到五氟化碘,放出氙,同时得到B。
(1)写出C的化学式,正负离子应分开写_______ 。
(2)根据什么结构特征把C归为有机氙比合物_______ 。
(3)写出C的合成反应方程式_______ 。
(4)写出C和碘的反应_______ 。
(5)画出五氟化碘分子的立体结构:_______ 。
(1)写出C的化学式,正负离子应分开写
(2)根据什么结构特征把C归为有机氙比合物
(3)写出C的合成反应方程式
(4)写出C和碘的反应
(5)画出五氟化碘分子的立体结构:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱。其中的关键反应是硫酸钠和焦炭、石灰石的反应,其反应的化学方程式为:_______ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
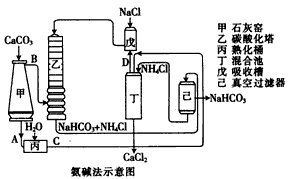
①用化学式表示出图中的中间产物C是_______ ,D是_______ ;
②装置乙中发生反应的化学方程式为_______ ;
(3)联合制碱法是对氨碱法的改进,其优点是(不低于2条)_______ 。
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行___________ ?

(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱。其中的关键反应是硫酸钠和焦炭、石灰石的反应,其反应的化学方程式为:
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。

①用化学式表示出图中的中间产物C是
②装置乙中发生反应的化学方程式为
(3)联合制碱法是对氨碱法的改进,其优点是(不低于2条)
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行

您最近一年使用:0次
【推荐3】箱中微粒:多烯
量子力学中,π电子沿碳原子中性共轭链的移动可以仿照“ 箱中微粒”的方法。π电子的能量在下面的方程中给出: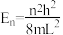 ,n是量子数(n= 1, 2, 3,…。),h是Planck's常数,m是电子质量,L是势箱的长度,并可近似地用L=(k+ 2) ×1.40 Å (k是分子碳链上共轭双键的数目)表示。适当波长λ 的光子可使π电子从最高占据轨道(HOMO)到最低未占据轨道(LUMO)。一个近似的半径验公式基于这个模型,将波长λ,双键数目k与常数B用下列关系式联系起来:
,n是量子数(n= 1, 2, 3,…。),h是Planck's常数,m是电子质量,L是势箱的长度,并可近似地用L=(k+ 2) ×1.40 Å (k是分子碳链上共轭双键的数目)表示。适当波长λ 的光子可使π电子从最高占据轨道(HOMO)到最低未占据轨道(LUMO)。一个近似的半径验公式基于这个模型,将波长λ,双键数目k与常数B用下列关系式联系起来:
λ (nm)=B×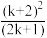 等式1
等式1
(1).用这个半径验公式,取B= 65.01 nm,计算辛四烯(CH2= CH- CH=CH- CH= CH- CH = CH2)的波长λ (nm)___________ 。
(2).推导等式1(电子从HOMO转移到LUMO对应波长λ(nm)的表达式),用k与基本常数表示。并以此计算常数Bcalc的理论值___________ 。
(3).我们想合成一个线型多烯,在激发电子从HOMO到LUMO时需要吸收大概600nm的光子。用你第二部分的表达式,确定多烯中共轭双键数(k)并给出它的结构___________ 。[如果你没有做出第二部分,用半径验公式等式1,取B= 65.01 nm来完成第三部分。]
(4).对于第三部分得到的多烯分子,计算HOMO与LUMO之间的能量差△E,(kJ·mol-1)。如果第三部分未解决,取k= 5解决这个问题。
(5).粒子在一维势箱中的模型可被扩展到三维长方体势箱中,长宽高为Lx、Ly与Lz。得到下列允许能级的表达式: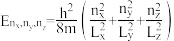
三个量子数nx,ny与nz必须为整数且相互独立。
①给出三个不同的最低能量的表达式,假定为边长L的立方势箱___________ 。
②能级的能量相同称为简并。画出草图展示所有能量的能级,包括所有简并能级,立方势箱对应的量子数取1或2___________ 。

量子力学中,π电子沿碳原子中性共轭链的移动可以仿照“ 箱中微粒”的方法。π电子的能量在下面的方程中给出:
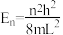 ,n是量子数(n= 1, 2, 3,…。),h是Planck's常数,m是电子质量,L是势箱的长度,并可近似地用L=(k+ 2) ×1.40 Å (k是分子碳链上共轭双键的数目)表示。适当波长λ 的光子可使π电子从最高占据轨道(HOMO)到最低未占据轨道(LUMO)。一个近似的半径验公式基于这个模型,将波长λ,双键数目k与常数B用下列关系式联系起来:
,n是量子数(n= 1, 2, 3,…。),h是Planck's常数,m是电子质量,L是势箱的长度,并可近似地用L=(k+ 2) ×1.40 Å (k是分子碳链上共轭双键的数目)表示。适当波长λ 的光子可使π电子从最高占据轨道(HOMO)到最低未占据轨道(LUMO)。一个近似的半径验公式基于这个模型,将波长λ,双键数目k与常数B用下列关系式联系起来:λ (nm)=B×
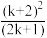 等式1
等式1(1).用这个半径验公式,取B= 65.01 nm,计算辛四烯(CH2= CH- CH=CH- CH= CH- CH = CH2)的波长λ (nm)
(2).推导等式1(电子从HOMO转移到LUMO对应波长λ(nm)的表达式),用k与基本常数表示。并以此计算常数Bcalc的理论值
(3).我们想合成一个线型多烯,在激发电子从HOMO到LUMO时需要吸收大概600nm的光子。用你第二部分的表达式,确定多烯中共轭双键数(k)并给出它的结构
(4).对于第三部分得到的多烯分子,计算HOMO与LUMO之间的能量差△E,(kJ·mol-1)。如果第三部分未解决,取k= 5解决这个问题。
(5).粒子在一维势箱中的模型可被扩展到三维长方体势箱中,长宽高为Lx、Ly与Lz。得到下列允许能级的表达式:
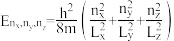
三个量子数nx,ny与nz必须为整数且相互独立。
①给出三个不同的最低能量的表达式,假定为边长L的立方势箱
②能级的能量相同称为简并。画出草图展示所有能量的能级,包括所有简并能级,立方势箱对应的量子数取1或2

您最近一年使用:0次



