生活污水中氮元素是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180 mg/L。
(1)写出NH4Cl的电子式_________ 。
(2)写出与氯同周期,有2个未成对电子的原子的电子排布式:_______ 、________
(3)为除去废水中的NH4+,向103 L该污水中加入0.1 mol/L NaOH溶液,理论上需要NaOH 溶液的体积为_________ L(计算结果保留两位小数)。
(4)若某污水中同时存在NH4+和NO3-时。可用下列方法除去:可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目:___ Fe +___ NO3- +___ H+=___ Fe2+ +___ NH4+ +___ H2O,____________ 。
(1)写出NH4Cl的电子式
(2)写出与氯同周期,有2个未成对电子的原子的电子排布式:
(3)为除去废水中的NH4+,向103 L该污水中加入0.1 mol/L NaOH溶液,理论上需要NaOH 溶液的体积为
(4)若某污水中同时存在NH4+和NO3-时。可用下列方法除去:可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目:
更新时间:2020-03-24 19:22:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同(设NA为阿伏加 德罗常数的值)。

回答下列问题:
(1)乙中的N为___________ ,丙中的V为___________ 。
(2)甲中NO2和丁中N2H4的物质的量之比为___________ 。
(3)乙中SO2和丁中N2H4的质量之比为___________ 。

回答下列问题:
(1)乙中的N为
(2)甲中NO2和丁中N2H4的物质的量之比为
(3)乙中SO2和丁中N2H4的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)O2和O3是氧元素的两种单质。根据分子式回答。等质量的O2和O3的物质的量之比为____ ,原子个数比为_____ 。
(2)NO2和N2O4是氮元素的两种常见氧化物,常温下都是气体,它们之间在常温下就能相互转化,因而经常见到的是两种气体的混合物。现取46g该气体,所含氮原子的物质的量为_____ 。
(3)已知三种物质NaCl、MgCl2、AlCl3分别溶于水,若溶液中的钠、镁、铝三种元素的质量比为23︰16︰9。则:
①NaCl、MgCl2、AlCl3三种物质的物质的量之比为_____ ;
②其中所含Cl-物质的量之比为_____ 。
(2)NO2和N2O4是氮元素的两种常见氧化物,常温下都是气体,它们之间在常温下就能相互转化,因而经常见到的是两种气体的混合物。现取46g该气体,所含氮原子的物质的量为
(3)已知三种物质NaCl、MgCl2、AlCl3分别溶于水,若溶液中的钠、镁、铝三种元素的质量比为23︰16︰9。则:
①NaCl、MgCl2、AlCl3三种物质的物质的量之比为
②其中所含Cl-物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】完成下列问题。
(1)现有m g某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:
①该气体的物质的量为______ mol。
②一个X原子的质量________ g。
③该气体在标准状况下的体积为_______ L。
④该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_______ mol·L-1。
⑤该气体溶于1L水中(不考虑反应,常温下水的密度为1g/cm3),所得溶液的密度为ρg/cm3,则该溶液的物质的量浓度为_______ mol。
(2)某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为______ g,该饱和溶液中溶质的物质的量浓度为_______ mol/L。
(1)现有m g某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:
①该气体的物质的量为
②一个X原子的质量
③该气体在标准状况下的体积为
④该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
⑤该气体溶于1L水中(不考虑反应,常温下水的密度为1g/cm3),所得溶液的密度为ρg/cm3,则该溶液的物质的量浓度为
(2)某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】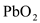 是很强的氧化剂,在酸性溶液中它可将
是很强的氧化剂,在酸性溶液中它可将 氧化成
氧化成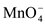 。取1支试管,加入少量
。取1支试管,加入少量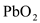 固体和2mL6 mol
固体和2mL6 mol
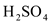 ,然后滴入2mL1 mol
,然后滴入2mL1 mol
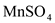 溶液。试回答:
溶液。试回答:
(1) 搅拌后,溶液的颜色变化是_______
(2) 反应的化学方程式是_______ ,硫酸的作用是_______
(3) 能否用盐酸代替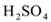
_______ (填“能”或“不能”),用化学方程式回答
_______
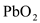 是很强的氧化剂,在酸性溶液中它可将
是很强的氧化剂,在酸性溶液中它可将 氧化成
氧化成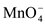 。取1支试管,加入少量
。取1支试管,加入少量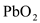 固体和2mL6 mol
固体和2mL6 mol
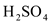 ,然后滴入2mL1 mol
,然后滴入2mL1 mol
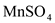 溶液。试回答:
溶液。试回答:(1) 搅拌后,溶液的颜色变化是
(2) 反应的化学方程式是
(3) 能否用盐酸代替
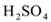
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___ 。
(2)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为___ 。
(3)实验室中可用次氯酸钠溶液与氨反应制备联氨(N2H4),反应的化学方程式为___ 。
(4)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如表。
写出NaClO2溶液脱硝过程中主要反应的离子方程式___ 。
(2)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为
(3)实验室中可用次氯酸钠溶液与氨反应制备联氨(N2H4),反应的化学方程式为
(4)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如表。
| 离子 | SO | SO | NO |
| c/(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 |
| 离子 | NO | Cl- | |
| c/(mol·L-1) | 1.2×10-5 | 3.4×10-3 |
写出NaClO2溶液脱硝过程中主要反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
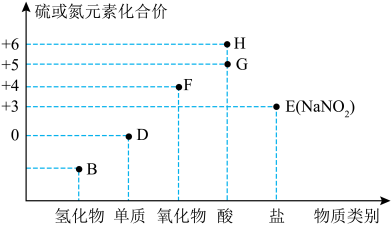
【推荐3】“价—类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价—类”二维图如图所示,回答下列问题: ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):_______ 。
(2)若B为 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),该反应的化学方程式为
),该反应的化学方程式为_______ ;某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是_______ (填字母)。
A.NaOH B. C.
C. D.浓硫酸
D.浓硫酸
(4)D可以是 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=_____ 。
(5) 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:_______ 。
(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是_______ 。
 ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):(2)若B为
 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。| A.氨气易液化;液氨可用作制冷剂 | B.可用排水法收集氨气 |
| C.氨气是一种无色、无味的气体 | D.向氨水中滴加酚酞,溶液变红 |
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),该反应的化学方程式为
),该反应的化学方程式为 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是A.NaOH B.
 C.
C. D.浓硫酸
D.浓硫酸(4)D可以是
 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=(5)
 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知氢化钠(NaH)属于离子化合物,NaH跟水反应可以放出氢气。则
(1)NaH与水反应的化学方程式为_______________ ,氧化剂为________ ,氧化产物为________ ,生成1mol H2转移电子_____ mol;
(2)NaH中的两种离子,离子半径小的是______ (填离子符号);
(3)如何通过实验证明NaH属于离子化合物?__________________ 。
(1)NaH与水反应的化学方程式为
(2)NaH中的两种离子,离子半径小的是
(3)如何通过实验证明NaH属于离子化合物?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是__________ ,该化合物是由__________ 键形成的。
(2)Na3N与盐酸反应生成生成两种盐,其电子式分别是__________ 、 __________ 。
(3)比较Na3N中两种微粒的半径:r(Na+)__________ r(N3-)(填“>”“=”或“<”)。
(1)Na3N的电子式是
(2)Na3N与盐酸反应生成生成两种盐,其电子式分别是
(3)比较Na3N中两种微粒的半径:r(Na+)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】车辆碰撞瞬间,安全装置通电点火,使其中的粉末分解释放出大量保护气形成安全气囊。经分析确定气囊中粉末含有Na、Fe、N、O四种元素。
(1)铁元素在周期表中位置_______________ ,氧原子最外层电子排布式为_____________ 。
(2)上述主族元素中,简单离子半径最小的是________ (写微粒符号);气态氢化物之间发生反应的相关方程式为_______________________________________ 。
(3)气囊粉末中能释放出保护气的化合物由两种短周期元素组成,且2 mol 该物质分解可产生3 mol非金属单质和2 mol 金属单质。该化合物的化学式为______ ,晶体类型是______ 。
(4)下列能用于判断氮、氧两种元素非金属性强弱的是_______ (填序号)。
a. 气态氢化物稳定性 b. 最高价氧化物对应水化物酸性强弱
c. 单质沸点高低 d. 在氮氧化物中,氧显负价,氮显正价
(1)铁元素在周期表中位置
(2)上述主族元素中,简单离子半径最小的是
(3)气囊粉末中能释放出保护气的化合物由两种短周期元素组成,且2 mol 该物质分解可产生3 mol非金属单质和2 mol 金属单质。该化合物的化学式为
(4)下列能用于判断氮、氧两种元素非金属性强弱的是
a. 气态氢化物稳定性 b. 最高价氧化物对应水化物酸性强弱
c. 单质沸点高低 d. 在氮氧化物中,氧显负价,氮显正价
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1) 某元素价层电子排布式为3d64s2,该元素在周期表中位于_____ 区_____ 族。
(2)某元素N能层只有1个电子,其余能层均已填满电子,该元素价层电子排布图为_____ 。
(3) SO2分子中,S原子采用_____ 杂化轨道成键,该分子的价层电子对互斥模型_____ 。
(2)某元素N能层只有1个电子,其余能层均已填满电子,该元素价层电子排布图为
(3) SO2分子中,S原子采用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)。
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍_______ 。
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3_______ 。
(3)最外层电子数不会超过8个,次外层电子数不会超过18个_______ 。
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2_______ 。
(5)在磷原子的基态原子结构中,有3个未成对的单电子_______ 。
(6)第四周期元素中,4p轨道半充满的是_______ ,3d轨道半充满的是_______ ,4s轨道半充满的是_______ 。(填元素符号)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3
(3)最外层电子数不会超过8个,次外层电子数不会超过18个
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2
(5)在磷原子的基态原子结构中,有3个未成对的单电子
(6)第四周期元素中,4p轨道半充满的是
您最近一年使用:0次



