车辆碰撞瞬间,安全装置通电点火,使其中的粉末分解释放出大量保护气形成安全气囊。经分析确定气囊中粉末含有Na、Fe、N、O四种元素。
(1)铁元素在周期表中位置_______________ ,氧原子最外层电子排布式为_____________ 。
(2)上述主族元素中,简单离子半径最小的是________ (写微粒符号);气态氢化物之间发生反应的相关方程式为_______________________________________ 。
(3)气囊粉末中能释放出保护气的化合物由两种短周期元素组成,且2 mol 该物质分解可产生3 mol非金属单质和2 mol 金属单质。该化合物的化学式为______ ,晶体类型是______ 。
(4)下列能用于判断氮、氧两种元素非金属性强弱的是_______ (填序号)。
a. 气态氢化物稳定性 b. 最高价氧化物对应水化物酸性强弱
c. 单质沸点高低 d. 在氮氧化物中,氧显负价,氮显正价
(1)铁元素在周期表中位置
(2)上述主族元素中,简单离子半径最小的是
(3)气囊粉末中能释放出保护气的化合物由两种短周期元素组成,且2 mol 该物质分解可产生3 mol非金属单质和2 mol 金属单质。该化合物的化学式为
(4)下列能用于判断氮、氧两种元素非金属性强弱的是
a. 气态氢化物稳定性 b. 最高价氧化物对应水化物酸性强弱
c. 单质沸点高低 d. 在氮氧化物中,氧显负价,氮显正价
12-13高三上·上海虹口·期末 查看更多[1]
(已下线)上海市虹口区2012届高三上学期期末教学质量监控测试化学试题
更新时间:2020-03-31 17:22:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表列出了9种元素在元素周期表中的位置示意图。
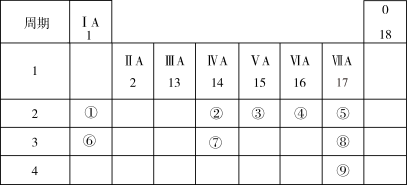
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______________ 。
(2)画出元素⑧形成的简单离子的结构示意图_______________ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______________ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______________ 。
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是______________ (填化学式),写出元素⑤的单质与水反应的化学方程式_______________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______________ 。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
完成下列填空:
(1)上述反应中的还原剂为___ ,还原产物有___ ,当有1molKNO3参加反应时,转移电子的数目为___ 。
(2)KNO3晶体类型是___ ,其晶体中存在的化学键有___ 。
(3)硫原子的核外电子排布式为___ ,原子核外有___ 种不同能量的电子。将SO2和Cl2分别通入品红溶液中,产生的现象是___ ;若将SO2和Cl2等体积混合后再缓缓通入品红溶液,发现品红溶液___ ,其原因是___ 。
(4)S、C和N三种元素的原子半径从小到大的顺序是___ ;K2S溶液中除OH-外其它各离子物质的量浓度的大小顺序为___ 。
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___ 。
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
 K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑完成下列填空:
(1)上述反应中的还原剂为
(2)KNO3晶体类型是
(3)硫原子的核外电子排布式为
(4)S、C和N三种元素的原子半径从小到大的顺序是
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是___________ (填元素符号),酸性最强的最高价氧化物对应水化物是___________ (填化学式)。
(2)写出⑤和⑨两种元素组成的化合物的电子式________ ,该化合物中含有________ (填“离子键”“共价键”)
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(5)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)写出⑤和⑨两种元素组成的化合物的电子式
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(5)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】M、X、Y、Z、W元素的原子序数依次增大,M与Y同主族,X、Z的最外层电子数之和等于Z的内层电子数,最外层电子数Y是X的2倍,X、W的单质是生产、生活中应用最广的两种金属。回答下列问题:
(1)M、X、Z的简单离子半径由大到小的顺序为___________ (用离子符号表示);实验室检验 常用的试剂是
常用的试剂是___________ 。
(2)Z离子结构示意图为___________ ;W在元素周期表中的位置是___________ 。
(3)X最高价氧化物对应水化物与强碱溶液反应的离子方程式为___________ ;W的单质与水蒸气在高温下反应,此反应中还原剂与还原产物的物质的量之比为___________ ;写出一个能体现X、W金属性强弱的离子方程式:___________ 。
(4)M、Y、Z元素非金属性由强到弱的顺序是___________ (用元素符号表示);能比较Y和Z的非金属性强弱的依据是___________ (填标号)。
A.氢化物酸性Z强于Y
B.Z的单质能与Y的氢化物反应得到Y的单质
C.气态氢化物的稳定性Z强于Y
D.最高价氧化物对应水化物的酸性Z强于Y
(1)M、X、Z的简单离子半径由大到小的顺序为
 常用的试剂是
常用的试剂是(2)Z离子结构示意图为
(3)X最高价氧化物对应水化物与强碱溶液反应的离子方程式为
(4)M、Y、Z元素非金属性由强到弱的顺序是
A.氢化物酸性Z强于Y
B.Z的单质能与Y的氢化物反应得到Y的单质
C.气态氢化物的稳定性Z强于Y
D.最高价氧化物对应水化物的酸性Z强于Y
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为_____________
(2)W与Y 可形成化合物W2Y,该化合物的电子式为________________________ 。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_________________________ 。Y的最高价氧化物是否满足8电子稳定结构______________ (填是.否)
(4)比较Y、Z气态氢化物的稳定性由大到小的顺序是________________ (用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
____________________________________________________ 。(用离子符号表示)。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(2)W与Y 可形成化合物W2Y,该化合物的电子式为
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(4)比较Y、Z气态氢化物的稳定性由大到小的顺序是
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用。NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是________ 。
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
①在周期表中,最可能处于同一族的是_________ 。
②T元素最可能是_______ 区元素。若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物的空间构型为________ ,其中心原子的杂化方式为________ 。
(1)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是
②T元素最可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.有下列几种物质:①CH4②N2③CO2④CH3CH3⑤C2H4⑥H2O2。请按要求回答下列问题(填写编号):
(1)只有σ键的有____ ,既有σ键又有π键的有____ 。
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为___ 。
II.2019年1月3日,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。其所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(3)基态Ga原子价电子排布式为____ ,核外电子占据最高能级的电子云形状为____ ;基态As原子最高能层上有___ 个电子。
(4)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____ 和+3,砷的第一电离能比镓___ (填“大”或“小”)。
(5)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为____ 。
(6)砷化镓可由(CH3)3Ga和AsH3在700℃制得,其中AsH3分子的VSEPR模型为____ 。
(7)与砷同主族的氮容易形成三键,但砷却难以形成三键的原因是___ 。
(1)只有σ键的有
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为
II.2019年1月3日,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。其所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(3)基态Ga原子价电子排布式为
(4)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(5)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(6)砷化镓可由(CH3)3Ga和AsH3在700℃制得,其中AsH3分子的VSEPR模型为
(7)与砷同主族的氮容易形成三键,但砷却难以形成三键的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)Fe基态原子核外电子排布式为_____________________ 。
(2)H、N、O的电负性从小到大的顺序是___________________ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为______________ (填化学式)。
氨基(-NH2)中氮原子的杂化类型为_________________ 。
(4)1mol乙酸分子中含有σ键的数目为____________________ 。
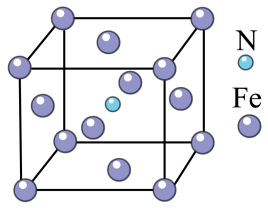
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为_______________ 。
(2)H、N、O的电负性从小到大的顺序是
(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为氨基(-NH2)中氮原子的杂化类型为
(4)1mol乙酸分子中含有σ键的数目为
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为_______ 。
② ,烯丙醇分子中碳原子的杂化类型为
,烯丙醇分子中碳原子的杂化类型为_______ 。
③某种含Cu2+的化合物可催化烯丙醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在烯丙醇分子中σ键和π键的个数比为_______ 。
(2) 具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则
具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则 中的配位数为
中的配位数为_______ ,配离子的空间构型为_______ 。
(3)铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺可形成如图所示配离子。
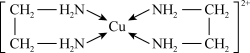
①Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是_______ (填字母序号)。
a.配位键 b.极性键 c.离子键 d.非极性键
②乙二胺和三甲胺 均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
均属于胺。但乙二胺比三甲胺的沸点高很多,原因是_______ 。
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为
 。请回答下列问题:
。请回答下列问题:①基态镍原子的价电子排布式为
②
 ,烯丙醇分子中碳原子的杂化类型为
,烯丙醇分子中碳原子的杂化类型为③某种含Cu2+的化合物可催化烯丙醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在烯丙醇分子中σ键和π键的个数比为
(2)
 具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则
具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则 中的配位数为
中的配位数为(3)铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺可形成如图所示配离子。

①Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是
a.配位键 b.极性键 c.离子键 d.非极性键
②乙二胺和三甲胺
 均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】晶体的性质与晶体类型和结构紧密相关。
(1)氯酸钾熔化时克服的作用力是______ ;二氧化硅熔化时克服的作用力是______ ;碘升华时克服的作用力是______ 。三种晶体的熔点由高到低的顺序是______ (填化学式)。
(2)下列六种晶体:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥金刚石,它们的熔点从低到高的顺序为
,⑥金刚石,它们的熔点从低到高的顺序为______ (填序号)。
(1)氯酸钾熔化时克服的作用力是
(2)下列六种晶体:①
 ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥金刚石,它们的熔点从低到高的顺序为
,⑥金刚石,它们的熔点从低到高的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据要求回答下列问题:
(1)下列有关晶体结构和性质的说法中,正确的是_______ (填序号)。
①由金属元素和非金属元素组成的晶体一定是离子晶体
②分子晶体中不一定都存在共价键
③溶于水能导电的晶体一定是离子晶体
④离子晶体一定都含有金属元素
⑤通过X—射线衍射实验的方法可以区分晶体和非晶体
⑥在NaCl晶体中,每个Na+周围与其距离最近的Na+有12个
(2)在下列物质形成的晶体中:NaCl、NaOH、Na2S、H2O2、Na2O2、(NH4)2S、CO2、CCl4、C2H2、SiO2、SiC、晶体硅、金刚石。
①其中只含有离子键的离子晶体是_______ 。
②其中既含有离子键又含有极性共价键的离子晶体是_______ 。
③其中既含有离子键又含有极性共价键和配位键的离子晶体是_______ 。
④其中既含有离子键又含有非极性共价键的离子晶体是_______ 。
⑤其中含有极性共价键的共价晶体是_______ 。
⑥其中属于分子晶体的是_______ 。
(1)下列有关晶体结构和性质的说法中,正确的是
①由金属元素和非金属元素组成的晶体一定是离子晶体
②分子晶体中不一定都存在共价键
③溶于水能导电的晶体一定是离子晶体
④离子晶体一定都含有金属元素
⑤通过X—射线衍射实验的方法可以区分晶体和非晶体
⑥在NaCl晶体中,每个Na+周围与其距离最近的Na+有12个
(2)在下列物质形成的晶体中:NaCl、NaOH、Na2S、H2O2、Na2O2、(NH4)2S、CO2、CCl4、C2H2、SiO2、SiC、晶体硅、金刚石。
①其中只含有离子键的离子晶体是
②其中既含有离子键又含有极性共价键的离子晶体是
③其中既含有离子键又含有极性共价键和配位键的离子晶体是
④其中既含有离子键又含有非极性共价键的离子晶体是
⑤其中含有极性共价键的共价晶体是
⑥其中属于分子晶体的是
您最近一年使用:0次



