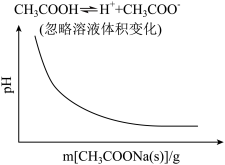
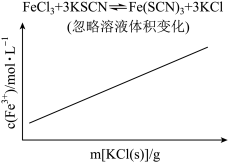
在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH= -164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= 41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)=CO2(g)+CH4(g) ΔH= -247.1 kJ/mol
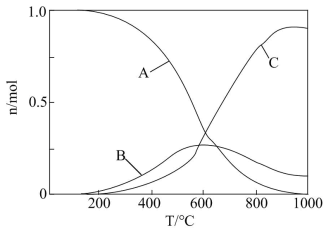
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法正确的是
反应Ⅰ:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH= -164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= 41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)=CO2(g)+CH4(g) ΔH= -247.1 kJ/mol
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法正确的是

A.反应Ⅰ的平衡常数可表示为K=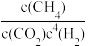 |
| B.图中曲线B表示CO的物质的量随温度的变化 |
| C.提高 CO2转化为CH4的转化率,需要研发在低温区高效的催化剂 |
| D.CH4(g)+H2O(g) =CO(g)+3H2(g)的ΔH= -205.9 kJ/mol |
2021高三·全国·专题练习 查看更多[17]
(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)2021年秋季高三化学开学摸底考试卷03(广东专用)(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)河北省实验中学2022届高三年级上学期开学考试化学试题江苏省南通市海安高级中学2022届高三期中考试化学试题江苏省海安市实验中学2021-2022学年高三上学期第一次月考化学试题河北深州市长江中学2021-2022学年高二上学期10月月考化学(理)试题河北省石家庄市第二中学2022届高三补偿诊断性考试江苏省高邮市2021-2022学年高二上学期期中学情调研化学试题(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)(已下线)专题12 化学反应速率与化学平衡-2022年高考化学二轮复习重点专题常考点突破练2.3.2温度 催化剂对化学平衡的影响 课后江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题湖北省武汉市第四十九中学2023-2024学年高二上学期10月月考化学试题河南省焦作市第十一中学2023-2024学年高二上学期9月份月考 化学试卷四川省眉山市仁寿县校际2023-2024学年高二上学期10月联考化学试题
更新时间:2021-08-11 20:41:48
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】工业上利用碳热还原 制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。
制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。
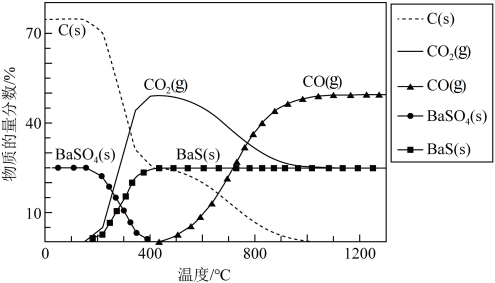
已知:碳热还原 过程中可能发生下列反应。
过程中可能发生下列反应。
i.

ii.
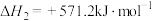
iii.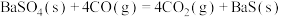
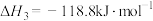
下列关于碳热还原 过程的说法中正确的是
过程的说法中正确的是
 制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。
制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。
已知:碳热还原
 过程中可能发生下列反应。
过程中可能发生下列反应。i.


ii.

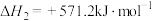
iii.
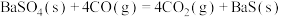
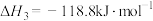
下列关于碳热还原
 过程的说法中正确的是
过程的说法中正确的是| A.要想得到更多的BaS,温度应该越高越好 |
B.对于反应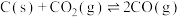 ,温度升高,CO的物质的量分数减小 ,温度升高,CO的物质的量分数减小 |
C.400℃后,C、 的量减少是由 的量减少是由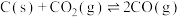 的移动导致的 的移动导致的 |
D.根据原子守恒规律可知生成的 和CO的物质的量之和始终等于投入C的物质的量 和CO的物质的量之和始终等于投入C的物质的量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应1: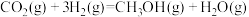

反应2:
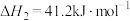
恒压下,将起始 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
的选择性[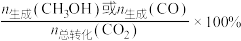 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法不 正确的是
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应1:
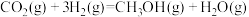

反应2:

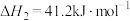
恒压下,将起始
 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
的选择性[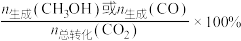 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法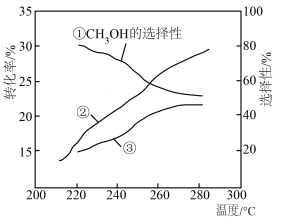
A.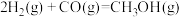 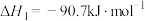 |
| B.曲线③表示CO的选择性 |
C.280℃时出口处 的物质的量分数比220℃时小 的物质的量分数比220℃时小 |
D.为提高 生产效率,需研发单位时间 生产效率,需研发单位时间 转化率高和 转化率高和 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确 的是
 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述
| A.1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子 |
| B.室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性 |
| C.NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol |
| D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】研究表明,纳米0价金属能去除地下水中的NO3-,不同初始pH和不同金属组成对NO3-的去除效果如图所示。图1初始pH=5.5,图2初始pH=2,NO3-初始浓度均为50mg·L-1,纳米级金属添加量均为2g·L-1。下列说法正确的是




| A.纳米铁的去除效果优于纳米镍 |
B.图2纳米铁反应60mn时NO3-去除率67.2%,则60min内 |
| C.当加入的金属是Fe0/Ni05/1,在不同的初始pH下,经过60min后,NO3-的去除率相等 |
| D.其他条件相同时,若pH过低,可能会导致去除率下降 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】乙烯可用于制备乙醇:
 。向10L某恒容密闭容器中通入2mol
。向10L某恒容密闭容器中通入2mol  (g)和m mol
(g)和m mol  (g)发生上述反应,测得
(g)发生上述反应,测得 (g)的平衡转化率与投料比
(g)的平衡转化率与投料比 以及温度的关系如图所示。下列说法正确的是
以及温度的关系如图所示。下列说法正确的是


 。向10L某恒容密闭容器中通入2mol
。向10L某恒容密闭容器中通入2mol  (g)和m mol
(g)和m mol  (g)发生上述反应,测得
(g)发生上述反应,测得 (g)的平衡转化率与投料比
(g)的平衡转化率与投料比 以及温度的关系如图所示。下列说法正确的是
以及温度的关系如图所示。下列说法正确的是
A. |
B.a、b点对应的平衡常数 |
C.a点对应的体系中,反应从开始到平衡的2min内,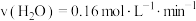 |
| D.b点对应的体系中,m=1.8 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在一定容积的密闭容器中发生可逆反应A(g)+2B(g) 2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是
2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是
 2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是
2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是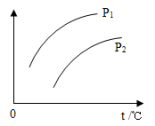
| A.P1<P2,纵坐标表示C的质量分数 |
| B.P1<P2,纵坐标表示A的质量分数 |
| C.P1>P2,纵坐标表示A的转化率 |
| D.P1<P2,纵坐标表示混合气体的平均摩尔质量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】温度T℃时,在初始体积为1L的两个密闭容器甲(恒容)、乙(恒压)中分别加入0.2molA和0.1molB,发生反应2A(g)+B(g)  x C(g),实验测得甲、乙容器中A的转化率随时间的变化关系如图所示。下列说法错误的是
x C(g),实验测得甲、乙容器中A的转化率随时间的变化关系如图所示。下列说法错误的是

 x C(g),实验测得甲、乙容器中A的转化率随时间的变化关系如图所示。下列说法错误的是
x C(g),实验测得甲、乙容器中A的转化率随时间的变化关系如图所示。下列说法错误的是
| A.x可能为4 |
| B.M为容器甲 |
| C.容器乙达平衡时B的转化率为25% |
| D.M的平衡常数大于N |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
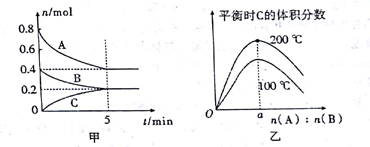
【推荐3】在4 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
| A.200 ℃时,该反应的平衡常数为6.25L2/mol2 |
B.由甲图和乙图可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2 zC(g)的ΔH<0,且a=2 |
| C.200℃时,向容器中加入2molA 和1molB,达到平街时C的体积分数大于0.25 |
| D.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正反应速率均增大,逆反应速率减小 |
您最近一年使用:0次