下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题;
(1)④表示的元素是___________ (填元素符号);
(2)②、③两种元素相比较,原子半径较大的是___________ (填元素符号);
(3)写出①与⑥两种元素所形成化合物的电子式___________ ;
(4)③和⑤两种元素的非金属性强弱顺序是③___________ ⑤(填“<”或“>”)。
族 周期 | ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ② | ③ | F | Ne | |||||
| 3 | ④ | Mg | Si | ⑤ | ⑥ |
(2)②、③两种元素相比较,原子半径较大的是
(3)写出①与⑥两种元素所形成化合物的电子式
(4)③和⑤两种元素的非金属性强弱顺序是③
更新时间:2021-09-08 18:53:07
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表中的一部分。
根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)化学性质最不活泼的元素是___________ ,氧化性最强的单质是___________ ,还原性最强的单质是___________ 。
(2)最高价氧化物对应的水化物中,碱性最强的是___________ ,酸性最强的是___________
(3)A分别与E、F、G、H、I形成的化合物中,最稳定的是___________ 。
(4)在B、C、D、G、I中,离子半径最大的是___________ 。
(5)元素C与I形成的化合物的电子式是___________ 。
(6)53号元素在元素周期表中的位置___________ 。
(7)D单质与B的最高价氧化物对应水化物反应的离子方程式___________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | E | F | H | J | ||||
| 3 | B | C | D | G | I |
(1)化学性质最不活泼的元素是
(2)最高价氧化物对应的水化物中,碱性最强的是
(3)A分别与E、F、G、H、I形成的化合物中,最稳定的是
(4)在B、C、D、G、I中,离子半径最大的是
(5)元素C与I形成的化合物的电子式是
(6)53号元素在元素周期表中的位置
(7)D单质与B的最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】以下是元素周期表前四周期的部分元素,请用合适的化学用语回答问题。
(1)J元素在周期表中的位置是_______ 。
(2)D元素的名称是_______ ,含5个中子的B原子的符号是_______ 。
(3)写出C2J的电子式_______ 。
(4)元素A~M中,化学性质最不活泼的是_______ (填元素符号,下同),无正化合价的是_______ 。
(5)用“>”“<”或“=”回答酸性:H2SO4_______ HClO4;
| A | |||||||||||||||||
| B | G | L | M | ||||||||||||||
| C | F | H | I | J | K | ||||||||||||
| D | E |
(2)D元素的名称是
(3)写出C2J的电子式
(4)元素A~M中,化学性质最不活泼的是
(5)用“>”“<”或“=”回答酸性:H2SO4
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分,针对表中①~⑧元素,回答下列问题:_____ ,M层有___ 个电子。写出③的原子结构示意图_____ 。
(2)元素②在周期表中的位置是_____ ,③元素在周期表中的位置是第2周期_____ 族。
(3)写出②的最高价氧化物_______ ,写出⑥的最高价氧化物_____ 。
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是______ (填化学式)。
(5)⑤的单质在③中燃烧,产物是______ 。

(2)元素②在周期表中的位置是
(3)写出②的最高价氧化物
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是
(5)⑤的单质在③中燃烧,产物是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】动手实践:某同学探究同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究___ 元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等。
仪器:①___ ,②___ ,③___ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)___
①的化学方程式___ ,
②的化学方程式___ 。
(4)实验结论:
失电子能力:___ ,得电子能力:___ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制的Na2S溶液中滴入新制氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加溶液至过量 | F.生成淡黄色沉淀 |
(1)实验目的:研究
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等。
仪器:①
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
①的化学方程式
②的化学方程式
(4)实验结论:
失电子能力:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
请你帮助该同学整理并完成实验报告
(1)实验目的:_____________________________________________________________ 。
(2)实验用品:仪器、材料: 略 药品: 略
(3)实验内容:用序号填写下表中的实验方案,并完成相关的离子方程式___________________ 。
(4)实验结论:____________________________________________________ 。
(5)请用原子结构理论解释上述结论的原因___________________________
| 实验方案 | 实验现象 | ||||
| ①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞。 ②向新制的H2S饱和溶液中滴加新制的氯水 ③钠与滴有酚酞试液的冷水反应 ④镁带与2mol/L的盐酸反应 ⑤铝条与2mol/L的盐酸反应 |
|
请你帮助该同学整理并完成实验报告
(1)实验目的:
(2)实验用品:仪器、材料: 略 药品: 略
(3)实验内容:用序号填写下表中的实验方案,并完成相关的离子方程式
| 实验方案 | 实验现象 | 有关离子方程式 |
| A | ||
| B | 不填 | |
| C | 不填 | |
| D | 不填 | |
| E |
(4)实验结论:
(5)请用原子结构理论解释上述结论的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题
(1)上述元素中,金属性最强的是_______ (填元素名称),最高价氧化物对应水化物酸性最强的是_______ (写出酸的化学式)。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:_______ 。(用离子符号表示)
(3)由元素①和④形成的18电子的结构式为_______ ;由元素①、③、⑨形成的离子化合物的电子式为_______ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程_______ 。
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:_______
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系_______ 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
(7)元素③、磷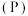 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置_______ 。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ | |||||||
(1)上述元素中,金属性最强的是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:
(3)由元素①和④形成的18电子的结构式为
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
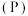 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)在①~⑩元素中,最活泼的金属元素是_____ ,最活泼的非金属元素是____ ,最不活泼的元素是_____ ,非金属气态氢化物最稳定的是______ ,原子半径最大的是______ ,可做半导体材料的是______ 。(填元素符号)
(2)在①~⑩元素中,⑧的氢化物是_____ ,最高价氧化物对应的水化物中碱性最强的是______ ,呈两性的是_____ 。写出在水溶液中三者之间相互反应的离子方程式:____ ,____ ,_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
4 | ⑩ |
(2)在①~⑩元素中,⑧的氢化物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩中10种元素用元素符号或化学式填空回答以下问题:
(1)⑥的原子结构示意图_____ ;
(2)非金属性最强的元素是_____ (填元素符号);
(3)②、⑨的氢化物比较稳定的是_____ (填化学式)
(4)写出①与③形成原子个数比为1:1化合物的电子式:_____ ;
(5)③、⑧形成的原子个数比为2:1的物质属于_____ (填“晶体类型”)。
(6)最高价氧化物对应的水化物中碱性最强的是_____ (填化学式),写出该物质与⑦的最高价氧化物对应的水化物反应的离子方程式为:_____ ;由①③⑩元素组成的一种强酸,该强酸的浓溶液与铜反应的化学方程式_____ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
(2)非金属性最强的元素是
(3)②、⑨的氢化物比较稳定的是
(4)写出①与③形成原子个数比为1:1化合物的电子式:
(5)③、⑧形成的原子个数比为2:1的物质属于
(6)最高价氧化物对应的水化物中碱性最强的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】钠、钾与水反应的实验如下图所示:
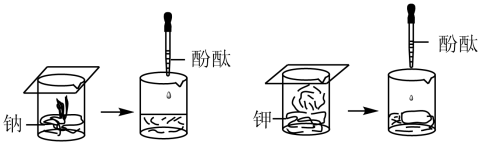
(1)钠、钾与水反应两个实验现象的相同点:
①金属________ 水面上;
②金属________ 成闪亮的小球;
③小球四处游动;
④产生嘶嘶的声音;
⑤反应后的溶液使酚酞________ 。
(2)_______ 与水反应有轻微的爆鸣声,并很快燃烧起来。
(3)实验结论:________ 更易与水反应,且反应更_____________________________________ 。
(4)钾与水反应的化学方程式是___________________________________________________ 。

(1)钠、钾与水反应两个实验现象的相同点:
①金属
②金属
③小球四处游动;
④产生嘶嘶的声音;
⑤反应后的溶液使酚酞
(2)
(3)实验结论:
(4)钾与水反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经150年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以下问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___ ;
(2)元素①的单质电子式为____ 。
(3)比较③、⑤元素的金属性强弱___ >___ ;并写出它们最高价氧化物对应的水化物间反应的化学方程式____ 。
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是____ 。
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是_____ ;
(6)工业制取⑥的单质的反应的化学方程式为_______ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)元素①的单质电子式为
(3)比较③、⑤元素的金属性强弱
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是
(6)工业制取⑥的单质的反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A、B、C、D、E、F六种元素为短周期主族元素,且原子序数依次增大。A为第IA族的非金属元素,A、D元素同主族,B元素的一种核素可用于测定一些文物的年代,C元素的原子最外层电子数是内层电子数的3倍,且C元素与F元素同主族,E元素的周期数等于其主族族序数。回答下列问题:
(1)B、F元素分别为___________ 、___________ 。(填元素符号)
(2)E元素在周期表中的位置是___________ ;化合物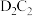 的电子式为
的电子式为___________ 。
(3)C、D、F三种元素形成的简单离子,其半径由大到小的顺序是___________ (用离子符号表示)。
(4)C、F两种元素简单气态氢化物的稳定性:___________ >___________ (均填化学式)。
(5)E的最高价氧化物对应的水化物可用于治疗胃酸过多,反应的离子方程式为___________ 。
(6)锗(Ge)与元素B为同一主族元素,Ge原子比B原子多两个电子层,则Ge的原子序数为___________ 。
(1)B、F元素分别为
(2)E元素在周期表中的位置是
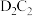 的电子式为
的电子式为(3)C、D、F三种元素形成的简单离子,其半径由大到小的顺序是
(4)C、F两种元素简单气态氢化物的稳定性:
(5)E的最高价氧化物对应的水化物可用于治疗胃酸过多,反应的离子方程式为
(6)锗(Ge)与元素B为同一主族元素,Ge原子比B原子多两个电子层,则Ge的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如图所示是部分短周期元素原子半径与原子序数的关系,回答下列问题:
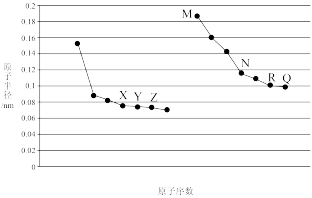
(1)X在周期表中的位置是_______ 。
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是_______ 。(填化学式)。
(3)用电子式表示化合物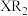 的形成过程
的形成过程_______ 。
(4)请写出实验室制备Y的气态氢化物的化学方程式_______ 。
(5)写出 的结构式
的结构式_______ 。
(6)均含有M、Z、R和H四种元素的两种化合物反应的化学方程式为_______ 。

(1)X在周期表中的位置是
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是
(3)用电子式表示化合物
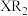 的形成过程
的形成过程(4)请写出实验室制备Y的气态氢化物的化学方程式
(5)写出
 的结构式
的结构式(6)均含有M、Z、R和H四种元素的两种化合物反应的化学方程式为
您最近一年使用:0次



