某容器中发生一个化学反应,反应过程中存在Fe2+、 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、 的质量分数(w)随时间变化的曲线如图所示,下列有关判断中错误的是
的质量分数(w)随时间变化的曲线如图所示,下列有关判断中错误的是

 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、 的质量分数(w)随时间变化的曲线如图所示,下列有关判断中错误的是
的质量分数(w)随时间变化的曲线如图所示,下列有关判断中错误的是
A.在反应中 被还原,发生还原反应 被还原,发生还原反应 |
B.还原性:Fe2+> |
| C.该反应中Fe2+被还原为Fe3+ |
| D.在反应中参加反应的还原剂与氧化剂的个数之比为8:1 |
20-21高一上·河北石家庄·期中 查看更多[9]
陕西省西安市碑林区教育局2023-2024学年高一上学期期中教育质量监测化学试题新疆乌鲁木齐市第101中学2023-2024学年高三上学期8月月考化学试题微专题(四) 氧化还原反应的简单规律及应用云南省富宁县第一中学2021-2022学年高一下学期开学考试化学试题浙江省北斗联盟2022-2023学年高一上学期期中考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期开学考试化学试题辽宁省葫芦岛市第八高级中学2022届高三上学期10月月考化学试题河北省衡水市武强中学2021-2022学年高一上学期第一次月考化学试题河北省石家庄市第二十三中学2020-2021学年高一上学期期中考试化学试题
更新时间:2021-09-12 13:41:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2 4NO+6H2O,对于该反应判断正确的是( )
4NO+6H2O,对于该反应判断正确的是( )
 4NO+6H2O,对于该反应判断正确的是( )
4NO+6H2O,对于该反应判断正确的是( )| A.氨气是氧化剂 |
| B.该反应是置换反应 |
| C.氧气被还原 |
| D.若有17g氨参加反应,反应中转移10mol电子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
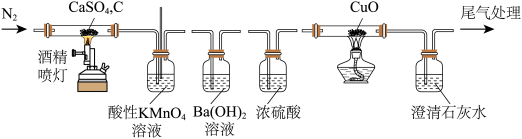
【推荐2】工业上用碳粉在高温条件下还原CaSO4可以生产脱毛剂、杀虫剂CaS,反应的化学方程式为C+CaSO4 CaS+CaO+SO2↑+CO↑+CO2↑(未配平)。下列说法错误的是
CaS+CaO+SO2↑+CO↑+CO2↑(未配平)。下列说法错误的是
 CaS+CaO+SO2↑+CO↑+CO2↑(未配平)。下列说法错误的是
CaS+CaO+SO2↑+CO↑+CO2↑(未配平)。下列说法错误的是
| A.两种含硫产物均属于还原产物 |
| B.改变碳粉用量可能使产物与上述产物不同 |
| C.参加反应的n(C):n(CaSO4)=3:2时,会生成4mol气体 |
| D.用图示装置可检验三种气体产物(试剂均足量) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氢化铝锂(LiAlH4)和硼氢化钠(NaBH4)在有机合成中非常重要,可发生如下反应:①LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑②NaBH4+NH4Cl=NH3BH3+NaCl+H2↑,则下列说法错误的是 ( )
| A.LiAlH4中H元素为-1价 |
| B.反应②中,每生成1 mol NH3BH3会转移2 mol e- |
| C.两个反应中,H2均既是氧化产物,又是还原产物 |
| D.NH4Cl和NaBH4所含化学键类型相同 |
您最近半年使用:0次
【推荐1】下列转化及解释均正确的是
| 转化 | 解释 | |
| A | CuS+H2SO4=CuSO4+H2S↑ | 酸性:H2SO4>H2S |
| B | AgCl(s)+I-(aq)⇌AgI(s)+Cl-(aq) | Ksp(AgCl)<Ksp(AgI) |
| C | 2Fe+3Cl2 2FeCl3;Fe+S 2FeCl3;Fe+S FeS FeS | 氧化性:Cl2>S |
| D | C(s,石墨)=C(s,金刚石)△H=+1.9kJ/mol | 稳定性:石墨 金刚石 金刚石 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
【推荐2】已知反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列关于该反应的说法正确的是
| A.Na2O2中的氧元素全部被还原 |
| B.氧化性:Na2O2<Na2FeO4 |
| C.每生成1个Na2FeO4,反应有4个电子转移 |
| D.Na2O为还原产物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知:①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
下列结论正确的是
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
下列结论正确的是
| A.①②③均是氧化还原反应 |
| B.氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2 |
| C.反应②中氧化剂与还原剂的物质的量之比为6:1 |
| D.反应③中0.1mol还原剂共失去电子数为NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】工业上常用浓氨水检验氯气管道,其反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2,利用该反应中产生白烟这一现象来判断管道是否漏气。下列关于该反应的说法错误的是
| A.氧化剂是Cl2,N2是氧化产物 |
| B.每生成22.4L的N2,转移6mol电子 |
| C.氧化剂与还原剂的物质的量之比为3∶2 |
| D.被氧化与未被氧化的NH3的物质的量之比为1∶3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】新型锂电池的电极材料LiFePO4可通Li2CO3+H2C2O4+2FePO4=2LiFePO4+H2O+3CO2制得。该电池充电时,LiFePO4变成Li1-xFePO4(0<x<1)。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是
| A.该制备原理中H2C2O4作氧化剂 |
| B.由LiFePO4变成Li1-xFePO4时,属于还原反应 |
| C.常温常压下生成4.4gCO2时,反应中转移0.1mol电子 |
| D.当Li1-xFePO4中x=0.4时,Li1-xFePO4中的Fe2+和Fe3+的个数值比为3∶2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】分析含有少量NaOH的NaClO溶液与FeSO4溶液的反应。
已知:①图1表示将FeSO4溶液逐滴滴加到含少量NaOH的NaClO溶液中的pH变化;②图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系[注:饱和NaClO溶液的pH约为11; Ksp[Fe(OH)3]=2.8×10−39]。
已知:①图1表示将FeSO4溶液逐滴滴加到含少量NaOH的NaClO溶液中的pH变化;②图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系[注:饱和NaClO溶液的pH约为11; Ksp[Fe(OH)3]=2.8×10−39]。
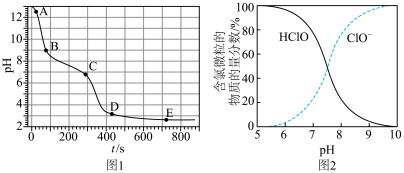
A.A点溶液的pH约为13,主要原因是ClO− + H2O HClO + OH− HClO + OH− |
| B.AB段pH显著下降的原因是5ClO-+2Fe2+ + 5H2O=Cl−+ 2Fe(OH)3↓+ 4HClO |
| C.CD段较BC段pH下降快的主要原因是HClO+2Fe2+ +5H2O=2Fe(OH)3↓+Cl-+ 5H+ |
| D.反应进行至400s时溶液中产生Cl2的原因是:ClO-+ Cl-+2H+=Cl2↑+ H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,通过下列实验探究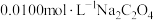 溶液的性质。
溶液的性质。
实验1:实验测得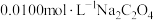 溶液的pH为8.6。
溶液的pH为8.6。
实验2:向溶液中滴加等体积 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积 溶液,出现白色沉淀。
溶液,出现白色沉淀。
实验4:向稀硫酸酸化的 溶液中滴加
溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。
已知室温时 ,下列说法错误的是
,下列说法错误的是
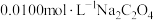 溶液的性质。
溶液的性质。实验1:实验测得
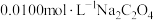 溶液的pH为8.6。
溶液的pH为8.6。实验2:向溶液中滴加等体积
 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。实验3:向溶液中加入等体积
 溶液,出现白色沉淀。
溶液,出现白色沉淀。实验4:向稀硫酸酸化的
 溶液中滴加
溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。已知室温时
 ,下列说法错误的是
,下列说法错误的是A.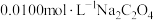 溶液中满足: 溶液中满足: |
B.实验2滴加盐酸过程中存在某一点满足: |
C.实验3所得上层清液中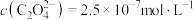 |
D.实验4发生反应的离子方程式为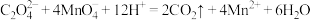 |
您最近半年使用:0次

 该反应中,被氧化与被还原的氯原子个数之比为
该反应中,被氧化与被还原的氯原子个数之比为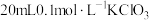 溶液和
溶液和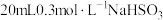 溶液,
溶液, 随时间变化的曲线如图所示。下列说法错误的是
随时间变化的曲线如图所示。下列说法错误的是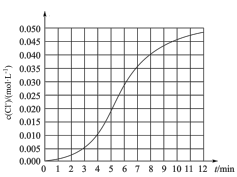
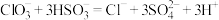
 和
和 的浓度之比为1∶1
的浓度之比为1∶1

