室温下,通过下列实验探究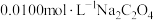 溶液的性质。
溶液的性质。
实验1:实验测得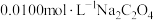 溶液的pH为8.6。
溶液的pH为8.6。
实验2:向溶液中滴加等体积 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积 溶液,出现白色沉淀。
溶液,出现白色沉淀。
实验4:向稀硫酸酸化的 溶液中滴加
溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。
已知室温时 ,下列说法错误的是
,下列说法错误的是
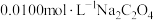 溶液的性质。
溶液的性质。实验1:实验测得
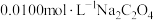 溶液的pH为8.6。
溶液的pH为8.6。实验2:向溶液中滴加等体积
 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。实验3:向溶液中加入等体积
 溶液,出现白色沉淀。
溶液,出现白色沉淀。实验4:向稀硫酸酸化的
 溶液中滴加
溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。已知室温时
 ,下列说法错误的是
,下列说法错误的是A.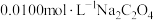 溶液中满足: 溶液中满足: |
B.实验2滴加盐酸过程中存在某一点满足: |
C.实验3所得上层清液中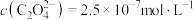 |
D.实验4发生反应的离子方程式为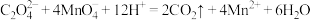 |
更新时间:2022-09-29 17:28:04
|
相似题推荐
【推荐1】《环境科学》刊发了我国科研部门采用零价铁活化过二硫酸钠(Na2S2O3)去除废水中的正五价砷[ As( V) ]的研究成果,其反应机理如图所示。下列叙述错误的是
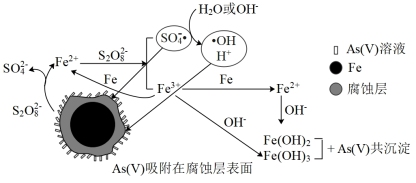

| A.1.0 mol过二硫酸钠含有1.0 mol过氧键 |
B.56gFe参加反应,共有1.0mol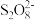 被还原 被还原 |
| C.零价铁活化去除砷[ As( V)]的机理主要包括还原、吸附和共沉淀 |
D.碱性条件下,硫酸根自由基发生的反应为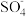 ·+OH-= ·+OH-=  +·OH +·OH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2005年10月12日,我国“神舟六号”载人飞船成功发射。航天飞船是用铝粉与高氯酸铵的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应: 2NH4ClO4 = N2↑+ 4H2O + Cl2 + 2O2↑;Δ H <0 下列对该反应的叙述中不正确的是 ( )
| A.高氯酸铵的水溶液呈中性 |
| B.每生成2 mol O2,反应中转移的电子数为14mol |
| C.该反应中Cl2是还原产物,N2和O2是氧化产物 |
| D.该反应是焓减,熵增的反应,能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,用0.1000 mol·L-1NaOH 溶液滴定0.1000 mol·L-1H3PO4溶液,滴定曲线如图所示,滴定分数是指滴定剂与被滴定物质的物质的量之比。下列说法正确的是


A.当滴定分数为1.00时,溶液中c(H3PO4)>c( ) ) |
| B.在滴定过程中,水的电离程度先增大后减小,水的电离程度最大时对应的滴定分数在1.00和2.00之间 |
| C.当滴定分数为2.00时,生成物的主要成分为Na3PO4 |
D.当滴定分数为1.50时,溶液中存在关系式:2c(H+)+3c(H3PO4)+c( )=3c( )=3c( )+c( )+c( )+2c(OH-) )+2c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.10mol·L-1NaOH溶液滴定10 mL0.10mol·L-1H2A溶液,测得滴定曲线如图,下列说法正确的是


| A.溶液①中H2A的电离方程式是H2A=2H++A2- |
| B.溶液②中c(HA-)>c(A2-)>c(H2A) |
| C.溶液③中c(Na+)=c(HA-)+c(A2-) |
| D.溶液④中2c(Na+)=c(A2-)+c(HA-)+c(H2A) |
您最近一年使用:0次
单选题
|
适中
(0.65)
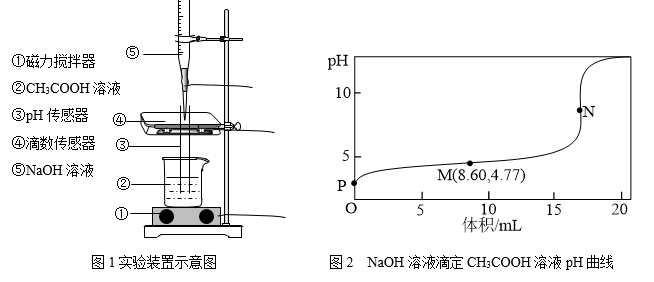
【推荐3】25℃下,某同学按图1所示,边用磁力搅拌器搅拌边向20.00mL浓度为 的
的 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
 的
的 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
A.25℃时, 的电离常数 的电离常数 的数量级为 的数量级为 |
B.N点溶液中: |
C.水的电离程度: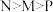 |
D.M点溶液中: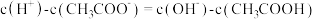 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种废电解质渣(Ni、Fe、Cu及NH4F)制备NiCO3的工艺流程如下:

已知:①25℃时,一些金属氢氧化物沉淀时的pH如下:
②25℃时, ,
, ,
, ;
;
③某离子沉淀完全时,其浓度
下列说法错误的是

已知:①25℃时,一些金属氢氧化物沉淀时的pH如下:
 |  |  |  | |
| 开始沉淀的pH | 2.3 | 6.8 | 4.2 | 7.0 |
| 完全沉淀的pH | 3.2 | 8.3 | 6.7 | 9.5 |
 ,
, ,
, ;
;③某离子沉淀完全时,其浓度

下列说法错误的是
A.“洗脱”可去除 ,所得滤液显酸性 ,所得滤液显酸性 |
| B.“酸浸”可选用30%盐酸代替20%硝酸 |
| C.“调pH”应调整pH的范围为6.7~7.0 |
D.“沉镍”使 沉淀完全,应控制溶液中 沉淀完全,应控制溶液中 |
您最近一年使用:0次
【推荐2】在 时,
时,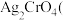 橘红色
橘红色 在水中的沉淀溶解平衡平衡曲线如图所示。又知
在水中的沉淀溶解平衡平衡曲线如图所示。又知 时AgCl的
时AgCl的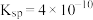 ,下列说法不正确的是
,下列说法不正确的是
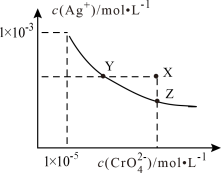
 时,
时, 橘红色
橘红色 在水中的沉淀溶解平衡平衡曲线如图所示。又知
在水中的沉淀溶解平衡平衡曲线如图所示。又知 时AgCl的
时AgCl的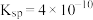 ,下列说法不正确的是
,下列说法不正确的是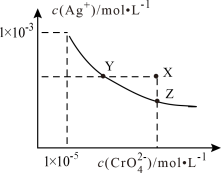
A.在 时, 时, 的Ksp为 的Ksp为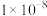 |
B.在 饱和溶液中加入 饱和溶液中加入 可使溶液由Y点到Z点 可使溶液由Y点到Z点 |
C.在 时, 时,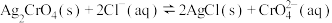 平衡常数 平衡常数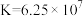 |
D.在 时,以0.001 mol/LAgNO3溶液滴定20 mL0.001 mol/L KCl和0.001 mol/L的 时,以0.001 mol/LAgNO3溶液滴定20 mL0.001 mol/L KCl和0.001 mol/L的 的混合溶液, 的混合溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.25℃时,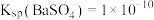 ,则1 L饱和BaSO4溶液中Ba2+数目为10-5NA ,则1 L饱和BaSO4溶液中Ba2+数目为10-5NA |
| B.25℃时,1 LpH=13的Ba(OH)2溶液中含有OH-数目为0.1NA |
C.25℃时,1 L0.1 mol/L的NH4Cl溶液中 数目为0.1NA 数目为0.1NA |
| D.H2和N2充分反应生成0.2 mol NH3时,转移电子数为0.6NA |
您最近一年使用:0次



