铝土矿是生产金属铝的最佳原料,也是最主要的应用领域,其用量占世界铝土矿总产量的90%以上。以铝土矿(主要成分为Al2O3,含有Fe2O3和SiO2)等杂质)为原料,制备有机合成中的重要还原剂铝氢化钠(NaAlH4) 的一种工业流程如图:

已知: AlCl3、 NaH、NaAlH4遇水都能迅速发生反应。
(1)写出碱溶时发生反应的离子方程式:_______ 、_______ 。
(2)滤渣I中的主要成分为_______ (写物质名称)。
(3)写出反应I中主要反应的化学方程式:_______ 。
(4)甲同学设计了如图实验装置在实验室模拟制备无水氯化铝,应用该装置制备无水氯化铝,B、C中的试剂分别为_______ 和_______ 。

(5)A中发生反应的化学方程式为_______ ;该反应中氧化剂和还原剂的物质的量之比为_______ 。
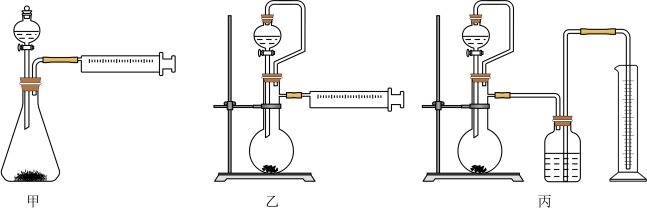
(6)乙同学设计了以下三种装置测定工业制取的铝氢化钠样品的纯度,从易操作、准确性角度考虑宜选择的装置是_______ (填“甲”“乙”或“丙”)

已知: AlCl3、 NaH、NaAlH4遇水都能迅速发生反应。
(1)写出碱溶时发生反应的离子方程式:
(2)滤渣I中的主要成分为
(3)写出反应I中主要反应的化学方程式:
(4)甲同学设计了如图实验装置在实验室模拟制备无水氯化铝,应用该装置制备无水氯化铝,B、C中的试剂分别为

(5)A中发生反应的化学方程式为
(6)乙同学设计了以下三种装置测定工业制取的铝氢化钠样品的纯度,从易操作、准确性角度考虑宜选择的装置是

更新时间:2021-09-24 11:05:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】如图所示, 某小组同学拟利用下列仪器,在实验室中制备干燥、纯净的氯气。请完成下列空白。


(1)上述仪器正确连接后应进行的操作是_______ 。
(2)实验室制备氯气反应的化学方程式是_______ 。
(3)饱和食盐水的作用是_______ ,浓硫酸的作用是_______ 。
(4)为防止污染空气,实验时图中烧杯所盛溶液化学式为_______ ,发生反应的离子 方程式是_______ 。
(5)下列说法正确的是_______ 。


(1)上述仪器正确连接后应进行的操作是
(2)实验室制备氯气反应的化学方程式是
(3)饱和食盐水的作用是
(4)为防止污染空气,实验时图中烧杯所盛溶液化学式为
(5)下列说法正确的是_______ 。
| A.钠、铁和铜都能和氯气反应, 生成金属氯化物 |
| B.液氯是氯气的水溶液,它能使干燥的有色布条褪色 |
| C.氢气在氯气中燃烧, 发出苍白色火焰 |
| D.氯水中含有次氯酸,氯水具有杀菌、漂白作用 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。

(1)用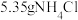 固体与足量
固体与足量 反应,最多可制得标准状况下氨气的体积为
反应,最多可制得标准状况下氨气的体积为_______ L。
(2)B装置中的干燥剂可选用_______ (填名称),F装置的作用为_______ 。
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:_______ 。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐陵,可观察到的现象是_______ 。
(5)在BC间增加一个集气瓶可用于收集氨气。检验氨气是否收集满的方法是_______ 。

(1)用
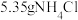 固体与足量
固体与足量 反应,最多可制得标准状况下氨气的体积为
反应,最多可制得标准状况下氨气的体积为(2)B装置中的干燥剂可选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐陵,可观察到的现象是
(5)在BC间增加一个集气瓶可用于收集氨气。检验氨气是否收集满的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
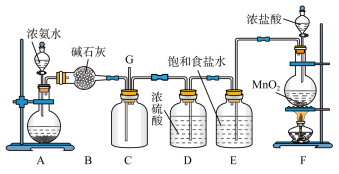
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用________ (填字母)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)B装置的作用是___________________ ;
(3)装置F中发生反应的化学方程式是________________ 。
(4)通入C装置的左右两根导管左边较长、右边较短,目的_______________ 。
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?_____________________ 。

请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)B装置的作用是
(3)装置F中发生反应的化学方程式是
(4)通入C装置的左右两根导管左边较长、右边较短,目的
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某铜矿石的主要成分是Cu2O,还含有少量的Al2O3、Fe2O3和 SiO2。某工厂利用此矿石炼制粗铜的工艺流程如图所示(已知:Cu2O+2H+=Cu+Cu2++H2O)。

请结合流程图回答下列问题:
(1)滤液A中铁元素的存在形式为________ (填离子符号),生成该离子的离子方程式为____________ 。
(2)已知滤液C的主要成分为NaAlO2溶液,请写出由滤液A生成滤液C的离子方程式____________ 。
(3)固体F中有两种物质,一种是黑色固体,另一种为______ (填化学式),生成黑色固体的化学方程式为___________ 。
(4)已知废液的主要成分是Na2SiO3溶液。固体混合物B中加入溶液G发生反应的离子方程式为_________ ;反应后,实现铜与废液分离的实验操作为_______ (填实验名称)。

请结合流程图回答下列问题:
(1)滤液A中铁元素的存在形式为
(2)已知滤液C的主要成分为NaAlO2溶液,请写出由滤液A生成滤液C的离子方程式
(3)固体F中有两种物质,一种是黑色固体,另一种为
(4)已知废液的主要成分是Na2SiO3溶液。固体混合物B中加入溶液G发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图中的每一方格表示相关的一种反应物或生成物。其中B是一种单质,其余物质也都是含有B元素的化合物。C是一种钠盐,E是C对应的酸,B的结构类似金刚石,D为氧化物。
请回答下列问题:
(1)A、D、E的化学式分别为________ 、________ 、________ 。
(2)A和B的互相转化在工业上有什么实际意义?_____________________ 。
(3)写出D→C反应的化学方程式:_____________________ 。
(4)写出E→D反应的化学方程式:_____________________ 。

请回答下列问题:
(1)A、D、E的化学式分别为
(2)A和B的互相转化在工业上有什么实际意义?
(3)写出D→C反应的化学方程式:
(4)写出E→D反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组用铬铁矿(FeCr2O4,含Al、Si氧化物等杂质)为主要原料制备K2Cr2O7晶体,流程如下:
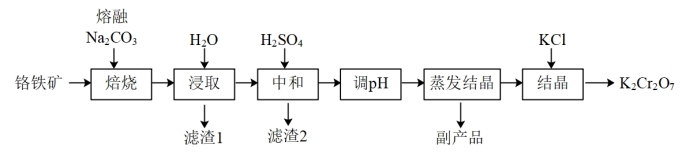
(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,并将Al、Si氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是___________ 。该步骤不能使用陶瓷容器,原因是___________ 。
(2)滤渣2的主要成份是Al(OH)3和___________ 。
(3)流程中调溶液的pH使之变___________ (填“大”或“小”),原因是___________ (用离子方程式表示)。
(4)蒸发结晶所产生的副产品是___________ 。
(5)为结晶得到杂质较少的K2Cr2O7粗产品,请结合下图从下列选项中选出合理的操作并排序___________ 。

a.50℃蒸发溶剂
b.100℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液出现大量晶体,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O460%)制备K2Cr2O7,最终得到产品m2kg,产率为___________ (列出计算式)。

(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,并将Al、Si氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是
(2)滤渣2的主要成份是Al(OH)3和
(3)流程中调溶液的pH使之变
(4)蒸发结晶所产生的副产品是
(5)为结晶得到杂质较少的K2Cr2O7粗产品,请结合下图从下列选项中选出合理的操作并排序

a.50℃蒸发溶剂
b.100℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液出现大量晶体,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O460%)制备K2Cr2O7,最终得到产品m2kg,产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为:_______________ (注明试剂、现象)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________ (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边___________________ (填操作名称)、过滤、洗涤。
④高铁酸钠(Na2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与漂白液(主要成分NaClO)在强碱性条件下反应可制取Na 2FeO4,反应的离子方程式为___________________________ 。
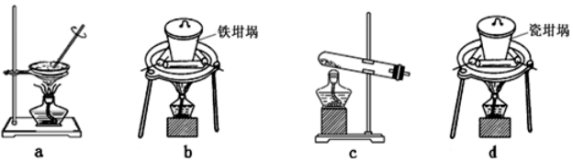
(2) ①SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______________ (填代号)。
②过量CO2通入到硅酸钠的溶液中,然后加热蒸干,再高温灼烧,最后所得固体成分___________ 。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边
④高铁酸钠(Na2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与漂白液(主要成分NaClO)在强碱性条件下反应可制取Na 2FeO4,反应的离子方程式为
(2) ①SiO2和NaOH焙烧制备硅酸钠,可采用的装置为

②过量CO2通入到硅酸钠的溶液中,然后加热蒸干,再高温灼烧,最后所得固体成分
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某混合物A含有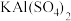 、
、 和
和 ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
 、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是______ .
 根据上述框图反应关系,写出下列B、D所含物质的化学式固体B
根据上述框图反应关系,写出下列B、D所含物质的化学式固体B______ ;沉淀D______ ;
 写出
写出 的化学方程式
的化学方程式 _____________ ;
 写出
写出 、
、 两个反应的离子方程式
两个反应的离子方程式
___________________ ;
_______________ ;
(5)写出 在工业上的一种主要用途:
在工业上的一种主要用途:_________________ 。
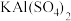 、
、 和
和 ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:
据此回答下列问题:
 、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是 根据上述框图反应关系,写出下列B、D所含物质的化学式固体B
根据上述框图反应关系,写出下列B、D所含物质的化学式固体B 写出
写出 的化学方程式
的化学方程式  写出
写出 、
、 两个反应的离子方程式
两个反应的离子方程式

(5)写出
 在工业上的一种主要用途:
在工业上的一种主要用途:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某矿渣的成分为Cu2O、Al2O3、Fe2O3、FeO、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如图:
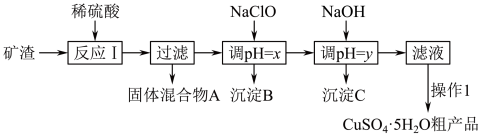
已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
(1)为了加快反应Ⅰ的速率,可以采取的措施是_________ (任写1条)。
(2)固体混合物A中的成分是_______ 。
(3)操作1主要包括:_____ 、_____ 、_______ 。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是________ 。
(4)用NaClO调pH可以生成沉淀B,利用题中所给信息分析沉淀B为______ ,该反应中氧化剂与还原剂的物质的量之比为______ 。
(5)用NaOH调pH可以生成沉淀C,利用题中所给信息分析y的范围为______ 。

已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是
(2)固体混合物A中的成分是
(3)操作1主要包括:
(4)用NaClO调pH可以生成沉淀B,利用题中所给信息分析沉淀B为
(5)用NaOH调pH可以生成沉淀C,利用题中所给信息分析y的范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。工业上用铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。
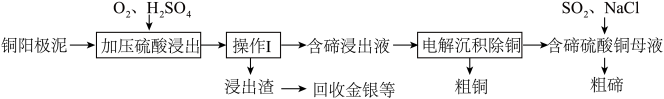
已知: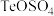 为正盐。
为正盐。
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应: ;
; 。“含碲浸出液”的溶质成分除了
。“含碲浸出液”的溶质成分除了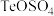 外,主要是
外,主要是_______ (填化学式)。
(2)操作Ⅰ的分离方法是_______ 。
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应是_______ 。
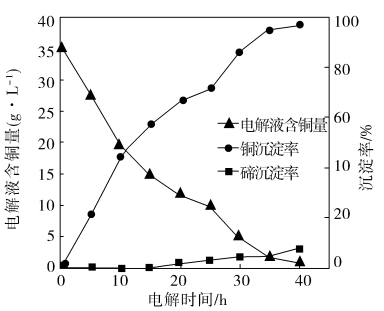
(4)通过图像分析,你认为工业上该过程持续的时段最好是_______(填标号)。
(5)向“含碲硫酸铜母液”中通入 并加入NaCl反应一段时间后,Te(Ⅳ)浓度从
并加入NaCl反应一段时间后,Te(Ⅳ)浓度从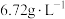 下降到
下降到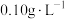 ,该过程生成粗碲的离子方程式:
,该过程生成粗碲的离子方程式:_______ 。
(6)25℃时,亚碲酸 的
的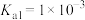 ,
,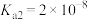 。
。
①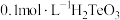 的pH约为
的pH约为_______ 。
② 的
的 溶液中,下列粒子的物质的量浓度关系正确的是
溶液中,下列粒子的物质的量浓度关系正确的是_______ (填标号)。
A.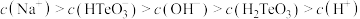
B.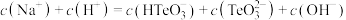
C.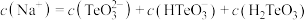
D.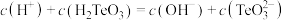

已知:
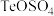 为正盐。
为正盐。(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:
 ;
; 。“含碲浸出液”的溶质成分除了
。“含碲浸出液”的溶质成分除了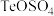 外,主要是
外,主要是(2)操作Ⅰ的分离方法是
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应是

(4)通过图像分析,你认为工业上该过程持续的时段最好是_______(填标号)。
| A.20h | B.30h | C.35h | D.40h |
 并加入NaCl反应一段时间后,Te(Ⅳ)浓度从
并加入NaCl反应一段时间后,Te(Ⅳ)浓度从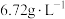 下降到
下降到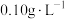 ,该过程生成粗碲的离子方程式:
,该过程生成粗碲的离子方程式:(6)25℃时,亚碲酸
 的
的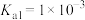 ,
,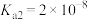 。
。①
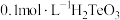 的pH约为
的pH约为②
 的
的 溶液中,下列粒子的物质的量浓度关系正确的是
溶液中,下列粒子的物质的量浓度关系正确的是A.
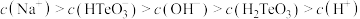
B.
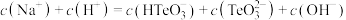
C.
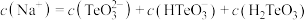
D.
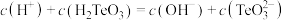
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,易溶于水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[(NH4)2Fe(SO4)2·6H2O]制备K3[Fe(C2O4)3]·3H2O的流程如图所示。

回答下列问题:
(1)K3[Fe(C2O4)3]中铁离子的配位数为___ ,其配体C2O 中C原子的杂化方式为
中C原子的杂化方式为___ 。
(2)步骤②发生反应的化学方程式为___ 。
(3)步骤③将Fe(OH)3加入到KHC2O4溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量___ (已知:常温下KHC2O4溶液的pH约为3.5)。
(4)得到的三草酸合铁酸钾晶体依次用少量冰水、95%乙醇洗涤的目的是___ 。
(5)某研究小组将K3[Fe(C2O4)3]·3H2O在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有CO和CO2。

①按气流从左到右的方向,依次连接的合理顺序为___ (填装置序号)。
②确认气体产物中含CO的现象为___ 。
(6)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,[Ni(NH3)6]SO4中配体的构型是___ ,阴离子的立体构型是___ 。

回答下列问题:
(1)K3[Fe(C2O4)3]中铁离子的配位数为
 中C原子的杂化方式为
中C原子的杂化方式为(2)步骤②发生反应的化学方程式为
(3)步骤③将Fe(OH)3加入到KHC2O4溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量
(4)得到的三草酸合铁酸钾晶体依次用少量冰水、95%乙醇洗涤的目的是
(5)某研究小组将K3[Fe(C2O4)3]·3H2O在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有CO和CO2。

①按气流从左到右的方向,依次连接的合理顺序为
②确认气体产物中含CO的现象为
(6)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,[Ni(NH3)6]SO4中配体的构型是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】湿法炼锌综合回收系统的萃余液中含有 、
、 、
、 ,还含有
,还含有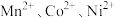 、
、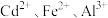 等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:

(1)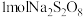 中过氧键的数目为
中过氧键的数目为___________  (设
(设 为阿伏加德罗常数的值);其氧化
为阿伏加德罗常数的值);其氧化 的离子方程式为
的离子方程式为___________ 。
(2)常温下,部分难溶化合物的溶度积相关数据如下表所示:
“调 ”时,应控制
”时,应控制 的范围为
的范围为___________ 。(已知溶液中 ;当溶液中某离子浓度
;当溶液中某离子浓度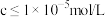 时,可视为沉淀完全)
时,可视为沉淀完全)
(3)“除镉”时所得“滤渣2”主要成分为___________ (写化学式)。
(4)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为___________ 。
(5)“沉锌”所得滤液经处理可得 溶液,已知
溶液,已知 的溶解度随温度变化如图1所示,由该溶液制备芒硝
的溶解度随温度变化如图1所示,由该溶液制备芒硝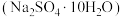 的操作为
的操作为___________ 、过滤、洗涤、干燥。
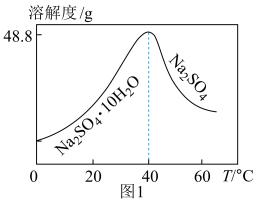
(6)一种 的立方晶胞结构如图2所示,已知晶胞参数为
的立方晶胞结构如图2所示,已知晶胞参数为 ,密度为
,密度为 ,则NA=
,则NA=________ mol-1(用含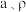 的计算表达式表示)。
的计算表达式表示)。

 、
、 、
、 ,还含有
,还含有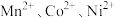 、
、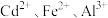 等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
(1)
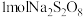 中过氧键的数目为
中过氧键的数目为 (设
(设 为阿伏加德罗常数的值);其氧化
为阿伏加德罗常数的值);其氧化 的离子方程式为
的离子方程式为(2)常温下,部分难溶化合物的溶度积相关数据如下表所示:
| 化合物 |  |  |  |
 近似值 近似值 | 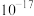 | 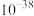 |  |
 ”时,应控制
”时,应控制 的范围为
的范围为 ;当溶液中某离子浓度
;当溶液中某离子浓度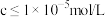 时,可视为沉淀完全)
时,可视为沉淀完全)(3)“除镉”时所得“滤渣2”主要成分为
(4)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为
(5)“沉锌”所得滤液经处理可得
 溶液,已知
溶液,已知 的溶解度随温度变化如图1所示,由该溶液制备芒硝
的溶解度随温度变化如图1所示,由该溶液制备芒硝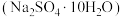 的操作为
的操作为
(6)一种
 的立方晶胞结构如图2所示,已知晶胞参数为
的立方晶胞结构如图2所示,已知晶胞参数为 ,密度为
,密度为 ,则NA=
,则NA=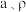 的计算表达式表示)。
的计算表达式表示)。
您最近一年使用:0次



