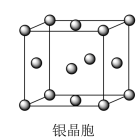
下面的叙述不正确的是
| A.晶胞空间利用率:金属镁>金属钾>金属钋 |
B.六方最密堆积(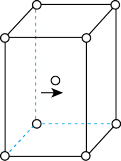 )晶胞中原子个数的计算: )晶胞中原子个数的计算: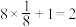 |
C.酸性: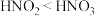 ; ;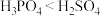 |
| D.SF6的空间构型为正八面体,在氧气中不能燃烧 |
20-21高二上·四川内江·期中 查看更多[2]
更新时间:2021-09-26 20:31:12
|
相似题推荐
【推荐1】下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 液氨常用作制冷剂 | 氨分子间能形成氢键 |
| B | 电解氯化镁溶液可制得金属 |  可在电解池的阴极还原成 可在电解池的阴极还原成 |
| C | 热的 溶液可去除油污 溶液可去除油污 |  能与油污中的羧基反应 能与油污中的羧基反应 |
| D |  的硫酸中 的硫酸中 浓度大于同 浓度大于同 的醋酸 的醋酸 | 硫酸是强酸,醋酸是弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科学家通过以下方法合成了具有半导体性能的C18,设NA为阿伏加德罗常数的值,下列说法错误的是
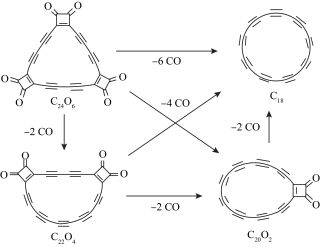

| A.C18、C60与石墨互为同素异形体 |
| B.由C24O6生成1molC22O4,碳碳三键的数目增加NA |
| C.C20O2和C22O4分子中碳原子的杂化方式相同 |
| D.图中涉及的5种分子除CO外均为非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实的解释不正确的是
| 事实 | 解释 | |
| A | 苯与液溴在催化剂作用下生成溴苯,稀的苯酚溶液与浓溴水作用生成三溴苯酚白色沉淀 | 羟基对苯环的影响使得苯环上的氢原子更易被取代 |
| B | CH 中H-C-H键角比CH 中H-C-H键角比CH 中的大 中的大 | 中心原子的孤电子对数目CH >CH >CH ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 |
| C | 晶体熔点:HF>HCl | HF分子间能形成氢键 |
| D | 酸性:CF3COOH>CCl3COOH | 氟的电负性大于氯的电负性,F-C的极性大于Cl-C的性,使-CF3的极性大于-CCl3的极性,导致CF3COOH的羧基中的羟基的极性更大,更易电离出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于BeF2和SF2的说法错误的是
| A.BeF2分子中,中心原子Be的价层电子对数等于2,成键电子对数也等于2 |
| B.BeF2分子的孤电子对数为0 |
| C.SF2分子中,中心原子S的价层电子对数等于4,其空间结构为四面体形,成键电子对数等于2,没有孤电子对 |
| D.在气相中,BeF2是直线形而SF2是V形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】元素X的某价态离子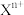 中所有电子正好充满K、L、M三个电子层,它与
中所有电子正好充满K、L、M三个电子层,它与 形成晶体的晶胞结构如图所示(已知该晶胞参数
形成晶体的晶胞结构如图所示(已知该晶胞参数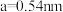 )。下列说法错误的是
)。下列说法错误的是

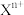 中所有电子正好充满K、L、M三个电子层,它与
中所有电子正好充满K、L、M三个电子层,它与 形成晶体的晶胞结构如图所示(已知该晶胞参数
形成晶体的晶胞结构如图所示(已知该晶胞参数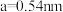 )。下列说法错误的是
)。下列说法错误的是
| A.X元素的原子序数是29 |
B.两个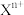 最近距离为 最近距离为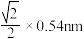 |
C.该晶体中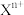 与 与 配位数之比为3:1 配位数之比为3:1 |
D.该晶体的密度为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氮化硅(Si3N4)是一种重要的结构陶瓷材料。用石英砂和原料气(含N2和少量O2)制备Si3N4的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物),下列叙述不正确的是




| A.“还原”时焦炭主要被氧化为CO2 |
B.“高温氮化”反应的化学方程式为3Si+2N2 Si3N4 Si3N4 |
| C.“操作X”可将原料气通过灼热的铜粉 |
| D.AgI晶胞中含4个I- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钠晶体(如图)为体心立方晶胞,晶胞的边长为a,假定金属钠原子为等径的刚性球,且晶胞中处于体对角线上的三个球相切,则钠原子的半径r为( )
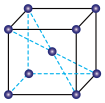

A. | B.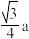 | C.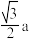 | D.2a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法不正确的是( )
A.水合铜离子的模型如图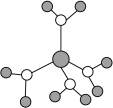 ,该微粒中存在极性共价键、配位键 ,该微粒中存在极性共价键、配位键 |
B.CaF2晶体的晶胞如图 ,距离F-最近的Ca2+组成正四面体 ,距离F-最近的Ca2+组成正四面体 |
C.氢原子的电子云图如图 ,氢原子核外大多数电子在原子核附近运动 ,氢原子核外大多数电子在原子核附近运动 |
D.金属Cu中Cu原子堆积模型如图 ,为面心立方最密堆积,Cu原子的配位数均为12 ,为面心立方最密堆积,Cu原子的配位数均为12 |
您最近一年使用:0次


 )分别为578、1817、2745、11575、14830、18376,当它与氯气反应时可能生成的阳离子是
)分别为578、1817、2745、11575、14830、18376,当它与氯气反应时可能生成的阳离子是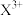
 晶胞中含有8个
晶胞中含有8个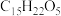 ,结构如图所示,该分子中包含7个手性碳原子
,结构如图所示,该分子中包含7个手性碳原子 晶胞相似)。下列有关说法正确的是
晶胞相似)。下列有关说法正确的是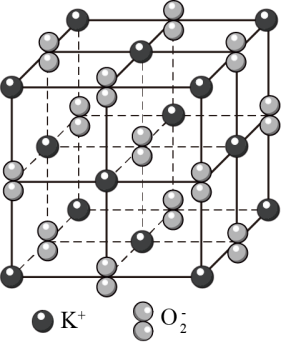
 等距且紧邻的
等距且紧邻的