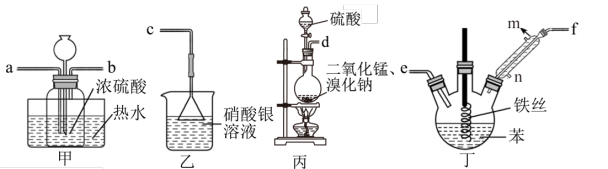
和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯
和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯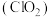 气体,该反应的化学方程式为
气体,该反应的化学方程式为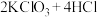 (浓)
(浓) 。
。(1)该反应的氧化剂是

 (填< > =)。
(填< > =)。(2)用双线桥在方程式中标出电子转移的情况:
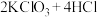 (浓)
(浓) 。
。(3)以上反应中盐酸具有的性质是___________(填序号)。
| A.只有还原性 | B.只有氧化性 |
| C.还原性和酸性 | D.氧化性和还原性,还有酸性 |
| A.NaOH | B.NaCl | C.KCl | D. |
更新时间:2021-10-22 13:04:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝,这是因为_______ ,离子方程式是_______ 。在上述蓝色溶液中滴加少量的Na2SO3 ,蓝色逐渐消失,这是因为:_______ ,离子方程式是_______ 。以上实验条件下,ClO-、I2、SO 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是_______ 。
 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”,发生反应:Cu+Fe3+→Cu2++Fe2+
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
(1)配平写出i中反应的离子方程式:___________ 。
(2)反应ii中氧化剂与还原剂的物质的量之比为___________ ,用双线桥法标出电子转移的方向与数目:___________ ,当反应中有0.6mol电子转移时,生成NO的体积为___________ L(标准状况)。
(3)向含有0.2molFeCl3、0.2molCuCl2的混合溶液中加入0.1molZn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、___________ 。
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为___________ 。
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
(1)配平写出i中反应的离子方程式:
(2)反应ii中氧化剂与还原剂的物质的量之比为
(3)向含有0.2molFeCl3、0.2molCuCl2的混合溶液中加入0.1molZn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钠( );是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
);是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为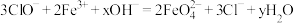 。回答下列问题:
。回答下列问题:
(1)上述反应中的y=___________ 。
(2)上述反应中氧化剂为___________ ;还原产物为___________ 。
(3)由上述反应可知,氧化性强弱:
___________ (填“>”或“<”,下同) ;还原性强弱:
;还原性强弱:
___________  。
。
(4)请用单线桥法表示该反应中电子的转移情况:___________ 。
(5)已知: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 月胶体,
月胶体, 胶体具有吸附性。
胶体具有吸附性。
① 在处理饮用水的过程中
在处理饮用水的过程中___________ (填“发生了”或“未发生”)氧化还原反应。
② 胶体为
胶体为___________ 色,写出区分胶体与溶液的操作及现象:___________ 。
 );是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
);是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为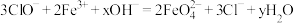 。回答下列问题:
。回答下列问题:(1)上述反应中的y=
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:

 ;还原性强弱:
;还原性强弱:
 。
。(4)请用单线桥法表示该反应中电子的转移情况:
(5)已知:
 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 月胶体,
月胶体, 胶体具有吸附性。
胶体具有吸附性。①
 在处理饮用水的过程中
在处理饮用水的过程中②
 胶体为
胶体为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氮元素形成物质的价类二维图的及氮的循环的部分信息。
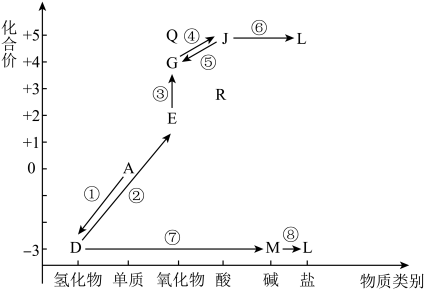
(1)①是一种人工固氮的重要途径,该反应的化学方程式是__________ 。
(2)②的化学方程式是__________ 。
(3)⑤的化学方程式是(任写一种)__________ 。
(4)R可与 NaOH溶液反应:HNO2+NaOH=NaNO2+H2O,该反应体现了R(HNO2)的_____ 性。
(5)Q的化学式是_______ ,Q属于酸性氧化物,写出Q与水反应的化学方程式________ 。
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转化为无污染气体以去除。写出L与NaClO反应的离子方程式_________ 。

(1)①是一种人工固氮的重要途径,该反应的化学方程式是
(2)②的化学方程式是
(3)⑤的化学方程式是(任写一种)
(4)R可与 NaOH溶液反应:HNO2+NaOH=NaNO2+H2O,该反应体现了R(HNO2)的
(5)Q的化学式是
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转化为无污染气体以去除。写出L与NaClO反应的离子方程式
您最近一年使用:0次
【推荐2】 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
(1)①将以上物质分别填入下面对应的横线上,并配平化学方程式:_______ 。
_______+_______+_______=_______+_______+_______
②该反应中,被氧化的元素是_______ (填元素名称);氧化剂是_______ ,氧化产物_______ 。
③反应中若产生 的还原产物,则有
的还原产物,则有_______  电子转移。
电子转移。
(2)已知常温下在溶液中可发生如下两个反应:
①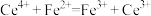
②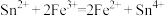
由此可以确定Fe2+、Sn2+、Ce3+三种离子的还原性由强到弱的顺序是_______ 。
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。(1)①将以上物质分别填入下面对应的横线上,并配平化学方程式:
_______+_______+_______=_______+_______+_______
②该反应中,被氧化的元素是
③反应中若产生
 的还原产物,则有
的还原产物,则有 电子转移。
电子转移。(2)已知常温下在溶液中可发生如下两个反应:
①
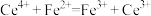
②
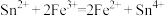
由此可以确定Fe2+、Sn2+、Ce3+三种离子的还原性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,回答下列问题:
(1)该反应中还原产物的化学式是______ ,被氧化的元素是______ (填元素符号)。
(2)用双线桥标出上述反应的电子转移情况______ 。
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为______ mol,消耗还原剂的物质的量为______ mol。
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为______ ,此过程说明ClO2具有______ (填“氧化”或“还原”)性。
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:______ 。
ClO2+ S2- H2O= Cl-+ SO H+
H+
(1)该反应中还原产物的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:
ClO2+ S2- H2O= Cl-+ SO
 H+
H+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是___ 。
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为___ 。
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)铁钉在氯气中被锈蚀为棕黄色物质FeCl3,而在盐酸中生成浅绿色的FeCl2溶液。则在Cl2、Cl-、H+中,具有氧化性的是________ (写化学式)。
(2)盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下三个反应,请按要求回答问题:
①在反应Fe+2HCl=FeCl2+H2中盐酸表现的性质为_______ ;
②写出反应Fe2O3+6HCl=2FeCl3+3H2O 的离子方程式_________ ;
③配平方程式并用单线桥表示反应的电子转移方向和数目:_________
KMnO4+ HCl= KCl+ MnCl2+ Cl2+ H2O
反应中的还原剂为_______ 被还原的元素为_________ 还原产物为________
(2)盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下三个反应,请按要求回答问题:
①在反应Fe+2HCl=FeCl2+H2中盐酸表现的性质为
②写出反应Fe2O3+6HCl=2FeCl3+3H2O 的离子方程式
③配平方程式并用单线桥表示反应的电子转移方向和数目:
KMnO4+ HCl= KCl+ MnCl2+ Cl2+ H2O
反应中的还原剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径大小关系为______ ,碳原子核外有___ 种运动状态不同的电子。
(2)氰化钠(NaCN)中,N元素显-3价,则非金属性N___________ C(填“<”、“=”或“>”),写出氰化钠的电子式_______________ 。
(3)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(a)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑,则A的化学式为___ 。
(b)NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式____________ 。
(4)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是______ ;恰好反应后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是__________ 。
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径大小关系为
(2)氰化钠(NaCN)中,N元素显-3价,则非金属性N
(3)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(a)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑,则A的化学式为
(b)NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式
(4)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某些化学反应可表示为: .请回答下列问题:
.请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式_______
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式_______
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式_______
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为_______
 .请回答下列问题:
.请回答下列问题:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将含有少量 的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
(1)写出生成漂白粉的化学方程式是_______ 。
(2)此实验所得 产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
①温度较高时氯气与消石灰反应生成了 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是_______ ;如图为反应后溶液中 、
、 离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。

a.图中曲线Ⅰ表示_______ 离子的物质的量随反应时间变化的关系。
b.所用石灰乳中含有 的物质的量为
的物质的量为_______  。
。
c.另取一份含有等物质的量 的石灰乳,以较大的速率通入足量氯气,反应后测得产物中
的石灰乳,以较大的速率通入足量氯气,反应后测得产物中 的物质的量为
的物质的量为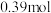 ,则产物中
,则产物中
_______ 。
②试判断另一个副反应是_______ (写出此反应的化学方程式);为避免此副反应发生,可以采取的改进措施是_______ 。
 的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:(1)写出生成漂白粉的化学方程式是
(2)此实验所得
 产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。①温度较高时氯气与消石灰反应生成了
 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是 、
、 离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
a.图中曲线Ⅰ表示
b.所用石灰乳中含有
 的物质的量为
的物质的量为 。
。c.另取一份含有等物质的量
 的石灰乳,以较大的速率通入足量氯气,反应后测得产物中
的石灰乳,以较大的速率通入足量氯气,反应后测得产物中 的物质的量为
的物质的量为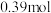 ,则产物中
,则产物中
②试判断另一个副反应是
您最近一年使用:0次

 MnSO4+Na2SO4 +Br2↑+2H2O
MnSO4+Na2SO4 +Br2↑+2H2O