铜、锌原子结构的特殊性,决定了它们的单质及其化合物在化工生产中发挥着重要的作用。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ,基态Cu2+的核外电子存在___________ 种不同空间运动状态。
(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
①[Cu(NH3)4]SO4中各非金属元素电负性由大到小的顺序为___________ ,阴离子的空间构型为___________ 。
②l mol [Cu(NH3)4]2+中含___________ mol σ键;[Cu(NH3)4]2+中NH3的键角比独立NH3的键角___________ (填“大”“小”或“相等”)。
(3)ZnF2的熔点为872°C,ZnCl2的熔点为275°C,ZnF2的熔点高于ZnCl2的原因为___________ 。
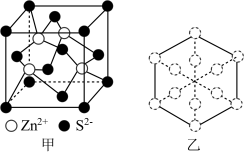
(4)立方ZnS晶体常用作半导体材料,其晶胞结构如下图甲所示,密度为d g· cm-3。
①两个S原子之间的最短距离为___________ nm(已知NA为阿伏加德罗常数的值,用含NA、d的代数式表示)。
②若ZnS晶胞沿体对角线方向投影,所得的Zn原子投影外围图形为正六边形,如下图乙所示,则S原子的投影外围图形为___________ 。
(1)基态锌原子的价电子排布式为
(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
①[Cu(NH3)4]SO4中各非金属元素电负性由大到小的顺序为
②l mol [Cu(NH3)4]2+中含
(3)ZnF2的熔点为872°C,ZnCl2的熔点为275°C,ZnF2的熔点高于ZnCl2的原因为
(4)立方ZnS晶体常用作半导体材料,其晶胞结构如下图甲所示,密度为d g· cm-3。
①两个S原子之间的最短距离为
②若ZnS晶胞沿体对角线方向投影,所得的Zn原子投影外围图形为正六边形,如下图乙所示,则S原子的投影外围图形为

更新时间:2021-10-30 17:55:32
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___________ ,3d 能级上的未成对电子数为__________ 。
(2) 硫酸镍溶于氨水形成 [ Ni(NH3 )6] SO4蓝色溶液 。
①[Ni(NH3)6]SO4中 的空间立体构型是
的空间立体构型是 _________ 。
②在[Ni(NH3)6]2+中Ni2+与 NH3之间形成的化学键称为__________ 。
③氨的沸点________ (填“高于”或“低于”)膦(PH3),原因是 _______ 。氨分子中,中心原子的轨道杂化类型为 ___________ 。
(3)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ•mol-1、INi= 1753 kJ•mol-l,ICu > INi的原因是_______ 。
(4)某镍白铜合金的立方晶胞结构如图所示。

若合金的密度为dg•cm-3,晶胞参数 a =________ nm 。
(1)镍元素基态原子的电子排布式为
(2) 硫酸镍溶于氨水形成 [ Ni(NH3 )6] SO4蓝色溶液 。
①[Ni(NH3)6]SO4中
 的空间立体构型是
的空间立体构型是 ②在[Ni(NH3)6]2+中Ni2+与 NH3之间形成的化学键称为
③氨的沸点
(3)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ•mol-1、INi= 1753 kJ•mol-l,ICu > INi的原因是
(4)某镍白铜合金的立方晶胞结构如图所示。

若合金的密度为dg•cm-3,晶胞参数 a =
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是元素周期表中原子半径最小的元素;Y元素基态原子有三个能级上有电子,且每个能级上的电子数相等;Z元素基态原子的单电子数在同周期元素基态原子中最多;W与Z同周期,第一电离能比Z的低;R与Y同主族;Q的最外层只有一个电子,其他电子层均有 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:
(1)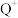 的核外电子排布式为
的核外电子排布式为______ 。
(2)化合物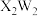 中W的杂化方式为
中W的杂化方式为______ ;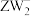 的空间结构为
的空间结构为______ 。
(3)Y、R的最高价氧化物中沸点较高的是______ (填化学式),原因是__________________ 。
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为______ ;若晶胞的边长为 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为______ (用含a和ρ的代数式表示)。
 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:(1)
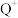 的核外电子排布式为
的核外电子排布式为(2)化合物
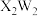 中W的杂化方式为
中W的杂化方式为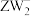 的空间结构为
的空间结构为(3)Y、R的最高价氧化物中沸点较高的是
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为
 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为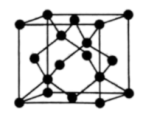
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)在第三周期元素中,S的第一电离能的大小(最小)范围为___________ <S<___________ (填元素符号)。
(2)[TiCl(H2O)5]Cl2中配位数为___________ ,0.5mol该物质中含σ键的数目为___________
(3)某基态原子核外电子有6个成单电子,该原子的电子排布式为___________
(4)Fe2+的价电子排布图为___________
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,所含元素的电负性由大到小的顺序为___________ ,阴离子空间构型为___________ ,C原子的杂化形式为___________ ,与其互为等电子体的分子为___________
(6)铜、锌两种元素的第一电离能、第二电离能如表所示
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是___________ 。
(1)在第三周期元素中,S的第一电离能的大小(最小)范围为
(2)[TiCl(H2O)5]Cl2中配位数为
(3)某基态原子核外电子有6个成单电子,该原子的电子排布式为
(4)Fe2+的价电子排布图为
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,所含元素的电负性由大到小的顺序为
(6)铜、锌两种元素的第一电离能、第二电离能如表所示
| 电离能kJ·mol-1 | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】硼、铁、镍及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)基态铁原子的外围电子排布式为__________ 。
(2)NaBH4、LiBH4常作有机合成的还原剂。LiBH4中B原子的杂化方式为________ ;BH4-的空间构型为____________ 。
(3)NiO、FeO的晶体类型相同,已知Ni2+、Fe2+的半径分别为72 pm、76 pm。熔点:FeO_____ NiO(填“>”、“<”或“=”),理由是____________ 。
(4)镍能形成多种配合物,如Ni(CO)4、[Ni(NH3)6]2+等。[Ni(NH3)6]2+中,Ni2+的配位数为_________ ;在Ni(CO)4中提供孤电子对的原子是C,不是O,可能的原因是_________ 。
(5)氧化镍晶胞如图所示,镍离子的配位数为__________ 。已知晶胞参数为a cm,NA为阿伏加 德罗常数的值,则氧化镍晶体密度为__________ g·cm-3。
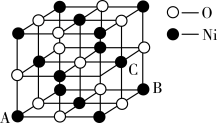
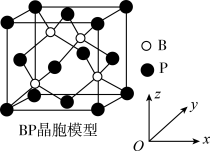
(6)磷化硼晶体结构类似金刚石,是一种耐磨材料,常作金属涂层,其晶胞如图所示。磷化硼晶胞沿z轴的平面投影图中,B原子构成的几何形状是__________ 。
(1)基态铁原子的外围电子排布式为
(2)NaBH4、LiBH4常作有机合成的还原剂。LiBH4中B原子的杂化方式为
(3)NiO、FeO的晶体类型相同,已知Ni2+、Fe2+的半径分别为72 pm、76 pm。熔点:FeO
(4)镍能形成多种配合物,如Ni(CO)4、[Ni(NH3)6]2+等。[Ni(NH3)6]2+中,Ni2+的配位数为
(5)氧化镍晶胞如图所示,镍离子的配位数为

(6)磷化硼晶体结构类似金刚石,是一种耐磨材料,常作金属涂层,其晶胞如图所示。磷化硼晶胞沿z轴的平面投影图中,B原子构成的几何形状是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳、氮、氧元素的单质或化合物在很多领域有着广泛的应用。回答下列问题:
(1) 、
、 、
、 的键角由大到小的顺序是
的键角由大到小的顺序是______ 。
(2) (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为______ 。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇( ,7.6℃)之间,原因是
,7.6℃)之间,原因是____________ 。
(4) (x=3,4,5,6)是一系列化合物,向含1mol
(x=3,4,5,6)是一系列化合物,向含1mol 的溶液中加入足量
的溶液中加入足量 溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
① 含有的化学键类型有
含有的化学键类型有______ (填标号)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.氢键
②能准确表示 结构的化学式为
结构的化学式为______ 。
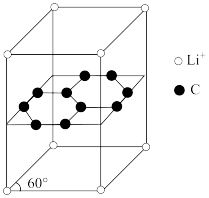
(5)锂电池负极材料晶体为 嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为
嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为______ ;其中与一个 距离最近且相等的C原子数为
距离最近且相等的C原子数为______ 。
(1)
 、
、 、
、 的键角由大到小的顺序是
的键角由大到小的顺序是(2)
 (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为(3)甲醇的沸点(64.7℃)介于水和甲硫醇(
 ,7.6℃)之间,原因是
,7.6℃)之间,原因是(4)
 (x=3,4,5,6)是一系列化合物,向含1mol
(x=3,4,5,6)是一系列化合物,向含1mol 的溶液中加入足量
的溶液中加入足量 溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。①
 含有的化学键类型有
含有的化学键类型有A.极性共价键 B.离子键 C.配位键 D.金属键 E.氢键
②能准确表示
 结构的化学式为
结构的化学式为(5)锂电池负极材料晶体为
 嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为
嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为 距离最近且相等的C原子数为
距离最近且相等的C原子数为
您最近一年使用:0次
【推荐3】以铁矿石(Fe2O3)为起始物,经过一系列反应可以得到Fe3[Fe(CN)6]2和Fe(SCN)3,请回答下列问题:
(1)写出Fe的原子结构示意图_____________ ,O原子核外电子轨道表示式为__________ 。
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为____________ 。SCN-的空间构型__________________ 。
(3)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为________________ ,该化学键能够形成的原因是______________________________ 。
(4)K3[Fe(CN)5NO]的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是_________________ ,该配合物中铁原子的配位数是________________ 。
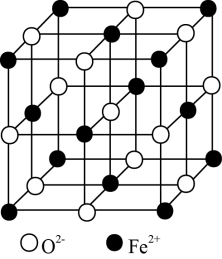
(5)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为________________ ,若该晶胞边长为a nm,则该晶体密度为_________ g·cm-3(阿伏伽德罗常数的值为NA)。
(1)写出Fe的原子结构示意图
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为
(3)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为
(4)K3[Fe(CN)5NO]的组成元素中,属于第2周期的元素的第一电离能由小到大的顺序是
(5)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】碳、氮和磷元素是几乎所有的生物体中均含有的生命元素。回答下列问题:
(1)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。
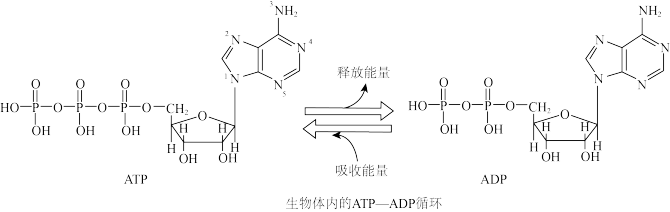
ATP分子中属于 杂化的N原子是
杂化的N原子是_______ (写序号),判断ATP生成ADP的反应类型_______ 。
(2)C可以形成多种有机物,以下四种的沸点数据如表:
 和
和 沸点相差较大,
沸点相差较大, 和
和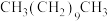 沸点相差小,原因
沸点相差小,原因_______ 。
(3)2001年德国专家从硫酸铵中检出一种组成为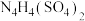 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和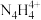 两种离子的形式存在。
两种离子的形式存在。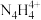 中N原子均为
中N原子均为 杂化,请推测
杂化,请推测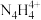 的结构式:
的结构式:_______ 。
(4)某种磁性氮化铁的晶胞结构如图所示。
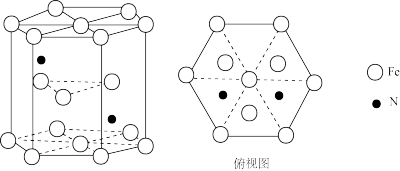
①基态Fe原子的电子排布式为_______ 。
②该化合物的化学式为_______ 。
③若晶胞底面积为 ,高为c nm,
,高为c nm, 为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为
为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为_______  (用含a、c、
(用含a、c、 的代数式表示)。
的代数式表示)。
(1)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。

ATP分子中属于
 杂化的N原子是
杂化的N原子是(2)C可以形成多种有机物,以下四种的沸点数据如表:
| 物质 |  |  |  | 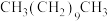 |
| 相对分子质量 | 32 | 30 | 158 | 156 |
| 沸点/℃ | 64.5 |  | 228 | 196 |
 和
和 沸点相差较大,
沸点相差较大, 和
和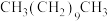 沸点相差小,原因
沸点相差小,原因(3)2001年德国专家从硫酸铵中检出一种组成为
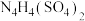 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和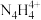 两种离子的形式存在。
两种离子的形式存在。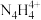 中N原子均为
中N原子均为 杂化,请推测
杂化,请推测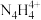 的结构式:
的结构式:(4)某种磁性氮化铁的晶胞结构如图所示。

①基态Fe原子的电子排布式为
②该化合物的化学式为
③若晶胞底面积为
 ,高为c nm,
,高为c nm, 为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为
为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为 (用含a、c、
(用含a、c、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】卤族元素是非常重要的非金属元素,其单质和化合物有广泛用途,化学性质也非常丰富。
(1)基态氯原子的价电子排布式为__________________ ,其核外电子占据的最高能层的符号是_________ 。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是___________ 。
(3)ClO2—的立体结构为_______ 形,中心氯原子的杂化轨道类型为_________ ,写出ClO2—一个等电子体的化学式 ______ 。
(4)下列分子中只存在s-p 键的是
键的是_____________ 。
A. H2 B.F2 C.HCl D.HClO
(5)CsICl2不稳定,受热时可能按下列两种方式分解,已知生成物晶格能越大反应越易发生,则CsICl2按下列______ 方式分解更合理。
A.CsICl2=CsI+Cl2 B. CsICl2=CsCl+ICl
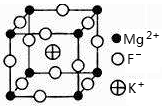
(6)由F、K、Mg三种元素形成的某离子晶体的晶胞结构如下图所示,晶胞边长为a nm(1nm=10—9m)。
①该晶体的化学式为___________________ 。
②该晶体的密度为____________ g•cm—3。(结果保留1位小数)
(1)基态氯原子的价电子排布式为
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是
(3)ClO2—的立体结构为
(4)下列分子中只存在s-p
 键的是
键的是A. H2 B.F2 C.HCl D.HClO
(5)CsICl2不稳定,受热时可能按下列两种方式分解,已知生成物晶格能越大反应越易发生,则CsICl2按下列
A.CsICl2=CsI+Cl2 B. CsICl2=CsCl+ICl
(6)由F、K、Mg三种元素形成的某离子晶体的晶胞结构如下图所示,晶胞边长为a nm(1nm=10—9m)。
①该晶体的化学式为
②该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。
请回答下列问题:
(1)化合物Cu(NH3)3(CO)Ac中,铜元素的化合价为___ 。
(2)该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序是___ 。
(3)写出基态Cu2+的电子排布式:___ ,向Cu2+的溶液中加入过量NaOH溶液,可生成Cu2+配位数为4的配位离子,写出该配位离子的结构式___ 。
(4)CO与N2互为等电子体,二者沸点较高的是___ ,理由是____ 。
(5)在一定条件下,NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子和氮原子的杂化轨道类型分别是:___ 和___ 。
(6)Cu与O形成的某种化合物的晶胞结构如图所示。
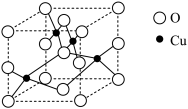
①在一个晶胞中,氧原子的数目为___ 。
②该化合物的化学式为____ 。
③晶胞的边长为apm,则该晶胞的密度为_____ g•cm-3。
请回答下列问题:
(1)化合物Cu(NH3)3(CO)Ac中,铜元素的化合价为
(2)该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序是
(3)写出基态Cu2+的电子排布式:
(4)CO与N2互为等电子体,二者沸点较高的是
(5)在一定条件下,NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子和氮原子的杂化轨道类型分别是:
(6)Cu与O形成的某种化合物的晶胞结构如图所示。

①在一个晶胞中,氧原子的数目为
②该化合物的化学式为
③晶胞的边长为apm,则该晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】荧光材料硫化锌(ZnS)的研究至今已有 150 多年的历史,可用于制白色颜料、发光粉、发光油漆等,其久置于湿空气中易被氧化为 ZnSO4。请回答下列问题:
(1)基态 Zn 原子的电子排布式为_________________________ ,核外电子占据最高能层的符号是__________________________ , 占据该能层电子的电子云轮廓图形状为__________________________ 。
(2)ZnSO4中三种元素的电负性由大到小的顺序为__________________________ , 的立体构型为
的立体构型为__________________________ ,其中 S 的杂化轨道类型为__________________________ 。
(3)ZnSO4溶于氨水可生成[Zn(NH3)4]SO4溶液,[Zn(NH3)4]SO4溶液中不存在的微粒间作用力有__________________________ 。
A.离子键B.共价键C.配位键D.范德华力
(4)根据下列锌卤化物的熔点和溶解性,判断 ZnF2晶体的类型为______ ;分析 ZnCl2、ZnBr2、ZnI2熔点依次增大的原因__________________________ 。
(5) 立方 ZnS 晶体的密度为 ρ g/cm3,其晶胞结构如图。
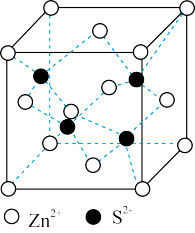
S2-周围等距离且最近的 Zn2+为__________________________ ;ZnS晶胞中的晶胞参数 a=__________________________ nm(列出计算式)。[ M(ZnS)=97 g/mol ]
(1)基态 Zn 原子的电子排布式为
(2)ZnSO4中三种元素的电负性由大到小的顺序为
 的立体构型为
的立体构型为(3)ZnSO4溶于氨水可生成[Zn(NH3)4]SO4溶液,[Zn(NH3)4]SO4溶液中不存在的微粒间作用力有
A.离子键B.共价键C.配位键D.范德华力
(4)根据下列锌卤化物的熔点和溶解性,判断 ZnF2晶体的类型为
| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
| 熔点/℃ | 872 | 275 | 394 | 446 |
| 在乙醇、乙醚中的溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
(5) 立方 ZnS 晶体的密度为 ρ g/cm3,其晶胞结构如图。

S2-周围等距离且最近的 Zn2+为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知X、Y、Z、M、N是原子序数依次增大的前四周期元素,其中Y是地壳中含量第二的元素,X、Y、Z是核外未成对电子数均为2的非金属元素,ZX3的空间结构为平面三角形,M的价层电子数为6,N与Z同族。请回答下列问题:
(1)X为____ (填元素名称,下同),Y为____ ,Z为____ 。
(2)M在元素周期表的位置是____ ,基态N原子的价层电子排布式为____ 。
(3)X、Y、Z的第一电离能由大到小的顺序为____ (填元素符号)。
(4)Z与N的最简单氢化物的稳定性比较:____ (写化学式),原因为____ 。
(5)YX2的晶体类型为____ ,其熔点____ (填“高于”或“低于”)NX2。
(1)X为
(2)M在元素周期表的位置是
(3)X、Y、Z的第一电离能由大到小的顺序为
(4)Z与N的最简单氢化物的稳定性比较:
(5)YX2的晶体类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途。
(1)Be基态原子的轨道表示式为_________________________ ;
镁和铝的第二电离能:I2(Mg)_____ I2(Al) (填“>”“ <”或“=”)。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (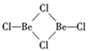 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
①在二聚体Be2Cl4中Be的杂化方式为___________ ,1mol Be2Cl4中含有_________ mol 配位键。
②MgCl2的熔、沸点比BeCl2高的原因是____________________ 。
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)____ S(BaF2) (填“>” “<””或“=”)。
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________ (填化学式),写出CN22-的电子式___________ 。
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数_______________ 。
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________ 。已知该晶胞参数a pm.则该晶体的密度为_________ g·cm-3(用a和NA表示)。
(1)Be基态原子的轨道表示式为
镁和铝的第二电离能:I2(Mg)
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (
 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。①在二聚体Be2Cl4中Be的杂化方式为
②MgCl2的熔、沸点比BeCl2高的原因是
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为

您最近一年使用:0次



