二甲醚是一种十分重要的化工原料,可用来制杀虫剂、抛光剂、防锈剂、烷基化剂、溶剂等,工业上利用“一步法”合成二甲醚的总反应为2CO(g)+4H2(g)  CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:
CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:
(1)600 °C时,在复合催化剂CuO/ZnO/Al2O3上合成二甲醚的过程如下:
ⅰ.合成气合成甲醇:CO(g) +2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
ⅱ.甲醇脱水生成二甲醚:2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1
CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1
ⅲ.水煤气变换反应:CO(g)+H2O(g) CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1
CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1
①ΔH1=___________ kJ·mol-1。
②传统合成法将反应i、ii分别在不同的反应器中进行,“一步法”连续发生以上i、ii、iii三步反应,“一步法”的优点是___________ 。
(2)实验室模拟上述“一步法”合成过程,在1 L容器中充入6 molCO和6 mol H2,t h后达到平衡,测得混合体系中各组分浓度如下表:
平衡后,整个过程中CO的转化率为___________ ,第ii步反应放出的热量为___________ kJ(保留一位小数),v(CH3OCH3)=___________ mol· L-1·h-1,第ii步反应的K=___________ (保留两位小数)。
(3)第iii步反应机理中,调控反应条件,CO和OH在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理的两种不同途径如图所示。

分析图象可知,以上过程为___________ ( 填“放热”或“吸热”)过程,从第一步来看,___________ (填“氧化还原机理”或“羧基机理”)对合成有利,最终选择另一反应机理途径更有利的原因是___________ 。
 CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:
CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:(1)600 °C时,在复合催化剂CuO/ZnO/Al2O3上合成二甲醚的过程如下:
ⅰ.合成气合成甲醇:CO(g) +2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1ⅱ.甲醇脱水生成二甲醚:2CH3OH(g)
 CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1
CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1ⅲ.水煤气变换反应:CO(g)+H2O(g)
 CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1
CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1①ΔH1=
②传统合成法将反应i、ii分别在不同的反应器中进行,“一步法”连续发生以上i、ii、iii三步反应,“一步法”的优点是
(2)实验室模拟上述“一步法”合成过程,在1 L容器中充入6 molCO和6 mol H2,t h后达到平衡,测得混合体系中各组分浓度如下表:
| 物质 | H2 | CH3OH | H2O | CO2 |
| 物质的量浓度/(mol· L-1) | 1.956 | 0.72 | 0.084 | 0.756 |
平衡后,整个过程中CO的转化率为
(3)第iii步反应机理中,调控反应条件,CO和OH在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理的两种不同途径如图所示。

分析图象可知,以上过程为
更新时间:2021-10-30 17:55:32
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,如图所示。
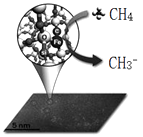
(1)已知相关物质的燃烧热如上表,写出甲烷制备乙烯的热化学方程式__________________________________________________________________ 。
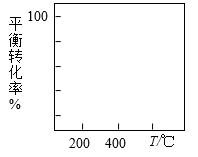
(2)在400℃时,向1L的恒容反应器中充入1mol CH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0 %。则在该温度下,其平衡常数K=__________________ 。按化学平衡移动原理,在图中画出该反应的平衡转化率与温度及压强(p1>p2)的关系曲线。_________
(3)工业上常采用除杂效率高的吸收-电解联合法,除去天然气中杂质气体H2S,并转化为可回收利用的单质硫,其装置如下图所示。
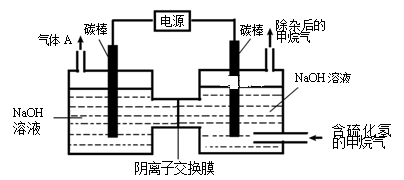
通电前,先通入一段时间含H2S的甲烷气,使部分NaOH吸收H2S转化为Na2S,再接通电源,继续通入含杂质的甲烷气,并控制好通气速率。则装置中右端碳棒为_____ 极,左端碳棒上的电级反应为________________ ,右池中的c(NaOH):c(Na2S)___________ (填“增大”、“ 基本不变”或“减小)。
(4)已知:HCN的电离常数Ka=4.9×10-10,H2S的电离常数Ka1=1.3×10−7,Ka2=7.0×10−15,向NaCN溶液中通入少量的H2S气体,反应的化学方程式为__________________________________________________________________ 。
(5)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.0020 mol·L−1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=_________________________________________ 。[已知:Ksp(MnS)=1.4×10−15]
| 物质 | 燃烧热(kJ/mol) |
| 氢气 | 285.8 |
| 甲烷 | 890.3 |
| 乙烯 | 1411.5 |

(1)已知相关物质的燃烧热如上表,写出甲烷制备乙烯的热化学方程式
(2)在400℃时,向1L的恒容反应器中充入1mol CH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0 %。则在该温度下,其平衡常数K=

(3)工业上常采用除杂效率高的吸收-电解联合法,除去天然气中杂质气体H2S,并转化为可回收利用的单质硫,其装置如下图所示。

通电前,先通入一段时间含H2S的甲烷气,使部分NaOH吸收H2S转化为Na2S,再接通电源,继续通入含杂质的甲烷气,并控制好通气速率。则装置中右端碳棒为
(4)已知:HCN的电离常数Ka=4.9×10-10,H2S的电离常数Ka1=1.3×10−7,Ka2=7.0×10−15,向NaCN溶液中通入少量的H2S气体,反应的化学方程式为
(5)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.0020 mol·L−1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】汽车尾气中NO和CO的催化转化是目前化学研究热点。回答下列问题:
(1)已知下列反应的热化学方程式:
①
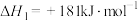

②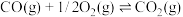


则反应 的
的
___________  ,平衡常数
,平衡常数
___________ (用 、
、 表示)。
表示)。
(2) 与
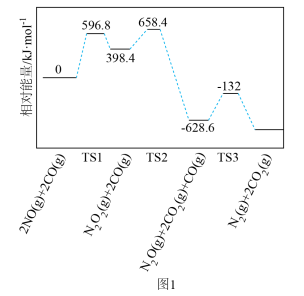
与 的反应机理及体系的相对能量变化如图1所示(TS表示过渡态)。该反应有
的反应机理及体系的相对能量变化如图1所示(TS表示过渡态)。该反应有___________ 个分步反应,写出最易发生的分步反应的化学方程式___________ 。
(3)当起始物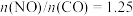 时,不同条件下达到平衡,设
时,不同条件下达到平衡,设 的转化率为
的转化率为 ,在
,在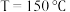 下
下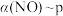 、
、 下
下 的关系如图2所示。
的关系如图2所示。
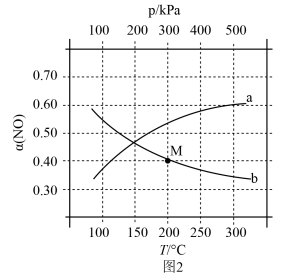
①图2中对应等温过程的曲线是___________ ,判断理由为___________ 。
②M点 的分压为
的分压为___________ kPa,该温度下此反应的分压平衡常数
___________  。
。
(1)已知下列反应的热化学方程式:
①

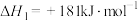

②
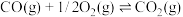


则反应
 的
的
 ,平衡常数
,平衡常数
 、
、 表示)。
表示)。(2)
 与
与 的反应机理及体系的相对能量变化如图1所示(TS表示过渡态)。该反应有
的反应机理及体系的相对能量变化如图1所示(TS表示过渡态)。该反应有
(3)当起始物
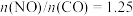 时,不同条件下达到平衡,设
时,不同条件下达到平衡,设 的转化率为
的转化率为 ,在
,在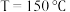 下
下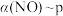 、
、 下
下 的关系如图2所示。
的关系如图2所示。
①图2中对应等温过程的曲线是
②M点
 的分压为
的分压为
 。
。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一。SCR法是工业上消除氮氧化物的常用方法,反应原理为:4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) △H<0。
(1)氮氧化物破坏臭氧层原理为:①NO+O3⇌NO2+O2②NO2+O⇌NO+O2常温下反应①的平衡常数为K1,反应热为△H1,反应②的平衡常数为K2,反应热为△H2 ,则反应O3+O⇌2O2的平衡常数K =_____ (用K1、K2表示),反应热△H =______ (用△H1、△H2表示)。氮氧化物在该反应中的作用是______ 。
(2)SCR法除NO时,投料比一定时有利于提高NO平衡转化率的反应条件是_______ 、_________ 。该法可能发生副反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),减少副反应的主要措施是_________ 。
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
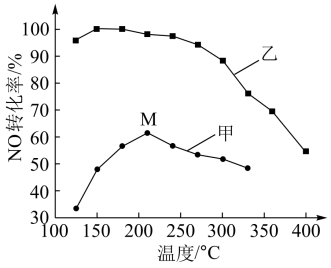
①工业上选择催化剂乙的原因是_____ ;
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______ (填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是______ 。
(1)氮氧化物破坏臭氧层原理为:①NO+O3⇌NO2+O2②NO2+O⇌NO+O2常温下反应①的平衡常数为K1,反应热为△H1,反应②的平衡常数为K2,反应热为△H2 ,则反应O3+O⇌2O2的平衡常数K =
(2)SCR法除NO时,投料比一定时有利于提高NO平衡转化率的反应条件是
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。

①工业上选择催化剂乙的原因是
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是________ 。氯碱工业生产时,由于食盐水中通常含有少量NH4Cl,而在阳极区与生成的氯气反应产生少量NCl3,该反应的化学方程式为__________ 。
(2)一定条件下,不同物质的量的CO2与不同体积的1.0 mol/L NaOH溶液充分反应放出的热量如下表所示:
该条件CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为________________ 。
(3)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g)+2CO(g) N2(g)+2CO2(g),向容积均为1 L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00 mol NO和2.00 mol CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g)+2CO2(g),向容积均为1 L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00 mol NO和2.00 mol CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
①甲容器中,0~40min 内用NO的浓度变化表示的反应速率v(NO)=_____________ 。
②该反应的△H____ 0(填“>”或“<”)。
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡_________ (填“正向”、“逆向”或“不”)移动。
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是
(2)一定条件下,不同物质的量的CO2与不同体积的1.0 mol/L NaOH溶液充分反应放出的热量如下表所示:
| 反应序号 | n(CO2)/mol | V (NaOH) /L | 放出的热量/kJ |
| 1 | 0.5 | 0.75 | a |
| 2 | 1.0 | 2.00 | b |
该条件CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为
(3)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g)+2CO(g)
 N2(g)+2CO2(g),向容积均为1 L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00 mol NO和2.00 mol CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g)+2CO2(g),向容积均为1 L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00 mol NO和2.00 mol CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①甲容器中,0~40min 内用NO的浓度变化表示的反应速率v(NO)=
②该反应的△H
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
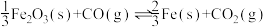
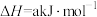
I、已知:①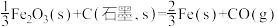
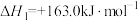
②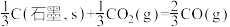
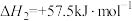
(1)
______
II、该反应在不同温度下的平衡常数如下。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、 、CO和
、CO和 各1.0mol,此时
各1.0mol,此时
______  (填>、<或=);反应经过10min后达到平衡,该时间范围内反应的平均反应速率
(填>、<或=);反应经过10min后达到平衡,该时间范围内反应的平均反应速率
______ 。
(3)下列叙述中能表示该反应达到平衡状态的是_____
(4)欲提高高炉中CO的平衡转化率,可采取的措施是_____
III、已知化学反应:
①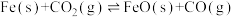

②

③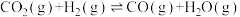
三个反应的平衡常数分别为K1、K2和K3。
(5)
______ 0(填“>”或“<”)。
(6)根据反应 ①和反应 ②可推导出K1、K2和K3的关系式:______ 。
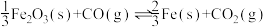
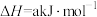
I、已知:①
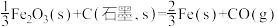
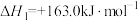
②
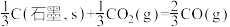
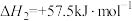
(1)

II、该反应在不同温度下的平衡常数如下。
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
 、CO和
、CO和 各1.0mol,此时
各1.0mol,此时
 (填>、<或=);反应经过10min后达到平衡,该时间范围内反应的平均反应速率
(填>、<或=);反应经过10min后达到平衡,该时间范围内反应的平均反应速率
(3)下列叙述中能表示该反应达到平衡状态的是_____
A.单位时间内消耗nmolCO的同时生成nmol | B.容器中气体压强不再变化 |
| C.容器中气体物质的量不再变化 | D.混合气体的密度不再变化 |
| A.减少Fe的量 | B.增加 的量 的量 | C.移出部分 | D.加入合适的催化剂 |
III、已知化学反应:
①
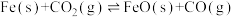

②


③
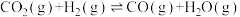
三个反应的平衡常数分别为K1、K2和K3。
(5)

(6)根据反应 ①和反应 ②可推导出K1、K2和K3的关系式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】甲醇制氢作为一种绿色能源技术备受关注。
I.甲醇裂解制氢法
(1)该方法的主反应:CH3OH(g) CO(g)+2H2(g) △H1>0此反应能自发进行的原因是
CO(g)+2H2(g) △H1>0此反应能自发进行的原因是___ 。
(2)一定温度下,向某一刚性恒容密闭容器中充入CH3OH(g),发生反应CH3OH(g) CO(g)+2H2(g),反应起始时CH3OH(g)的压强为5.00MPa,t h后反应达到平衡,此时H2的物质的量分数为60%,则0~t h内的平均反应速率v(CO)=
CO(g)+2H2(g),反应起始时CH3OH(g)的压强为5.00MPa,t h后反应达到平衡,此时H2的物质的量分数为60%,则0~t h内的平均反应速率v(CO)=___ MPa•h-1,CH3OH的平衡转化率α(CH3OH)=___ ,此时平衡常数Kp=___ (Kp为以平衡分压表示的平衡常数)。
(3)科研人员通过计算机模拟用Pd(III)催化甲醇裂解的反应机理,得到附着在Pd(III)表面上甲醇变换的反应历程图[如图1,附在Pd(III)表面的物种用*标注],此历程中活化能最小的反应方程式为___ 。

II.甲醇水蒸气重整制氢法
(4)该方法的部分反应如下:
主反应:CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H2=+49kJ•mol-1
CO2(g)+3H2(g) △H2=+49kJ•mol-1
副反应:H2(g)+CO2(g) CO(g)+H2O(g) △H3=-41kJ·mol-1
CO(g)+H2O(g) △H3=-41kJ·mol-1
①相同条件下,甲醇水蒸气重整制氢法与甲醇裂解制氢法相比较,从经济效益和绿色化学角度分析,前者先进之处在于___ 。
②在某催化剂的作用下,在相同时间内,不同温度下测得CH3OH的转化率、CO的生成率与温度的变化关系如图2所示。
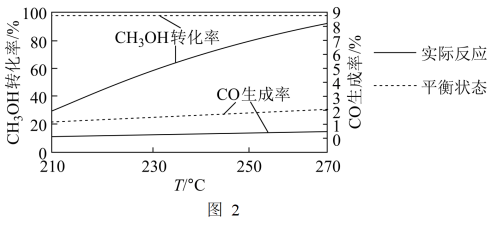
随着温度的升高,CH3OH实际反应转化率不断接近平衡状态转化率的原因是___ (填字母)。
A.主反应的活化能降低
B.主反应的反应速率增大
C.CH3OH的平衡转化率降低
随着温度的升高,CO的实际反应生成率没有不断接近平衡状态生成率的原因是___ 。为提高CH3OH的转化率且使副反应不向正反应方向进行,可采取的措施有___ (任写一条)。
I.甲醇裂解制氢法
(1)该方法的主反应:CH3OH(g)
 CO(g)+2H2(g) △H1>0此反应能自发进行的原因是
CO(g)+2H2(g) △H1>0此反应能自发进行的原因是(2)一定温度下,向某一刚性恒容密闭容器中充入CH3OH(g),发生反应CH3OH(g)
 CO(g)+2H2(g),反应起始时CH3OH(g)的压强为5.00MPa,t h后反应达到平衡,此时H2的物质的量分数为60%,则0~t h内的平均反应速率v(CO)=
CO(g)+2H2(g),反应起始时CH3OH(g)的压强为5.00MPa,t h后反应达到平衡,此时H2的物质的量分数为60%,则0~t h内的平均反应速率v(CO)=(3)科研人员通过计算机模拟用Pd(III)催化甲醇裂解的反应机理,得到附着在Pd(III)表面上甲醇变换的反应历程图[如图1,附在Pd(III)表面的物种用*标注],此历程中活化能最小的反应方程式为

II.甲醇水蒸气重整制氢法
(4)该方法的部分反应如下:
主反应:CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H2=+49kJ•mol-1
CO2(g)+3H2(g) △H2=+49kJ•mol-1副反应:H2(g)+CO2(g)
 CO(g)+H2O(g) △H3=-41kJ·mol-1
CO(g)+H2O(g) △H3=-41kJ·mol-1①相同条件下,甲醇水蒸气重整制氢法与甲醇裂解制氢法相比较,从经济效益和绿色化学角度分析,前者先进之处在于
②在某催化剂的作用下,在相同时间内,不同温度下测得CH3OH的转化率、CO的生成率与温度的变化关系如图2所示。

随着温度的升高,CH3OH实际反应转化率不断接近平衡状态转化率的原因是
A.主反应的活化能降低
B.主反应的反应速率增大
C.CH3OH的平衡转化率降低
随着温度的升高,CO的实际反应生成率没有不断接近平衡状态生成率的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】作为一种绿色消毒剂,H2O2在公共卫生事业中发挥了重要的作用。已知反应:H2O2(l)=H2O(1)+ O2(g) △H=-98kJ·mol-1,K=2.88×1020,回答问题:
O2(g) △H=-98kJ·mol-1,K=2.88×1020,回答问题:
(1)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是___________ 。
(2)纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+ O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上___________ (填“放出”或“吸收”)热量___________ 98kJ(填“大于”、“小于”或“等于”)。
(3)纯H2O2相对稳定,实验表明在54℃下恒温贮存2周,浓度仍能保持99%,原因是H2O2分解反应的___________ (填编号)。
a.ΔH比较小 b.K不够大 c.速率比较小 d.活化能比较大
(4)向H2O2稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起___________ 作用。某组实验数据如下:
0—30minH2O2反应的平均速率v=___________ mol·L·min-1。
(5)H2O2的一种衍生物K2S2O8,阴离子结构式为(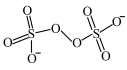 ),其中性溶液加热至沸后,溶液pH降低,用离子方程式表明原因:
),其中性溶液加热至沸后,溶液pH降低,用离子方程式表明原因:___________ 。
(6)我国科学家发明了制取H2O2的绿色方法,原理如图所示(已知:H2O2 H++HO
H++HO ,Y膜为HO
,Y膜为HO 选择性交换膜)。
选择性交换膜)。
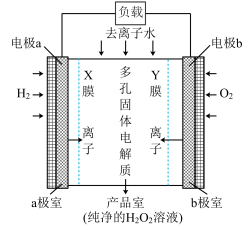
①X膜为选择性___________ 离子交换膜(填“阳”或“阴”)。
②b极上的电极反应为___________ 。
 O2(g) △H=-98kJ·mol-1,K=2.88×1020,回答问题:
O2(g) △H=-98kJ·mol-1,K=2.88×1020,回答问题:(1)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(2)纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+
 O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上(3)纯H2O2相对稳定,实验表明在54℃下恒温贮存2周,浓度仍能保持99%,原因是H2O2分解反应的
a.ΔH比较小 b.K不够大 c.速率比较小 d.活化能比较大
(4)向H2O2稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(H2O2)/mol·L-1 | 0.70 | 0.49 | 0.35 | 0.25 | 0.17 | 0.12 |
0—30minH2O2反应的平均速率v=
(5)H2O2的一种衍生物K2S2O8,阴离子结构式为(
 ),其中性溶液加热至沸后,溶液pH降低,用离子方程式表明原因:
),其中性溶液加热至沸后,溶液pH降低,用离子方程式表明原因:(6)我国科学家发明了制取H2O2的绿色方法,原理如图所示(已知:H2O2
 H++HO
H++HO ,Y膜为HO
,Y膜为HO 选择性交换膜)。
选择性交换膜)。
①X膜为选择性
②b极上的电极反应为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】 的资源化利用能有效减少
的资源化利用能有效减少 排放,对碳循环经济技术的发展具有重要意义。
排放,对碳循环经济技术的发展具有重要意义。
Ⅰ.利用 和
和 制备合成气
制备合成气 ,反应分两步进行:
,反应分两步进行:
反应①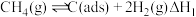
反应②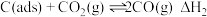
有关物质的相对能量与反应历程的变化如图a所示[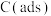 为吸附性活性炭]:
为吸附性活性炭]:
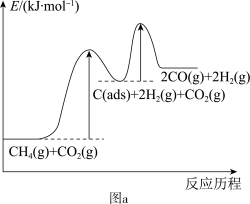
(1)总反应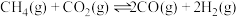 能自发进行的条件为
能自发进行的条件为_______ 。
(2)研究表明,总反应速率由反应①决定,请结合图a与碰撞理论说明原因:_______ 。
Ⅱ.工业上可利用 生产燃料甲醇。该过程发生下列反应:
生产燃料甲醇。该过程发生下列反应:
反应③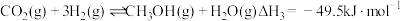
反应④
在 的恒压反应器中,按照
的恒压反应器中,按照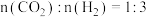 投料,测得体系中平衡时
投料,测得体系中平衡时 和
和 的选择性[
的选择性[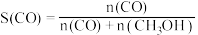 ,
, ]及
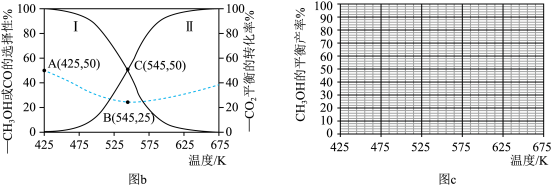
]及 的平衡转化率随温度的变化如图b所示。
的平衡转化率随温度的变化如图b所示。
(3)研究表明,原料气中掺入适量 能提高
能提高 的产率,说明其可能的原因:
的产率,说明其可能的原因:_______ 。
(4)下列说法正确的是_______。
(5)反应④在545K时的平衡常数
_______ 。
(6)结合图 b ,在图c中画出 的平衡产率随温度的变化曲线(标出B点坐标)
的平衡产率随温度的变化曲线(标出B点坐标)_______ 。
 的资源化利用能有效减少
的资源化利用能有效减少 排放,对碳循环经济技术的发展具有重要意义。
排放,对碳循环经济技术的发展具有重要意义。Ⅰ.利用
 和
和 制备合成气
制备合成气 ,反应分两步进行:
,反应分两步进行:反应①
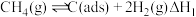
反应②
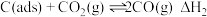
有关物质的相对能量与反应历程的变化如图a所示[
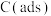 为吸附性活性炭]:
为吸附性活性炭]:
(1)总反应
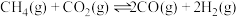 能自发进行的条件为
能自发进行的条件为(2)研究表明,总反应速率由反应①决定,请结合图a与碰撞理论说明原因:
Ⅱ.工业上可利用
 生产燃料甲醇。该过程发生下列反应:
生产燃料甲醇。该过程发生下列反应:反应③
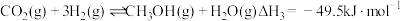
反应④

在
 的恒压反应器中,按照
的恒压反应器中,按照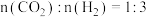 投料,测得体系中平衡时
投料,测得体系中平衡时 和
和 的选择性[
的选择性[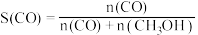 ,
, ]及
]及 的平衡转化率随温度的变化如图b所示。
的平衡转化率随温度的变化如图b所示。
(3)研究表明,原料气中掺入适量
 能提高
能提高 的产率,说明其可能的原因:
的产率,说明其可能的原因:(4)下列说法正确的是_______。
A.曲线Ⅰ代表 随温度变化 随温度变化 |
B.温度越低,越有利于工业生产 |
C.上述反应条件下, 的平衡转化率始终高于 的平衡转化率始终高于 的平衡转化率 的平衡转化率 |
D.其他条件不变,增大压强能同时提高 的平衡转化率和 的平衡转化率和 的平衡产率 的平衡产率 |

(6)
 的平衡产率随温度的变化曲线(标出B点坐标)
的平衡产率随温度的变化曲线(标出B点坐标)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】汽车在给人们带来出行方便的同时,也带来了环境污染。对机动车尾气进行无害化处理成为了科技工作者的重要课题。回答下列问题:
(1)汽车尾气中含 水蒸气等,目前汽车出厂均装有尾气净化装置,使
水蒸气等,目前汽车出厂均装有尾气净化装置,使 转化为无毒气体:
转化为无毒气体:
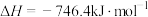 ,该反应在
,该反应在_____ (填“温度较高”“温度较低”或“任何温度”)下能自发进行。
(2)利用 的还原性可以使
的还原性可以使 转化为无毒气体:
转化为无毒气体:
 。
。
①已知:
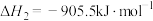 ,
,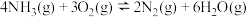
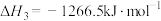 ,则
,则
_______  。
。
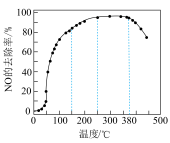
②在装有催化剂的反应体系中,匀速通入一定配比的 混合气体,相同时间内测得NO的去除率与温度的关系如图所示,随温度升高,NO的去除率先增大后减小,减小的原因可能是
混合气体,相同时间内测得NO的去除率与温度的关系如图所示,随温度升高,NO的去除率先增大后减小,减小的原因可能是________ 。
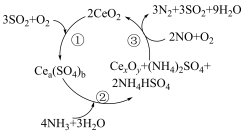
(3)过渡元素的化合物往往可以制作工业生产的催化剂,一种含CeO2的催化剂可使NO转化为无毒气体,其转化机理如图所示,该反应机理总反应的化学方程式是:___________ ;反应机理图的反应③中Ce的化合价_______ (填“升高”“降低”或“不变”)。
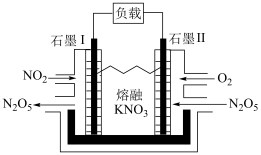
(4)汽车尾气中未被处理的NO在空气中转化为NO2.利用NO2可制作燃料电池,转化为易于收集的N2O5,其工作原理如图所示,该燃料电池中 移向
移向______ (填“正极”或“负极”),负极的电极反应式为________ 。
(1)汽车尾气中含
 水蒸气等,目前汽车出厂均装有尾气净化装置,使
水蒸气等,目前汽车出厂均装有尾气净化装置,使 转化为无毒气体:
转化为无毒气体:
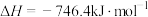 ,该反应在
,该反应在(2)利用
 的还原性可以使
的还原性可以使 转化为无毒气体:
转化为无毒气体:
 。
。①已知:

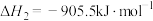 ,
,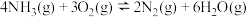
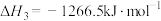 ,则
,则
 。
。②在装有催化剂的反应体系中,匀速通入一定配比的
 混合气体,相同时间内测得NO的去除率与温度的关系如图所示,随温度升高,NO的去除率先增大后减小,减小的原因可能是
混合气体,相同时间内测得NO的去除率与温度的关系如图所示,随温度升高,NO的去除率先增大后减小,减小的原因可能是
(3)过渡元素的化合物往往可以制作工业生产的催化剂,一种含CeO2的催化剂可使NO转化为无毒气体,其转化机理如图所示,该反应机理总反应的化学方程式是:

(4)汽车尾气中未被处理的NO在空气中转化为NO2.利用NO2可制作燃料电池,转化为易于收集的N2O5,其工作原理如图所示,该燃料电池中
 移向
移向
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)对于反应:2NO(g)+O2(g) 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:
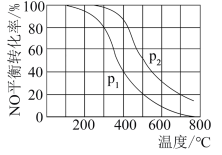
①比较p1、p2的大小关系:________ 。
②随温度升高,该反应平衡常数变化的趋势是________ (“增大”或“减小”)。
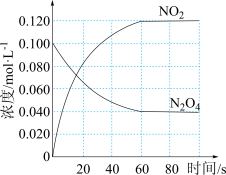
(2)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
①反应的ΔH______ 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为__________________ ;平衡时混合气体中NO2的体积分数为_______ 。
②100℃时达平衡后,向容器中迅速充入含0.08mol的NO2和0.08mol N2O4的混合气体,此时速率关系v(正)____ v(逆)。(填“大于”,“等于”,或“小于”)
③100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。
a.T________ 100℃(填“大于”或“小于”),判断理由是____________________
b.列式计算温度T时反应的平衡常数K2(写计算过程):______
 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:

①比较p1、p2的大小关系:
②随温度升高,该反应平衡常数变化的趋势是
(2)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)
 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:①反应的ΔH
②100℃时达平衡后,向容器中迅速充入含0.08mol的NO2和0.08mol N2O4的混合气体,此时速率关系v(正)
③100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。
a.T
b.列式计算温度T时反应的平衡常数K2(写计算过程):
您最近一年使用:0次
【推荐2】我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳
中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。异丁烯[CH2=C(CH3)2]作为汽油添加剂的主要成分,可利用异丁烷与CO2反应来制备。
反应I:CH3CH(CH3)CH3(g)+CO2(g) CH2=C(CH3)2(g)+H2O(g)+CO(g) △H1=+165.2kJ·mol-1
CH2=C(CH3)2(g)+H2O(g)+CO(g) △H1=+165.2kJ·mol-1
反应II:CH3CH(CH3)CH3(g) CH2=C(CH3)2(g)+H2(g) △H2
CH2=C(CH3)2(g)+H2(g) △H2
回答下列问题:
(1)已知:CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ·mol-1,则△H2=
CO2(g)+H2(g) △H=-41.2kJ·mol-1,则△H2=_______ 。
(2)向1.0L恒容密闭容器中加入1molCH3CH(CH3)CH3(g)和1molCO2(g),利用反应I制备异丁烯。已知正反应速率可表示为v正=k正c[CH3CH(CH3)CH3]·c(CO2),逆反应速率可表示为,v逆=k逆c[CH2=c(CH3)2]·c(H2O)·c(CO),其中k正、K逆为速率常数。
①图中能够代表k逆的曲线为_______ (填“L1”“L2”“L3”或“L4”)。
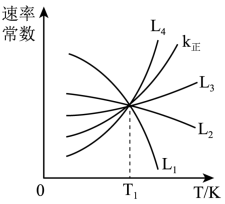
②温度为T1时,该反应的化学平衡常数K=_______ ,平衡时,CH3CH(CH3)CH3的转化率_______ 50%(填“以>”、“=”、“<”)。
(3)CH4-CO2重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g) 2CO(g)+2H2(g)。在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
2CO(g)+2H2(g)。在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
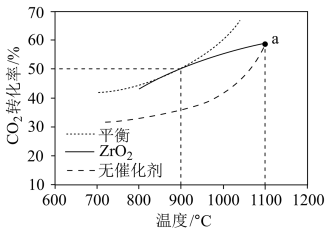
①a点CO2转化率相等的原因是_______ 。
②在pMPa、900°C、ZrO2催化条件下,将CO2、CH4、H2O按物质的量之比为1:1:n充入密闭容器,CO2的平衡转化率为α,此时平衡常数Kp=_______ (以分压表示,分压=总压×物质的量分数;写出含α、n、p的计算表达式)。
(4)利用电化学可以将CO2有效转化为HCOO-,装置如图所示。

①在该装置中,左侧Pt电极上的电极反应式:_______ 。
②装置工作时,阴极除有HCOO-生成外,还可能生成副产物降低电解效率。阴极生成的副产物可能是_______ ,标准状况下,当阳极生成O2的体积为224mL时,测得阴极区内的c(HCOO-)=0.015mol/L,则电解效率_______ 。(忽略电解前后溶液体积的变化)已知:电解效率=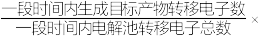 100%。
100%。
中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。异丁烯[CH2=C(CH3)2]作为汽油添加剂的主要成分,可利用异丁烷与CO2反应来制备。
反应I:CH3CH(CH3)CH3(g)+CO2(g)
 CH2=C(CH3)2(g)+H2O(g)+CO(g) △H1=+165.2kJ·mol-1
CH2=C(CH3)2(g)+H2O(g)+CO(g) △H1=+165.2kJ·mol-1反应II:CH3CH(CH3)CH3(g)
 CH2=C(CH3)2(g)+H2(g) △H2
CH2=C(CH3)2(g)+H2(g) △H2回答下列问题:
(1)已知:CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41.2kJ·mol-1,则△H2=
CO2(g)+H2(g) △H=-41.2kJ·mol-1,则△H2=(2)向1.0L恒容密闭容器中加入1molCH3CH(CH3)CH3(g)和1molCO2(g),利用反应I制备异丁烯。已知正反应速率可表示为v正=k正c[CH3CH(CH3)CH3]·c(CO2),逆反应速率可表示为,v逆=k逆c[CH2=c(CH3)2]·c(H2O)·c(CO),其中k正、K逆为速率常数。
①图中能够代表k逆的曲线为

②温度为T1时,该反应的化学平衡常数K=
(3)CH4-CO2重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g)
 2CO(g)+2H2(g)。在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
2CO(g)+2H2(g)。在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
①a点CO2转化率相等的原因是
②在pMPa、900°C、ZrO2催化条件下,将CO2、CH4、H2O按物质的量之比为1:1:n充入密闭容器,CO2的平衡转化率为α,此时平衡常数Kp=
(4)利用电化学可以将CO2有效转化为HCOO-,装置如图所示。

①在该装置中,左侧Pt电极上的电极反应式:
②装置工作时,阴极除有HCOO-生成外,还可能生成副产物降低电解效率。阴极生成的副产物可能是
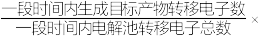 100%。
100%。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】氙及其化合物在工业生产中有重要用途。
(1)1962年,化学家巴特利特合成了氙的第一个化合物 ,其在熔化时电离出
,其在熔化时电离出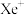 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为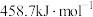 。
。
②Xe的第一电离能为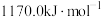 。
。
③
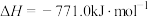 。
。
根据以上信息,计算反应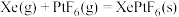

___________  。
。
(2)不久,在三个不同实验室里又分别合成了 、
、 、
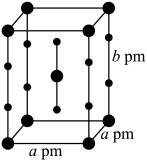
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为___________ ,中心原子的价层电子对数为___________ ,晶体密度为___________  。
。 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
已知:分压=总压×该组分物质的量分数;
对于反应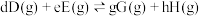
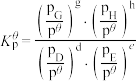
其中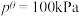 ,
,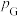 、
、 、
、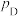 、
、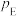 为各组分的平衡分压。
为各组分的平衡分压。
①
___________ 0(填“>”或“<”)。为提高平衡混合物中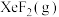 的含量,应
的含量,应___________ 投料比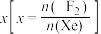 (填“增大”或“减小”)。
(填“增大”或“减小”)。
②673K时充入23.77molXe和 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:
则 平衡转化率
平衡转化率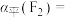
___________ (保留三位有效数字),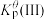
___________ 。
(1)1962年,化学家巴特利特合成了氙的第一个化合物
 ,其在熔化时电离出
,其在熔化时电离出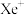 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: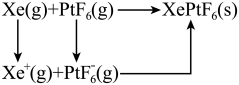
 )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为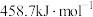 。
。②Xe的第一电离能为
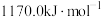 。
。③

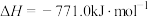 。
。根据以上信息,计算反应
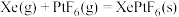

 。
。(2)不久,在三个不同实验室里又分别合成了
 、
、 、
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为 。
。
 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。已知:分压=总压×该组分物质的量分数;
对于反应
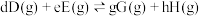
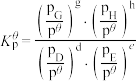
其中
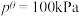 ,
,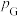 、
、 、
、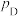 、
、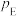 为各组分的平衡分压。
为各组分的平衡分压。标准压强平衡常数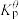 反应平衡 | 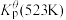 | 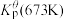 |
反应I: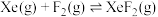  | 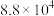 | 360 |
反应II: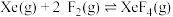  | ||
反应III: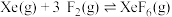  | 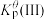 |

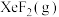 的含量,应
的含量,应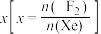 (填“增大”或“减小”)。
(填“增大”或“减小”)。②673K时充入23.77molXe和
 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:| 化学式 |  |  |  |
| 物质的量/mol | 3.60 | 19.80 | 0.36 |
 平衡转化率
平衡转化率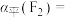
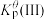
您最近一年使用:0次



