回答下列问题
(1)CH4-CO2催化重整反应为: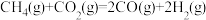 。某温度下,在体积为2L的容器中加入2mol CH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
。某温度下,在体积为2L的容器中加入2mol CH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为___________  。
。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
由上表判断,催化剂X___________ Y (填“优于”或“劣于”),理由是___________ 。
(3)用惰性电极电解下列溶液,按要求回答问题
①NaOH溶液:阳极反应式:___________ ;阴极反应式:___________
② 溶液:电解总反应的离子方程式:
溶液:电解总反应的离子方程式:___________
③HCl溶液:阳极反应式:___________ ;阴极反应式:___________ ;电解总反应的离子方程式:___________
④氯碱工业:阳极反应式:___________ ;电解总反应的离子方程式:___________
(1)CH4-CO2催化重整反应为:
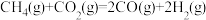 。某温度下,在体积为2L的容器中加入2mol CH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
。某温度下,在体积为2L的容器中加入2mol CH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为 。
。(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应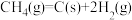 | 消碳反应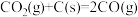 | ||
 /(kJ/mol) /(kJ/mol) | 75 | 172 | |
| 活化能/(kJ/mol) | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
(3)用惰性电极电解下列溶液,按要求回答问题
①NaOH溶液:阳极反应式:
②
 溶液:电解总反应的离子方程式:
溶液:电解总反应的离子方程式:③HCl溶液:阳极反应式:
④氯碱工业:阳极反应式:
更新时间:2021-10-28 15:21:44
|
相似题推荐
【推荐1】水煤气变换[CO(g)+H2O(g)⇌CO2(g)+H2(g) ]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中,其化学平衡常数K和温度T的关系如表所示。
回答下列问题:
(1)该反应的正反应为________ 反应。(填“吸热”或“放热”)
(2)某温度下,各物质的平衡浓度有如下关系:5c(CO)∙c(H2O)=3c(CO2) ∙c(H2),则此时的温度为________ ℃。
(3)830℃时,向2L的密闭容器中充入2molCO(g)和3molH2O(g),反应5min后达到平衡,此时CO的转化率α=________ ;5min内以H2表示的平均反应速率v (H2)=________ mol∙L−1∙min−1;5min后再向容器中充入0.2molCO和0.2molH2,平衡将________ 。(填“正向移动”“逆向移动”或“不移动”)
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1 | 0.59 | 0.38 |
回答下列问题:
(1)该反应的正反应为
(2)某温度下,各物质的平衡浓度有如下关系:5c(CO)∙c(H2O)=3c(CO2) ∙c(H2),则此时的温度为
(3)830℃时,向2L的密闭容器中充入2molCO(g)和3molH2O(g),反应5min后达到平衡,此时CO的转化率α=
您最近一年使用:0次
【推荐2】催化还原法是消除大气中 的主要方法之一。回答下列问题:
的主要方法之一。回答下列问题:
(1)小分子烃类作为还原剂可以在催化剂上选择性还原大气中的 。反应过程中部分热化学方程式如下(
。反应过程中部分热化学方程式如下( 表示正反应的活化能):
表示正反应的活化能):
i.

ii.

iii.

__________ (保留至小数点后一位) ;已知反应
;已知反应 的
的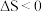 ,则
,则 自发进行的适合条件为
自发进行的适合条件为_______ (填“高温”“低温”或“任意温度”)。
(2)反应动力学研究发现,在催化剂作用下, 燃烧反应对
燃烧反应对 还原大气中的
还原大气中的 有一定的影响。
有一定的影响。
①相同条件下,反应速率:反应i______ (填“>”或“<”)反应ii,理由是_____________________ 。
②在 催化作用下,
催化作用下, 、
、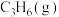 的平衡转化率随温度的变化如图所示:
的平衡转化率随温度的变化如图所示: 的转化率迅速升高,可能的原因为
的转化率迅速升高,可能的原因为______________ ;在673K之后, 的转化率不断升高至完全转化,但NO转化率随着温度升高而降低,试分析可能的原因:
的转化率不断升高至完全转化,但NO转化率随着温度升高而降低,试分析可能的原因:____________________________ (写出一条即可)。
(3)已知:

一定条件下,在1L密闭容器中通入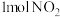 和
和 ,发生反应
,发生反应 ,反应达到平衡后放出的热量为20.9kJ,该反应的平衡常数为
,反应达到平衡后放出的热量为20.9kJ,该反应的平衡常数为____ 。
(4)含铜催化剂可用于氨选择性催化还原 。CuCl是一种应用较广的含铜催化剂,CuCl的晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
。CuCl是一种应用较广的含铜催化剂,CuCl的晶胞结构如图1,沿x、y、z轴方向的投影均为图2。____________ 。
②设 为阿伏加德罗常数的值,晶体密度为
为阿伏加德罗常数的值,晶体密度为 ,则晶胞中相邻Cu之间的最短距离为
,则晶胞中相邻Cu之间的最短距离为________ (列出计算式)pm。
 的主要方法之一。回答下列问题:
的主要方法之一。回答下列问题:(1)小分子烃类作为还原剂可以在催化剂上选择性还原大气中的
 。反应过程中部分热化学方程式如下(
。反应过程中部分热化学方程式如下( 表示正反应的活化能):
表示正反应的活化能):i.


ii.


iii.


 ;已知反应
;已知反应 的
的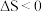 ,则
,则 自发进行的适合条件为
自发进行的适合条件为(2)反应动力学研究发现,在催化剂作用下,
 燃烧反应对
燃烧反应对 还原大气中的
还原大气中的 有一定的影响。
有一定的影响。①相同条件下,反应速率:反应i
②在
 催化作用下,
催化作用下, 、
、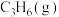 的平衡转化率随温度的变化如图所示:
的平衡转化率随温度的变化如图所示:
 的转化率迅速升高,可能的原因为
的转化率迅速升高,可能的原因为 的转化率不断升高至完全转化,但NO转化率随着温度升高而降低,试分析可能的原因:
的转化率不断升高至完全转化,但NO转化率随着温度升高而降低,试分析可能的原因:(3)已知:


一定条件下,在1L密闭容器中通入
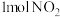 和
和 ,发生反应
,发生反应 ,反应达到平衡后放出的热量为20.9kJ,该反应的平衡常数为
,反应达到平衡后放出的热量为20.9kJ,该反应的平衡常数为(4)含铜催化剂可用于氨选择性催化还原
 。CuCl是一种应用较广的含铜催化剂,CuCl的晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
。CuCl是一种应用较广的含铜催化剂,CuCl的晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
②设
 为阿伏加德罗常数的值,晶体密度为
为阿伏加德罗常数的值,晶体密度为 ,则晶胞中相邻Cu之间的最短距离为
,则晶胞中相邻Cu之间的最短距离为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】二氧化碳是常见的温室气体,其回收利用是环保领域研究的热点课题。
Ⅰ.CO2可以与H2反应合成C2H4,该转化分两步进行:
第一步:CO2(g)+H2(g) CO(g)+H2O(g)△H=+41.3kJ·mol-1
CO(g)+H2O(g)△H=+41.3kJ·mol-1
第二步:2CO(g)+4H2(g) C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
(1)CO2与H2反应反应合成乙烯的热化学方程式为___ 。
(2)一定条件下的密闭容器中,要提高CO2合成乙烯的转化率,可以采取的措施是____ (填标号)。
①减小压强②增大H2的浓度③加入适当催化剂④分离出H2O(g)
(3)已知温度对CO2合成乙烯的平衡转化率及催化剂的催化效率的影响如图所示,下列说法正确的是____ (填标号)。

①N点的速率最大
②M点的平衡常数比N点的平衡常数大
③温度低于250℃时,随温度升高乙烯的平衡产率增大
④实际反应尽可能在较低的温度下进行,以提高CO2的转化率
Ⅱ.研究表明CO2和H2在一定条件下可以合成甲醇,反应方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:

(4)催化效果最佳的是催化剂____ (填“A”、“B”或“C”)。
(5)T2温度下,若反应进行10min达到图中a点状态,用CO2的浓度表示的反应速率v(CO2)=____ 。
(6)图中b点已达平衡状态,则该温度下反应的平衡常数K=____ 。
(7)在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应:CO2(g)+H2(g) CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
注:甲醇的选择性是指发生反应的CO2中转化为甲醇的百分比。表中数据说明,升高温度CO2的实际转化率提高而甲醇的选择性降低,其原因是____ 。
Ⅰ.CO2可以与H2反应合成C2H4,该转化分两步进行:
第一步:CO2(g)+H2(g)
 CO(g)+H2O(g)△H=+41.3kJ·mol-1
CO(g)+H2O(g)△H=+41.3kJ·mol-1第二步:2CO(g)+4H2(g)
 C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1(1)CO2与H2反应反应合成乙烯的热化学方程式为
(2)一定条件下的密闭容器中,要提高CO2合成乙烯的转化率,可以采取的措施是
①减小压强②增大H2的浓度③加入适当催化剂④分离出H2O(g)
(3)已知温度对CO2合成乙烯的平衡转化率及催化剂的催化效率的影响如图所示,下列说法正确的是

①N点的速率最大
②M点的平衡常数比N点的平衡常数大
③温度低于250℃时,随温度升高乙烯的平衡产率增大
④实际反应尽可能在较低的温度下进行,以提高CO2的转化率
Ⅱ.研究表明CO2和H2在一定条件下可以合成甲醇,反应方程式为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
(4)催化效果最佳的是催化剂
(5)T2温度下,若反应进行10min达到图中a点状态,用CO2的浓度表示的反应速率v(CO2)=
(6)图中b点已达平衡状态,则该温度下反应的平衡常数K=
(7)在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应:CO2(g)+H2(g)
 CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:| T(K) | CO2实际转化率(%) | 甲醇选择性(%) |
| 543 | 12.3 | 42.3 |
| 553 | 15.3 | 39.1 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】如图所示装置中,C、D、E、F都是惰性电极,A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)电源电极A名称为_________ 。
(2)写出C和F的电极名称,以及电极反应式。
C:____________________
F:____________________
(3)若装置中通过 电子时,通电后甲池溶液体积为
电子时,通电后甲池溶液体积为 ,则通电后所得
,则通电后所得 溶液的物质的量浓度为
溶液的物质的量浓度为______  。
。
(4)若装置中通过 电子时,丁池中电解足量
电子时,丁池中电解足量 溶液时,某一电极析出了
溶液时,某一电极析出了 金属R,则金属R的相对原子质量的计算公式为
金属R,则金属R的相对原子质量的计算公式为________ (用含a、x的代数式表示)。
(5)现用丙池给铜件镀银,则H应该是______ (填“铜件”或“银”)。

(1)电源电极A名称为
(2)写出C和F的电极名称,以及电极反应式。
C:
F:
(3)若装置中通过
 电子时,通电后甲池溶液体积为
电子时,通电后甲池溶液体积为 ,则通电后所得
,则通电后所得 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(4)若装置中通过
 电子时,丁池中电解足量
电子时,丁池中电解足量 溶液时,某一电极析出了
溶液时,某一电极析出了 金属R,则金属R的相对原子质量的计算公式为
金属R,则金属R的相对原子质量的计算公式为(5)现用丙池给铜件镀银,则H应该是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】工业上常用电解法制备化工产品。
Ⅰ. 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
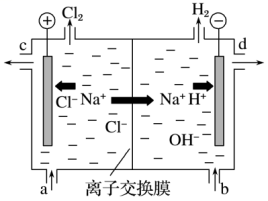
(1)写出电解饱和食盐水的离子方程式_______ 。
(2)精制饱和食盐水从图中_______ 位置补充,氢氧化钠溶液从图中_______ 位置流出。(选填“a”、“b”、“c”或“d”)
Ⅱ. 用惰性电极电解法制备硼酸[H3BO3或B(OH)3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。
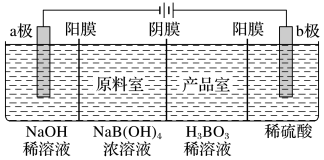
(3)标准状况下,阴极与阳极产生的气体体积比为_______ ;b极的电极反应式为_______ 。
(4)分析产品室中得到H3BO3的原因_______ (可结合化学用语描述)。
(5)每增加1 mol H3BO3产品,NaOH溶液增重_______ g
Ⅰ. 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

(1)写出电解饱和食盐水的离子方程式
(2)精制饱和食盐水从图中
Ⅱ. 用惰性电极电解法制备硼酸[H3BO3或B(OH)3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

(3)标准状况下,阴极与阳极产生的气体体积比为
(4)分析产品室中得到H3BO3的原因
(5)每增加1 mol H3BO3产品,NaOH溶液增重
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)烟气中CO2的捕集可通过如下所示的物质转化实现。
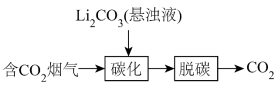
“脱碳”的化学反应方程式为_________ 。
(2)研究脱除烟气中的NO也是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为_______ 。

(3)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。
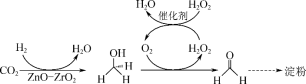
请写出前两步总反应的化学方程式:_________ 。
(4)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如左图所示。其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:

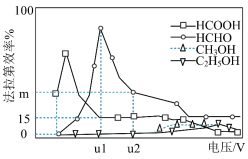
法拉第效率(FE)表示为:FE(B)%= ×100%
×100%
①b电极生成HCOOH的电极反应式为_______ 。
②科研小组利用13CO2代替原有的CO2进行研究,其目的是________ 。
③当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为_______ 。
(1)烟气中CO2的捕集可通过如下所示的物质转化实现。

“脱碳”的化学反应方程式为
(2)研究脱除烟气中的NO也是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示,该过程可描述为

(3)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。

请写出前两步总反应的化学方程式:
(4)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如左图所示。其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:


法拉第效率(FE)表示为:FE(B)%=
 ×100%
×100%①b电极生成HCOOH的电极反应式为
②科研小组利用13CO2代替原有的CO2进行研究,其目的是
③当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率m为
您最近一年使用:0次



