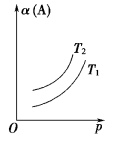
一定条件下,可逆反应aA(g) bB(g)+cC(g)达到平衡状态后,A的转化率α(A)与温度T(且T1<T2),压强(p)的关系如图所示。下列判断正确的是
bB(g)+cC(g)达到平衡状态后,A的转化率α(A)与温度T(且T1<T2),压强(p)的关系如图所示。下列判断正确的是
 bB(g)+cC(g)达到平衡状态后,A的转化率α(A)与温度T(且T1<T2),压强(p)的关系如图所示。下列判断正确的是
bB(g)+cC(g)达到平衡状态后,A的转化率α(A)与温度T(且T1<T2),压强(p)的关系如图所示。下列判断正确的是
| A.a<b+c | B.正反应为吸热反应 |
| C.该反应的平衡常数随温度的升高而增大 | D.该反应用于工业生产时,采用的压强越大越好 |
更新时间:2021-10-23 10:42:42
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】在密闭容器中,进行下列反应: 2A(g)+B(g)+C(s) D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
 D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是| A.若恒温定容情况下,充入一些稀有气体压强增大,但平衡不移动 |
| B.若恒温定压条件下,加入C(s),则B的转化率将增大 |
| C.若定容升温,在新平衡体系中A的质量分数将减小 |
| D.恒容,升高温度,正反应速率减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
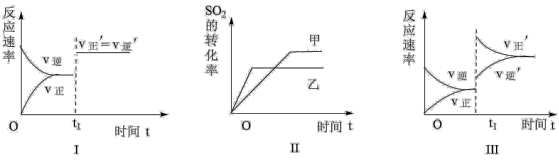
【推荐2】2SO2(g)+O2(g) 2SO3(g) ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是
2SO3(g) ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是
 2SO3(g) ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是
2SO3(g) ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是| A.乙中SO3的体积分数大于丙 |
| B.转化率:α甲(SO2)+α乙(SO3)>1 |
| C.P乙>P丙 |
| D.甲和丙中反应的化学平衡常数互为倒数 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知[Co(H2O)6]2+呈粉红色,[CoC14]2-呈蓝色,[ZnC14]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2+ + 4Cl-  [CoC14]2- + 6H2O ΔH
[CoC14]2- + 6H2O ΔH
用该溶液做实验,溶液的颜色变化如下:
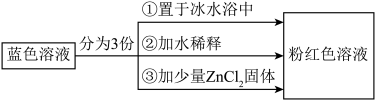
以下结论和解释正确的是
 [CoC14]2- + 6H2O ΔH
[CoC14]2- + 6H2O ΔH用该溶液做实验,溶液的颜色变化如下:

以下结论和解释正确的是
| A.由实验①可推知ΔH < 0 |
| B.等物质的量的[Co(H2O)6]2+和[CoC14]2- 中σ键数之比为9:2 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnC14]2- > [CoC14]2- |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法
I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确 的是( )
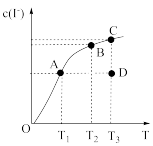
 I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法
I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法
| A.该反应ΔH>0 |
| B.若反应进行到状态D时,一定有v正>v逆 |
| C.若在T1、T2温度下,反应的平衡常数分别为K1、K2,则K1>K2 |
| D.状态A与状态B相比,状态A的c(I3-)大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】向2L恒容密闭容器中充入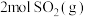 和
和 ,发生如下反应:
,发生如下反应: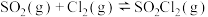 ,测得不同温度下
,测得不同温度下 的转化率
的转化率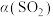 与时间(t)的关系如图所示。假设反应速率方程为
与时间(t)的关系如图所示。假设反应速率方程为 ,
, (k是速率常数,只与温度有关),下列说法错误的是
(k是速率常数,只与温度有关),下列说法错误的是

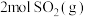 和
和 ,发生如下反应:
,发生如下反应: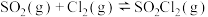 ,测得不同温度下
,测得不同温度下 的转化率
的转化率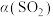 与时间(t)的关系如图所示。假设反应速率方程为
与时间(t)的关系如图所示。假设反应速率方程为 ,
, (k是速率常数,只与温度有关),下列说法错误的是
(k是速率常数,只与温度有关),下列说法错误的是
A.该反应的 |
B. 时, 时, |
C.M点: |
D.升高温度, 增大的倍数大于 增大的倍数大于 增大的倍数 增大的倍数 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知:在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数(简称平衡常数),用符号K表示。对于一般的可逆反应,mA(g)+nB(g) pC(g)+qD(g),当在一定温度下达到平衡时,K=
pC(g)+qD(g),当在一定温度下达到平衡时,K= 。对于给定的反应,化学平衡常数只受温度影响,与反应物或生成物的浓度变化无关。在密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应(温度相同)。下列分析正确的是( )
。对于给定的反应,化学平衡常数只受温度影响,与反应物或生成物的浓度变化无关。在密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应(温度相同)。下列分析正确的是( )
 pC(g)+qD(g),当在一定温度下达到平衡时,K=
pC(g)+qD(g),当在一定温度下达到平衡时,K= 。对于给定的反应,化学平衡常数只受温度影响,与反应物或生成物的浓度变化无关。在密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应(温度相同)。下列分析正确的是( )
。对于给定的反应,化学平衡常数只受温度影响,与反应物或生成物的浓度变化无关。在密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应(温度相同)。下列分析正确的是( )| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| Ⅰ | 恒温恒容 | 放热Q1kJ |
| Ⅱ | 恒温恒压 | 放热Q2kJ |
| A.放出热量:Q1<Q2 | B.N2的转化率:II<I |
| C.平衡常数:II>I | D.平衡时氨气的体积分数:I<II |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】在 下,向两容积均为
下,向两容积均为 的刚性密闭容器中分别投入
的刚性密闭容器中分别投入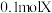 、
、 ,发生反应:
,发生反应: ,X的转化率随反应时间变化曲线如图所示,下列说法正确的是
,X的转化率随反应时间变化曲线如图所示,下列说法正确的是

 下,向两容积均为
下,向两容积均为 的刚性密闭容器中分别投入
的刚性密闭容器中分别投入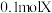 、
、 ,发生反应:
,发生反应: ,X的转化率随反应时间变化曲线如图所示,下列说法正确的是
,X的转化率随反应时间变化曲线如图所示,下列说法正确的是
A.曲线 表示的是 表示的是 反应的转化率 反应的转化率 |
B.逆反应速率: |
C.曲线 中 中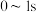 内的平均反应速率 内的平均反应速率 |
D.可利用 所得的平衡常数计算出 所得的平衡常数计算出 达平衡时X的转化率 达平衡时X的转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】向体积可变的密闭容器中通入 和
和 ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
。实验测得平衡时 的转化率
的转化率 随温度、压强的变化如图1所示。下列说法错误的是
随温度、压强的变化如图1所示。下列说法错误的是

 和
和 ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
。实验测得平衡时 的转化率
的转化率 随温度、压强的变化如图1所示。下列说法错误的是
随温度、压强的变化如图1所示。下列说法错误的是
A. 代表压强,且 代表压强,且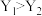 ;X代表温度,且 ;X代表温度,且 |
B.M点反应物转化率之比 ,N点该比例减小 ,N点该比例减小 |
C.若M点对应的容器体积为 ,则N点时反应的化学平衡常数 ,则N点时反应的化学平衡常数 |
D.图2中曲线a能正确表示正反应速率常数的负对数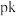 (pk=-lgk)与X的关系 (pk=-lgk)与X的关系 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】处理、回收CO是环境科学家研究的热点课题。CO用于处理大气污染物N2O,发生的反应为:N2O(g)+CO(g)  CO2(g)+N2(g) ΔH=-365 kJ·mol-1。上述反应可用“Fe+”作催化剂,其总反应分两步进行:
CO2(g)+N2(g) ΔH=-365 kJ·mol-1。上述反应可用“Fe+”作催化剂,其总反应分两步进行:
第一步:Fe++N2O=FeO++N2;
第二步:FeO++CO=Fe++CO2,第二步反应不影响总反应达到平衡所用的时间。
下列说法中正确的是
 CO2(g)+N2(g) ΔH=-365 kJ·mol-1。上述反应可用“Fe+”作催化剂,其总反应分两步进行:
CO2(g)+N2(g) ΔH=-365 kJ·mol-1。上述反应可用“Fe+”作催化剂,其总反应分两步进行:第一步:Fe++N2O=FeO++N2;
第二步:FeO++CO=Fe++CO2,第二步反应不影响总反应达到平衡所用的时间。
下列说法中正确的是
| A.FeO+也是该反应的催化剂 |
| B.第一步中Fe+与N2O的碰撞仅部分有效 |
| C.第二步反应速率大于第一步反应速率 |
| D.增大CO的浓度可显著增大处理N2O的反应速率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】SO2、NOx是主要的大气污染物。某研究小组采用微生物法同时脱硫脱硝(细菌生存的最佳温度为30~45℃,pH值为6.5~8.5),研究结果表明pH对脱硫、脱硝效果的影响如图1所示。该小组采用催化反应法研究时,发现NH3和NO在Ag2O催化剂表面反应时,相同时间条件下,NO生成N2的转化率随温度的变化关系如图2所示。下列说法正确的是
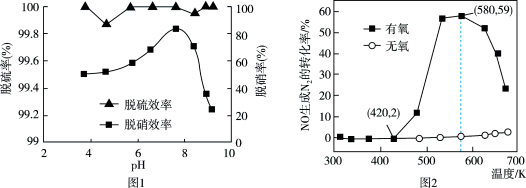

| A.从图 1 中可以看出,采用微生物治理法时应选择的最佳 pH 值是 8 |
| B.图 1 中 pH 过大时,细菌活性迅速降低,脱硝效率明显下降 |
| C.图 2 中,在温度为 420~580 K 时,有氧条件下 NO 生成 N2的转化率明显高于无氧条件的原因可能是:NO 与 O2反应生成 NO2,NO2更易与 NH3反应 |
| D.图 2 中,在有氧条件下,温度 580 K 之后 NO 生成 N2的转化率降低是因为 Ag2O 催化剂活性下降 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】在2 L恒容密闭容器中充入1mol CO、2mol H2,在一定条件下发生如下反应:2H2(g)+CO(g) CH3OH(g) ΔH=-90.1kJ·mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是
CH3OH(g) ΔH=-90.1kJ·mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是
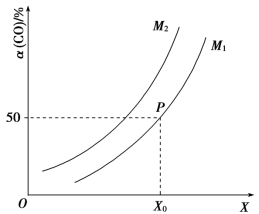
 CH3OH(g) ΔH=-90.1kJ·mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是
CH3OH(g) ΔH=-90.1kJ·mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是
| A.工业上,利用上述反应合成甲醇,温度越高越好 |
| B.图像中X代表压强,M1与M2代表不同温度,且M2<M1 |
| C.图像中P点代表的平衡常数K的数值为4 |
| D.若维持温度和容器容积不变,再充入1mol CO、2mol H2,达到平衡时CO的转化率不变 |
您最近一年使用:0次

 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是