下列事实中不能用勒夏特列原理加以解释的是
A.高压有利于合成 的反应 的反应 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
| D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 |
更新时间:2021-11-03 15:55:56
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某温度下,在恒容密闭容器中,加入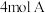 和
和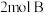 进行如下反应:
进行如下反应: 。反应一段时间后达到平衡,测得生成
。反应一段时间后达到平衡,测得生成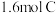 ,且反应前后的压强之比为5:4。下列说法正确的是
,且反应前后的压强之比为5:4。下列说法正确的是
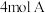 和
和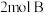 进行如下反应:
进行如下反应: 。反应一段时间后达到平衡,测得生成
。反应一段时间后达到平衡,测得生成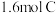 ,且反应前后的压强之比为5:4。下列说法正确的是
,且反应前后的压强之比为5:4。下列说法正确的是A.该反应的平衡常数表达式为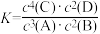 |
| B.平衡时,B的转化率为40% |
| C.增加生成物C的量,B的转化率变小 |
| D.增大压强,平衡向右移动,化学平衡常数K增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】臭氧(O3)是一种很好的消毒剂,可溶于水且在水中易分解产生游离氧原子[O],[O]具有很强的杀菌消毒能力。常温常压下发生反应如下:反应①O3 O2+[O] ΔH>0平衡常数为K1;反应②O3+[O]
O2+[O] ΔH>0平衡常数为K1;反应②O3+[O] 2O2 ΔH<0 平衡常数为K2;总反应为2O3
2O2 ΔH<0 平衡常数为K2;总反应为2O3 3O2 ΔH<0 平衡常数为K;下列叙述正确的是
3O2 ΔH<0 平衡常数为K;下列叙述正确的是
 O2+[O] ΔH>0平衡常数为K1;反应②O3+[O]
O2+[O] ΔH>0平衡常数为K1;反应②O3+[O] 2O2 ΔH<0 平衡常数为K2;总反应为2O3
2O2 ΔH<0 平衡常数为K2;总反应为2O3 3O2 ΔH<0 平衡常数为K;下列叙述正确的是
3O2 ΔH<0 平衡常数为K;下列叙述正确的是| A.适当升高温度,可提高消毒效率 |
| B.K=K1+K2 |
| C.使用合适催化剂,可使O3完全转化为O2 |
| D.压强增大,K2减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列关于实验现象的解释或所得结论正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某补血口服液中滴加酸性 溶液 溶液 | 酸性 溶液紫色褪去 溶液紫色褪去 | 该补血口服液中一定含有 |
| B | 用蒸馏水溶解 固体,并继续加水稀释 固体,并继续加水稀释 | 溶液由绿色逐渐变为蓝色 | 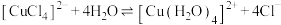 正向移动,黄绿色配离子转变为蓝色 正向移动,黄绿色配离子转变为蓝色 |
| C | 向NaBr溶液中滴加过量氯水,再加入淀粉-KI溶液 | 溶液先变橙色,后变为蓝色 | 氧化性: |
| D | 将铜与浓硫酸反应产生的气体通入 溶液中 溶液中 | 产生白色沉淀 | 该气体中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实,不能用勒夏特列原理来解释的是
| A.往稀硫酸中加入铁粉,溶液颜色加深 |
B.升高温度, 的醋酸溶液的导电能力增强 的醋酸溶液的导电能力增强 |
| C.拧开可乐瓶盖,有大量气泡冒出 |
| D.实验室制备乙酸乙酯时,使用过量的乙醇作原料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列过程中的颜色变化不能用勒夏特列原理解释的是
A.向5mL0.1mol•L-1重铬酸钾溶液中(存在平衡: (橙色)+H2O⇌2 (橙色)+H2O⇌2 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 |
| B.对2NO2(g)⇌N2O4(g)平衡体系增大压强(缩小体积)的瞬间,气体的颜色变深 |
| C.将NO2球浸泡在热水中,红棕色变深 |
| D.溴水中有平衡:Br2+H2O⇌HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g)  COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
下列说法正确的是( )
 COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:| 实验 | 温度/℃ | 起始时 | 平衡时 | |||
| n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
| 1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
| 2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
| 3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
| A.上述反应是吸热反应 |
| B.实验1达平衡时,CO的转化率为70% |
| C.实验2达平衡时,a<7.0 |
| D.实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,可溶性一元弱碱ROH的 。在某体系中,
。在某体系中, 与
与 离子不能穿过隔膜,未电离的ROH可自由穿过该膜(如图所示)。当达到平衡时,下列叙述不正确的是
离子不能穿过隔膜,未电离的ROH可自由穿过该膜(如图所示)。当达到平衡时,下列叙述不正确的是

 。在某体系中,
。在某体系中, 与
与 离子不能穿过隔膜,未电离的ROH可自由穿过该膜(如图所示)。当达到平衡时,下列叙述不正确的是
离子不能穿过隔膜,未电离的ROH可自由穿过该膜(如图所示)。当达到平衡时,下列叙述不正确的是
A.溶液Ⅰ和Ⅱ中的 相等 相等 |
B.溶液Ⅰ中 |
| C.溶液Ⅱ中的ROH的电离度约为1/101 |
| D.增大溶液Ⅰ的pH必然使溶液Ⅱ中的pH也增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A. 的电离方程式为 的电离方程式为 |
B.向 溶液中加水,氢氧根离子浓度减小,氢离子的物质的量增加 溶液中加水,氢氧根离子浓度减小,氢离子的物质的量增加 |
C.虽然 溶于水所得溶液中导电的离子不是它本身产生的,但它却是电解质 溶于水所得溶液中导电的离子不是它本身产生的,但它却是电解质 |
D.室温下 的 的 溶液和 溶液和 的 的 溶液中, 溶液中, 小于 小于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知 25℃时有关弱酸的电离平衡常数:
下列有关说法正确的是
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A.1 mol·L-1HCN溶液与1mol·L-1 NaOH溶液等体积混合后,测得所得溶液显酸性 |
| B.等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| C.NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) |
| D.1mol/L醋酸溶液加水稀释,所有离子浓度均减小 |
您最近一年使用:0次



