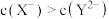某温度下,向10mL0.1mol·L-1 NaCl溶液和10 mL 0.1mol·L-1 K2CrO4溶液中分别滴加0.l mol·L-1 AgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
 )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
A.该温度下, |
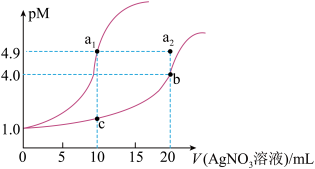
B. 、b、c三点所示溶液中 、b、c三点所示溶液中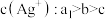 |
| C.若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点 |
| D.用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂 |
更新时间:2021-11-22 13:15:03
|
相似题推荐
多选题
|
适中
(0.65)
名校
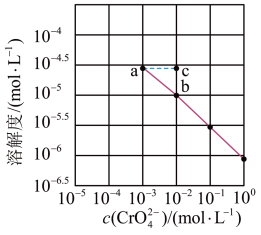
【推荐1】已知溶解度也可用物质的量浓度表示,25℃时, 在不同浓度
在不同浓度 溶液中的溶解度如图所示,下列说法错误的是
溶液中的溶解度如图所示,下列说法错误的是
 在不同浓度
在不同浓度 溶液中的溶解度如图所示,下列说法错误的是
溶液中的溶解度如图所示,下列说法错误的是
A.图中a、b两点 相同 相同 |
B.图中a点与b点 溶度积相等 溶度积相等 |
C.在a点向溶液中加入少量 ,溶解度可变为c点 ,溶解度可变为c点 |
D.该温度下, 溶度积的数量级为 溶度积的数量级为 |
您最近一年使用:0次
【推荐2】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述正确的是
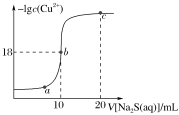

| A.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| B.Ksp(CuS)的数量级为10-36 |
| C.a、b、c三点溶液中,b点水的电离程度最大 |
| D.c点溶液中:2c(Cl-)=c(Na+) |
您最近一年使用:0次
【推荐3】常温下,金属离子(Mn+)浓度的负对数随溶液pH变化的关系如图所示[已知:pM=-lgc(Mn+),且假设c(Mn+)≤10-6mol·L-1认为该金属离子已沉淀完全]。下列说法正确的是
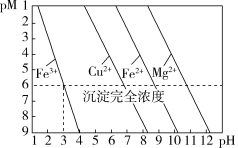

| A.常温下,Ksp[Mg(OH)2]>Ksp[Fe(OH)2] |
| B.可以通过调节溶液pH的方法分步沉淀Cu2+和Fe2+ |
| C.除去Cu2+中少量Fe3+,可控制溶液3≤pH<4 |
| D.pM与Ksp之间的关系式为pM=lgKsp-nlgc(OH-) |
您最近一年使用:0次
【推荐1】下列实验操作能达到实验目的的是
| 选项 | 操作及现象 | 目的 |
| A | 将含少量 的 的 溶于浓氨水中,过滤、洗涤、干燥 溶于浓氨水中,过滤、洗涤、干燥 | 提纯 |
| B | 加热溴乙烷和NaOH的乙醇溶液混合物,产生的气体通入酸性 溶液,溶液褪色 溶液,溶液褪色 | 证明溴乙烷发生了消去反应 |
| C | 在饱和 溶液中加入少量KI粉末,产生黄色沉淀 溶液中加入少量KI粉末,产生黄色沉淀 | 证明溶液存在沉淀溶解平衡 |
| D | 在 溶液中滴加酸化的双氧水,溶液变棕色 溶液中滴加酸化的双氧水,溶液变棕色 | 探究 、 、 的还原性强弱 的还原性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
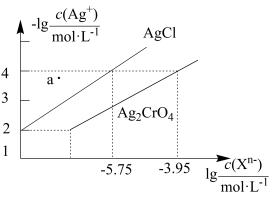
【推荐2】常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的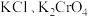 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
A.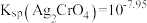 |
B.a点时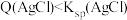 |
C.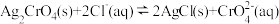 的平衡常数为 的平衡常数为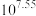 |
D.向等物质的量浓度的 与 与 混合液中逐滴滴加 混合液中逐滴滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列解释事实的方程式正确的是
| A.用FeCl3溶液制作铜质印刷线路板: 2Fe3++Cu =Cu2+ +2Fe2+ |
B.Al 片溶于NaOH溶液中产生气体: 2Al +2OH-=2AlO +H2↑ +H2↑ |
| C.用难溶的MnS除去MnCl2溶液中含有的Pb2+:MnS(s) + Pb2+(aq) =PbS(s) + Mn2+ (aq) |
D.向银氨溶液中滴加乙醛后水浴加热,出现银镜:CH3CHO+Ag(NH3)2OH CH3COONH4 +Ag↓+3NH3 +H2O CH3COONH4 +Ag↓+3NH3 +H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作、现象 | 结论 |
| A | 向 溶液中滴加 溶液中滴加 溶液,有白色胶状沉淀生成 溶液,有白色胶状沉淀生成 |  结合氢离子能力比 结合氢离子能力比 强 强 |
| B | 向等体积、等浓度的稀硫酸中分别加入少许等物质的量的ZnS和CuS固体,ZnS溶解而CuS不溶解 | 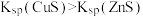 |
| C | 常温下,用pH计测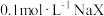 溶液和 溶液和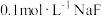 溶液的pH,前者小于后者 溶液的pH,前者小于后者 | 酸性:HX<HF |
| D | 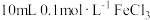 溶液和 溶液和 溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色 溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色 | 溶液中存在平衡: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.在一定温度下的AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数 |
| B.AgCl的Ksp=1.8×10-10 mol2·L-2在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2·L-2 |
| C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,此溶液为AgCl的饱和溶液 |
| D.向饱和AgCl水溶液中充入HCl,AgCl(s)⇌Ag+(aq)+Cl-(aq)平衡逆向移动 |
您最近一年使用:0次
【推荐3】下列实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溶液中滴加经过盐酸酸化的BaCl2溶液 | 溶液中产生白色沉淀 | 溶液中一定含有SO |
| B | 向盛有Fe(NO3)2溶液的试管中加入0.1mol·L-1H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO 被Fe2+还原为NO2 被Fe2+还原为NO2 |
| C | 用蘸有浓氨水的玻璃棒靠近某有色气体X | 玻璃棒周围产生白烟 | 气体X可能是氯气 |
| D | 向等浓度的KCl、KI溶液中分别滴加0.1mol·L-1AgNO3溶液2滴 | 只有KI溶液中出现沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】铬酸银(Ag2CrO4)微溶于水。常用作分析试剂,有机合成催化剂,电镀, 卤化物滴定确定终点的指示剂等。在 t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10−10.下列说法不正确的是


| A.t℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 |
| C.t℃时,Ag2CrO4的Ksp为 1×10−8 |
D.t℃时,将 0.01mol·L−1AgNO3溶液滴入20mL0.01mol·L−1KCl和 0.01mol·L−1K2CrO4的混合溶液中,CrO 先沉淀 先沉淀 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】草酸(H2C2O4)是一种二元弱酸。实验室配制了0.0100mol•L﹣1Na2C2O4标准溶液,现对25℃时该溶液的性质进行探究,下列所得结论正确的是
A.测得0.0100mol•L﹣1Na2C2O4溶液pH为8.6,此时溶液中存在:c(Na+)>c( )>c( )>c( )>c(H+) )>c(H+) |
B.向该溶液中滴加稀盐酸至溶液pH=7,此时溶液中存在:c(Na+)=c( )+2c( )+2c( ) ) |
C.向该溶液中加入足量稀硫酸酸化后,再滴加KMnO4溶液,发生反应的离子方程式为 +4 +4 +14H+=2CO2↑+4Mn2++7H2O +14H+=2CO2↑+4Mn2++7H2O |
D.已知CaC2O4难溶于水,存在溶解平衡,25℃时饱和CaC2O4溶液的浓度为5×10﹣5mol•L﹣1,向该溶液中加入等体积0.0200mol•L﹣1CaCl2溶液,所得上层清液中c( )<5.00×10﹣5mol•L﹣1 )<5.00×10﹣5mol•L﹣1 |
您最近一年使用:0次

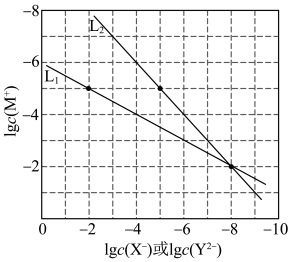
 价)的饱和溶液中离子浓度的关系如图所示。下列说法正确的是
价)的饱和溶液中离子浓度的关系如图所示。下列说法正确的是