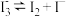下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作、现象 | 结论 |
| A | 向 溶液中滴加 溶液中滴加 溶液,有白色胶状沉淀生成 溶液,有白色胶状沉淀生成 |  结合氢离子能力比 结合氢离子能力比 强 强 |
| B | 向等体积、等浓度的稀硫酸中分别加入少许等物质的量的ZnS和CuS固体,ZnS溶解而CuS不溶解 | 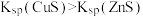 |
| C | 常温下,用pH计测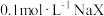 溶液和 溶液和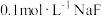 溶液的pH,前者小于后者 溶液的pH,前者小于后者 | 酸性:HX<HF |
| D | 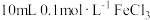 溶液和 溶液和 溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色 溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色 | 溶液中存在平衡: |
| A.A | B.B | C.C | D.D |
更新时间:2022-01-24 18:27:35
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】在密闭容器中X2 (g)+2Y2 (g) Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是
Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是
 Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是
Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是| A.c(Z) =0.45mol/L | B.c(X2) =0.3mol/L |
| C.c(X2) =0.5mol/L | D.c(Y2) =0.5mol/L |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】一定温度下, 将2 mol SO2 和 1 mol O2 充入一定容积的密闭容器中, 在催化剂存在下进行下列反应: 2SO2(g) + O2(g)  2SO3(g) △H= -197 kJ/ mol, 当达到平衡状态时,下列说法中正确的是
2SO3(g) △H= -197 kJ/ mol, 当达到平衡状态时,下列说法中正确的是
 2SO3(g) △H= -197 kJ/ mol, 当达到平衡状态时,下列说法中正确的是
2SO3(g) △H= -197 kJ/ mol, 当达到平衡状态时,下列说法中正确的是| A.达到反应限度时,生成 SO3 为2 mol |
| B.达到反应限度时反应放出的热量小于197 kJ |
| C.达到反应限度时SO2、O2、SO3的分子数之比一定为2∶1∶2 |
| D.达到反应限度时SO2的消耗速率等于SO3的消耗速率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.pH=2和pH=1的HNO3溶液中c(H+)之比为1∶10 |
| B.0.2mol/L与0.1mol/L醋酸溶液中,c(H+)之比大于2∶1 |
C.Na2CO3溶液中c(Na+)与c(CO )之比为2∶1 )之比为2∶1 |
| D.100mL0.1mol/L的醋酸溶液与10mL1.0mol/L的醋酸溶液中H+的数目,前者多 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列实验操作、实验现象及解释或结论都正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 工业上用 与焦炭在高温条件制备粗硅 与焦炭在高温条件制备粗硅 | 生成可燃性气体,得到黑色固体粗硅 | 非金属性:C>Si |
| B | 常温下,用pH计分别测定等体积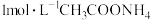 溶液和 溶液和 溶液的pH 溶液的pH | 测得pH都等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| C | 两块相同的未经打磨的铝片,相同温度下分别投入到5.0mL等浓度的 溶液和 溶液和 溶液中 溶液中 | 前者无明显现象,后者铝片发生溶解 |  能破坏铝片表面的氧化膜 能破坏铝片表面的氧化膜 |
| D | 向 溶液中通入 溶液中通入 气体 气体 | 产生白色沉淀 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐3】下列实验操作或设计与实验现象、结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 取少量某溶液于试管中,加入 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 湿润的红色石蕊试纸变蓝 | 溶液中一定含有 |
| B | 向 浓度为 浓度为 的 的 溶液中逐滴加入等浓度的 溶液中逐滴加入等浓度的 溶液 溶液 | 溶液褪色 |  漂白溶液,表现强氧化性 漂白溶液,表现强氧化性 |
| C | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 溶液 溶液 | 白色沉淀产生 | 样品已经变质 |
| D | 室温下,用 试纸分别测定浓度均为 试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 溶液 : : 约为9, 约为9, 约为10 约为10 | 酸性: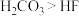 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】根据下列图示所得出的结论不正确 的是
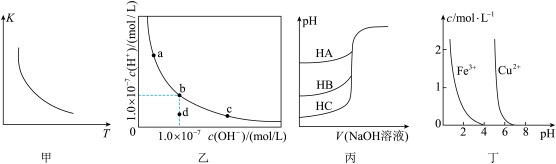

A.图甲是一定条件下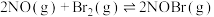 的平衡常数K随温度变化的曲线,可推知该反应的 的平衡常数K随温度变化的曲线,可推知该反应的 |
B.图乙是一定温度下水溶液中 、 、 的变化曲线。该温度下,加水稀释NaOH溶液可能引起沿曲线由c向b的变化 的变化曲线。该温度下,加水稀释NaOH溶液可能引起沿曲线由c向b的变化 |
| C.图丙是室温下用0.01mol/L NaOH溶液分别滴定同浓度同体积的HA、HB、HC三种酸的滴定曲线,可推知HA的酸性最强 |
D.图丁是在溶液中 、 、 的浓度与pH的关系曲线。可推知用氢氧化物沉淀除去 的浓度与pH的关系曲线。可推知用氢氧化物沉淀除去 溶液混有的 溶液混有的 ,所调pH的范围大致应为4~5 ,所调pH的范围大致应为4~5 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法中错误的是
A.某温度时的混合溶液中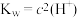 ,说明该溶液呈中性( ,说明该溶液呈中性( 为该温度时水的离子积常数) 为该温度时水的离子积常数) |
B.常温下,由水电离出的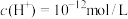 的溶液的pH可能为2或12 的溶液的pH可能为2或12 |
C.已知 , ,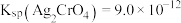 ,向含有 ,向含有 、 、 且浓度均为0.010mol/L溶液中逐滴加入0.010mol/L的AgNO3溶液时, 且浓度均为0.010mol/L溶液中逐滴加入0.010mol/L的AgNO3溶液时, 先产生沉淀 先产生沉淀 |
D.常温下CH3COOH的电离平衡常数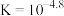 ,某pH=4.8的CH3COOH和CH3COONa混合溶液中, ,某pH=4.8的CH3COOH和CH3COONa混合溶液中,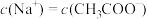 |
您最近一年使用:0次
【推荐3】利用平衡移动原理,分析一定温度下Mg2+在不同pH的Na2CO3体系中的可能产物。
已知:ⅰ、图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ、图2中曲线Ⅰ的离子浓度关系符合c(Mg2+)·c2(OH-)=Ksp[Mg(OH)2];曲线Ⅱ的离子浓度关系符合c(Mg2+)·c( )=Ksp(MgCO3);
)=Ksp(MgCO3);
[注:起始c(Na2CO3)=0.1mol·L−1,不同pH下c( )由图1得到]。
)由图1得到]。
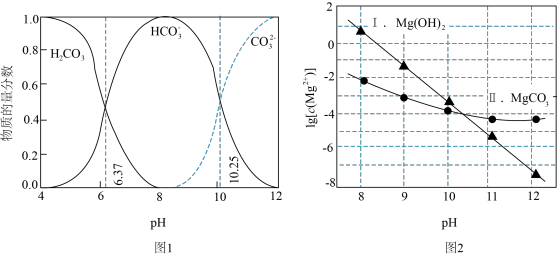
下列说法正确的是
已知:ⅰ、图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ、图2中曲线Ⅰ的离子浓度关系符合c(Mg2+)·c2(OH-)=Ksp[Mg(OH)2];曲线Ⅱ的离子浓度关系符合c(Mg2+)·c(
 )=Ksp(MgCO3);
)=Ksp(MgCO3);[注:起始c(Na2CO3)=0.1mol·L−1,不同pH下c(
 )由图1得到]。
)由图1得到]。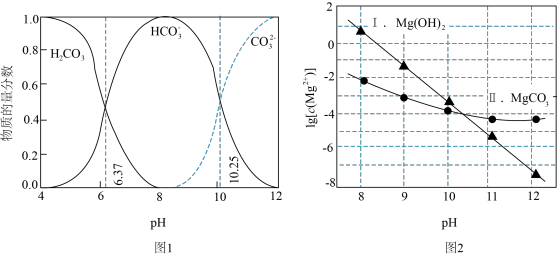
下列说法正确的是
A.由图1,pH=10.25,c( )=c( )=c( ) ) |
| B.由图2,初始状态pH=11、lg[c(Mg2+)]=-6,有沉淀生成 |
C.由图2,初始状态pH=9、lg[c(Mg2+)]=-2,平衡后溶液中存在:c(H2CO3)+c( )+c( )+c( )=0.1mol·L−1 )=0.1mol·L−1 |
D.由图1和图2,初始状态pH=8、lg[c(Mg2+)]=-1,发生反应:Mg2++2 =MgCO3↓+CO2↑+H2O =MgCO3↓+CO2↑+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】为完成下列各组实验,所选玻璃仪器和试剂均正确、完整的是(非玻璃仪器任选;不考虑存放试剂的容器)
| 实验 | 玻璃仪器 | 试剂 | |
| A | 证明HClO是弱酸 | 表面皿、玻璃棒 |  NaClO溶液 NaClO溶液 |
| B | 证明HCN和碳酸的酸性强弱 | 玻璃棒、玻璃片 |  NaCN溶液和 NaCN溶液和 Na2CO3溶液 Na2CO3溶液 |
| C | 测定醋酸溶液浓度 | 酸式滴定管、碱式滴定管、锥形瓶、烧杯 | 待测醋酸溶液、标准NaOH溶液、酚酞溶液 |
| D | 证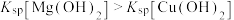 | 试管、胶头滴管 | 含有少量CuCl2的MgCl2溶液、稀氨水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列说法中不正确的是
| A.S在过量的O2中充分燃烧生成SO3 |
| B.常温下,浓硝酸可以用铁罐车贮运 |
| C.可用稀盐酸来鉴别NaHCO3溶液与Na2CO3溶液 |
| D.除去CO2中混有的HCl,可通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】我国自主发明的“钛战甲”——钛合金材料,为实现万米深潜的“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。四氯化钛(TiCl4)是生产钛合金的重要原料,某化学实验小组以TiO2和足量CCl4为原料制取TiCl4,装置如下图:
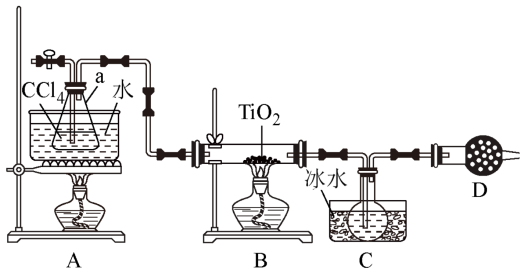
有关物质的性质如表:
下列说法错误的是

有关物质的性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| CCl4 | -23 | 76.8 | 与TiCl4互溶 |
| TiCl4 | -23 | 136 | 遇潮湿空气产生白雾 |
| A.欲分离C装置中的TiCl4,应采用的实验操作为蒸发 |
| B.实验开始时,先用N2或CCl4蒸气将装置中的空气排出 |
| C.钛合金强度大,能承受剧烈的压强差考验,可以适应万米深潜器的压强变化 |
D.B中TiO2反应的化学方程式为 ,该反应是氧化还原反应 ,该反应是氧化还原反应 |
您最近一年使用:0次

 的集气瓶中,有大量白烟和黑色颗粒产生
的集气瓶中,有大量白烟和黑色颗粒产生 溶液,生成蓝色沉淀
溶液,生成蓝色沉淀 ,不含有
,不含有
 溶液中通入
溶液中通入
 溶液的试管中,分别滴加淀粉溶液和
溶液的试管中,分别滴加淀粉溶液和 溶液,前者溶液变蓝,后者生成黄色沉淀
溶液,前者溶液变蓝,后者生成黄色沉淀