已知25℃时, 的
的 。
。
(1)当向醋酸中加入一定量的盐酸时, 的电离常数是否发生变化?为什么?
的电离常数是否发生变化?为什么?___________
(2)若初始时醋酸中 的浓度为0.010mol/L,则达到电离平衡时溶液中
的浓度为0.010mol/L,则达到电离平衡时溶液中 是多少?
是多少?___________
 的
的 。
。(1)当向醋酸中加入一定量的盐酸时,
 的电离常数是否发生变化?为什么?
的电离常数是否发生变化?为什么?(2)若初始时醋酸中
 的浓度为0.010mol/L,则达到电离平衡时溶液中
的浓度为0.010mol/L,则达到电离平衡时溶液中 是多少?
是多少?
更新时间:2021-12-01 23:57:53
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)工业上将含有硫化物的废水(以H2S、HS-、S2−的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+,碱性条件下的为MnO2。
①pH>7时高锰酸钾将废水中的硫化物氧化为S,该反应的离子方程式为_______ 。
②研究发现:其他条件相同时,废水呈酸性时硫化物的去除率明显大于呈碱性时去除率,则可能的原因_______ 。
(2)表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用图1表示。其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。

①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是_______ 。
②若水膜过厚,H2S的氧化去除率减小的原因是_______ 。
(3)向100mL含Na2CO3、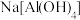 的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:

①已知 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式为
在溶液中反应而不能大量共存,写出两者反应的离子方程式为_______ 。
②d曲线表示的离子方程式为_______ 。
③加入HCl溶液的物质的量浓度为_______ 。
④原混合溶液中的Na+与 的物质的量之比为
的物质的量之比为_______ 。
(1)工业上将含有硫化物的废水(以H2S、HS-、S2−的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+,碱性条件下的为MnO2。
①pH>7时高锰酸钾将废水中的硫化物氧化为S,该反应的离子方程式为
②研究发现:其他条件相同时,废水呈酸性时硫化物的去除率明显大于呈碱性时去除率,则可能的原因
(2)表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用图1表示。其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。

①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是
②若水膜过厚,H2S的氧化去除率减小的原因是
(3)向100mL含Na2CO3、
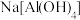 的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
①已知
 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式为
在溶液中反应而不能大量共存,写出两者反应的离子方程式为②d曲线表示的离子方程式为
③加入HCl溶液的物质的量浓度为
④原混合溶液中的Na+与
 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】水体中的含氮化合物是引起富营养化的主要污染物,分析监测水体中的硝酸(盐)和亚硝酸(盐)含量,控制水体中的含氮污染物,对水资源的循环利用意义重大。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为___________ ,其电离平衡常数的表达式为___________ 。
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为___________ 。
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为___________ ,其中氧化产物为___________ (写化学式)。
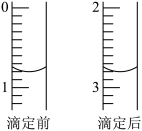
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为___________ mg/L。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为

您最近一年使用:0次
填空题
|
较易
(0.85)
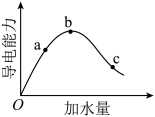
【推荐3】在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,请填写下列空白。
(1)写出醋酸的电离方程式___ 。
(2)a、b、c三点对应的溶液中,c(H+)由大到小的顺序为___ ,醋酸的电离程度由大到小的顺序为__ 。
(3)若使c点溶液中c(CH3COO-)增大,可采取的措施是___ (填标号)。
(4)25℃时,醋酸的电离平衡常数Ka=1.8×10-5,0.1mol•L-1醋酸溶液中c(H+)=___ (已知: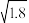 =1.34)。
=1.34)。
(5)c(H+)相同、体积相同的盐酸和醋酸分别与足量的锌反应,生成的H2在相同状况下的体积分别为V1和V2,则V1___ V2(填“>”“<”或“=”,下同);物质的量浓度相同、体积相同的盐酸和醋酸分别与足量的锌反应,生成的H2在相同状况下的体积分别为V3和V4,则V3__ V4。

(1)写出醋酸的电离方程式
(2)a、b、c三点对应的溶液中,c(H+)由大到小的顺序为
(3)若使c点溶液中c(CH3COO-)增大,可采取的措施是
| A.加水 | B.加入少量固体CH3COONa |
| C.加少量浓盐酸 | D.加入少量浓氨水 |
(4)25℃时,醋酸的电离平衡常数Ka=1.8×10-5,0.1mol•L-1醋酸溶液中c(H+)=
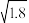 =1.34)。
=1.34)。(5)c(H+)相同、体积相同的盐酸和醋酸分别与足量的锌反应,生成的H2在相同状况下的体积分别为V1和V2,则V1
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学上常用电离度表示电解质的相对强弱:α=已电离的电解质分子数/溶液中原有电解质的总分子数×100%。
(1)25℃时,0.1 mol·L-1上述几种溶液中,c(H+)从大到小的顺序是______ (填序号);
(2)25℃时,0.1 mol·L-1硫酸溶液中HSO的电离度小于相同温度下0.1 mol·L-1硫酸氢钠溶液中HSO的电离度,其原因是______ 。
| 物质(微粒)及编号 | 电离度α |
A.硫酸溶液(第一步完全电离):HSO ⇌H++SO ⇌H++SO | 10% |
B.硫酸氢钠溶液:HSO ⇌H++SO ⇌H++SO | 29% |
| CH3COOH⇌CH3COO-+H+ | 1.33% |
| D.盐酸:HCl=H++Cl- | 100% |
(1)25℃时,0.1 mol·L-1上述几种溶液中,c(H+)从大到小的顺序是
(2)25℃时,0.1 mol·L-1硫酸溶液中HSO的电离度小于相同温度下0.1 mol·L-1硫酸氢钠溶液中HSO的电离度,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题:

(1)O点导电能力为零的原因是__________________________________ 。
(2)a、b、c三点中,CH3COOH的电离度最大的是________ ;CH3COOH的电离平衡常数表达式Ka=______________________ 。
(3)若使c点溶液中c(CH3COO-)增大,则下列措施中,可选择______ (填字母序号)。
A.加热 B.加入很稀的NaOH溶液 C.加入固体KOH
D.加水 E.加入固体CH3COONa F.加入锌粒
(4)在CH3COOH溶液的稀释过程中,始终保持增大趋势的是________ (填字母序号)。
A.c(H+) B.H+的个数 C.CH3COOH的分子数 D.c(H+)/c(CH3COOH)
(5)下列有关CH3COOH溶液的说法正确的是________ (填字母序号)。
A.CH3COOH溶液中各离子浓度的关系为c(H+)=c(OH-)+c(CH3COO-)
B.向0.10 mol/L的CH3COOH溶液中加水,c(H+)增大
C.CH3COOH溶液中各离子浓度的关系为c(CH3COO-)>c(H+)>c(OH-)
D.常温下,c(H+)=0.01 mol/L的CH3COOH溶液与c(OH-)=0.01 mol/L的NaOH溶液等体积混合后,溶液呈碱性

(1)O点导电能力为零的原因是
(2)a、b、c三点中,CH3COOH的电离度最大的是
(3)若使c点溶液中c(CH3COO-)增大,则下列措施中,可选择
A.加热 B.加入很稀的NaOH溶液 C.加入固体KOH
D.加水 E.加入固体CH3COONa F.加入锌粒
(4)在CH3COOH溶液的稀释过程中,始终保持增大趋势的是
A.c(H+) B.H+的个数 C.CH3COOH的分子数 D.c(H+)/c(CH3COOH)
(5)下列有关CH3COOH溶液的说法正确的是
A.CH3COOH溶液中各离子浓度的关系为c(H+)=c(OH-)+c(CH3COO-)
B.向0.10 mol/L的CH3COOH溶液中加水,c(H+)增大
C.CH3COOH溶液中各离子浓度的关系为c(CH3COO-)>c(H+)>c(OH-)
D.常温下,c(H+)=0.01 mol/L的CH3COOH溶液与c(OH-)=0.01 mol/L的NaOH溶液等体积混合后,溶液呈碱性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)内因:___________________ 。
(2)外因:①浓度:_________________________
②温度:________________________________________
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显__________ ,原因是_____________________________ 。多元弱酸酸式盐溶液的酸碱性取决于_____________________________________ ,例如NaHCO3溶液显碱性,原因是_________________ ,_______________________________ (离子方程式和文字说明);
NaHSO3溶液显酸性的原因是________________ ,_____________________ (离子方程式和文字说明)。
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-_______________
(2)外因:①浓度:
②温度:
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显
NaHSO3溶液显酸性的原因是
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O
 CH3COOH+OH-
CH3COOH+OH-| 改变条件 | 平衡移动 | c(CH3COO-) | c(OH-) | 水解 |
| 加入CH3COONa | ||||
| 通入HCl | ||||
| 升温 | ||||
| 加水 | ||||
| 加NaOH | ||||
| 加HAc | ||||
| 加NH4Cl |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】溶液中的化学反应大多是离子反应。根据要求回答问题。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,农业上用石膏降低其碱性的反应原理___________ 。(用化学方程式表示)。
(2)氯化铝水溶液呈酸性的原因是(用离子方程式表示)___________ ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
(3)教材课后习题中介绍了用SOCl2脱水制备无水氯化物的知识。请写出,将SOCl2与AlCl3·6H2O混合加热的化学反应方程式:___________ 。
(4)25℃时,在2.0×10-3mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图。
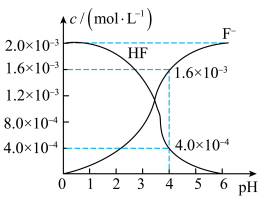
则25℃时,Ka(HF)=___________ 。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,农业上用石膏降低其碱性的反应原理
(2)氯化铝水溶液呈酸性的原因是(用离子方程式表示)
(3)教材课后习题中介绍了用SOCl2脱水制备无水氯化物的知识。请写出,将SOCl2与AlCl3·6H2O混合加热的化学反应方程式:
(4)25℃时,在2.0×10-3mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图。

则25℃时,Ka(HF)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】25℃时,五种酸的电离平衡常数如下:
回答下列问题:
(1)少量的H2SO3溶液和Na2CO3溶液发生反应的离子方程式为___________ ;足量的H2SO3溶液和NaClO 溶液发生反应的离子方程式为___________ 。
(2)亚磷酸(H3PO3)为二元酸,Na2HPO3 是___________ (填“酸式盐” 、“碱式盐”或“正盐”)。H3PO3 的第二级电离方程式为___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO | H2SO3 | H3PO3 亚磷酸 |
| 电离平衡常数 | Ka = 1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka =3.0×10-8 | Ka1=1.6×10-2 Ka2=1.0×10-7 | Ka1=8.3×10-3 Ka2=5.6×10-6 |
(1)少量的H2SO3溶液和Na2CO3溶液发生反应的离子方程式为
(2)亚磷酸(H3PO3)为二元酸,Na2HPO3 是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
(1)根据上表可知,酸性
_____  ,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3
,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3_____ Na2SO3。(填“>” “<”或 “=”,下同)
(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是______ 。
A NaCl溶液 B Na2CO3固体 C NH4Cl溶液 D CH3COONa固体
(3)已知常温下NH3∙H2O的电离常数 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH_______ 7。
(4)将pH=4的 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是_______ ,图中的纵坐标可以是______ 。

a.溶液的pH
b.醋酸的电离平衡常数
c.溶液的导电能力
d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡:
 Ka2
Ka2
 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)
已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈__________ (填“酸性”“碱性”或“中性”);
②溶液中c(Na+)______ c( )(填“>”“<”或“=”);
)(填“>”“<”或“=”);
③写出该溶液中的守恒式:
电荷守恒:_____________ ,物料守恒:________________ ,质子守恒:_______________ 。
| 酸 | 电离平衡常数 |
| 醋酸 | 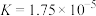 |
| 碳酸 | 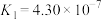 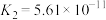 |
| 亚硫酸 |   |
(1)根据上表可知,酸性

 ,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3
,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是
A NaCl溶液 B Na2CO3固体 C NH4Cl溶液 D CH3COONa固体
(3)已知常温下NH3∙H2O的电离常数
 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH(4)将pH=4的
 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是
a.溶液的pH
b.醋酸的电离平衡常数
c.溶液的导电能力
d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。
 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡: Ka2
Ka2 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈
②溶液中c(Na+)
 )(填“>”“<”或“=”);
)(填“>”“<”或“=”);③写出该溶液中的守恒式:
电荷守恒:
您最近一年使用:0次



