按要求回答下列问题。
(1)某浓度的氨水中存在平衡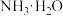

 。如想增大
。如想增大 的浓度而不增大
的浓度而不增大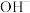 的浓度,应采取的措施是___________(填字母)。
的浓度,应采取的措施是___________(填字母)。
(2)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中
___________ (填“增大”“减小”或“不变”,下同),盐酸中
___________ 。
②加水稀释 倍后,醋酸溶液中的
倍后,醋酸溶液中的
___________ (填“ ”“
”“ ”或“
”或“ ”)盐酸中的
”)盐酸中的 。
。
③加等浓度的 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸
溶液的体积:醋酸___________ (填“ ”“
”“ ”或“
”或“ ”)盐酸。
”)盐酸。
④使温度都升高20℃,溶液中 :醋酸
:醋酸___________ (填“ ”“
”“ ”或“
”或“ ”)盐酸。
”)盐酸。
⑤分别与足量的锌粉发生反应,下列关于氢气体积( )随时间(
)随时间( )变化的示意图正确的是
)变化的示意图正确的是___________ (填字母)。(①表示盐酸,②表示醋酸)
a.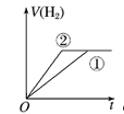 b.
b.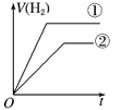 c.
c.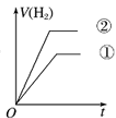 d.
d.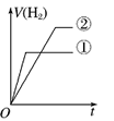
(1)某浓度的氨水中存在平衡
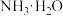

 。如想增大
。如想增大 的浓度而不增大
的浓度而不增大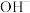 的浓度,应采取的措施是___________(填字母)。
的浓度,应采取的措施是___________(填字母)。| A.适当升高温度 | B.加入 固体 固体 | C.通入 | D.加入少量浓盐酸 |
 相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:①加适量醋酸钠晶体后,醋酸溶液中


②加水稀释
 倍后,醋酸溶液中的
倍后,醋酸溶液中的
 ”“
”“ ”或“
”或“ ”)盐酸中的
”)盐酸中的 。
。③加等浓度的
 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸
溶液的体积:醋酸 ”“
”“ ”或“
”或“ ”)盐酸。
”)盐酸。④使温度都升高20℃,溶液中
 :醋酸
:醋酸 ”“
”“ ”或“
”或“ ”)盐酸。
”)盐酸。⑤分别与足量的锌粉发生反应,下列关于氢气体积(
 )随时间(
)随时间( )变化的示意图正确的是
)变化的示意图正确的是a.
 b.
b. c.
c. d.
d.
更新时间:2021-11-10 15:49:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】一定条件下,在容积为 的密闭容器中发生反应:
的密闭容器中发生反应: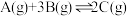 ,开始时加入
,开始时加入 ,在
,在 末测得C的物质的量是
末测得C的物质的量是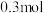 。
。
(1)2min内,用A该反应的平均化学反应速率为_______ 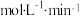 。
。
(2)在 末,B的浓度为
末,B的浓度为_______ 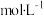 。
。
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”、“减小”或“不变”)。
a.升高温度,化学反应速率_______ ;
b.充入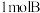 ,化学反应速率
,化学反应速率_______ ;
c.将容器的容积变为 ,化学反应速率
,化学反应速率_______ 。
 的密闭容器中发生反应:
的密闭容器中发生反应: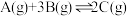 ,开始时加入
,开始时加入 ,在
,在 末测得C的物质的量是
末测得C的物质的量是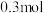 。
。(1)2min内,用A该反应的平均化学反应速率为
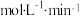 。
。(2)在
 末,B的浓度为
末,B的浓度为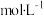 。
。(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”、“减小”或“不变”)。
a.升高温度,化学反应速率
b.充入
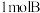 ,化学反应速率
,化学反应速率c.将容器的容积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
【推荐2】工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),下图是使用催化剂和不使用催化剂两种情况下反应过程中的能量变化情况。
CH3OH(g),下图是使用催化剂和不使用催化剂两种情况下反应过程中的能量变化情况。
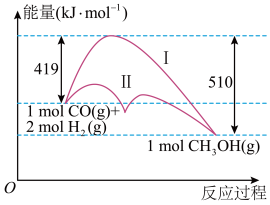
(1)表示使用催化剂的曲线是___________ (填“I”或“II”)。
(2)当反应生成2.5molCH3OH(g)时,反应中___________ (填“吸收”或“放出”)的能量为___________ kJ。
 CH3OH(g),下图是使用催化剂和不使用催化剂两种情况下反应过程中的能量变化情况。
CH3OH(g),下图是使用催化剂和不使用催化剂两种情况下反应过程中的能量变化情况。
(1)表示使用催化剂的曲线是
(2)当反应生成2.5molCH3OH(g)时,反应中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请根据有关知识,填写下列空白:
(1)拆开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3_____ 热量(填“吸收”或“放出”)_____ kJ;事实上,反应的热量总小于理论值,理由是_____ 。
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
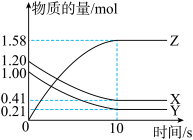
①写出该反应的化学方程式_____ 。
②从开始到10s用Z表示该反应的速率为______ 。
③为加快该反应的反应速率,可采取的措施是_____ 。
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。
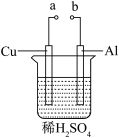
a和b用导线连接,Cu极为原电池______ 极填(“正”或“负”)。Al极发生_____ 填(“氧化”或“还原”)反应。溶液中SO 移向
移向_____ (填“Cu”或“Al”极)。溶液pH_____ (填增大或减小)。
(1)拆开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

①写出该反应的化学方程式
②从开始到10s用Z表示该反应的速率为
③为加快该反应的反应速率,可采取的措施是
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。

a和b用导线连接,Cu极为原电池
 移向
移向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列问题。
(1)25℃,两种酸的电离平衡常数如表。
①正常雨水显酸性的原因是___________ (用离子方程式表示)。
②25℃时某浓度 溶液的pH=5,该溶液中由水电离的
溶液的pH=5,该溶液中由水电离的 与溶液中的
与溶液中的 之比为
之比为___________ 。
③将少量 通入
通入 溶液中反应的离子方程式为
溶液中反应的离子方程式为___________ 。
④结合数据说明 溶液显酸性的原因
溶液显酸性的原因___________ 。
(2)25℃,调节0.10 二元弱酸
二元弱酸 溶液的pH(忽略溶液体积的变化),溶液中的
溶液的pH(忽略溶液体积的变化),溶液中的 、
、 、
、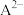 的物质的量分数
的物质的量分数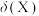 随pH的变化如图所示。[已知:
随pH的变化如图所示。[已知: ]
]

①25℃时, 的电离常数
的电离常数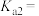
_____ 。
②下列说法不正确的是_____ (填字母序号)。
A.pH=1.2时,
B.对pH=2.7时的溶液升温,pH减小
C.pH增大时, 的值逐渐减小
的值逐渐减小
D. 和
和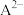 在溶液中能大量共存
在溶液中能大量共存
(1)25℃,两种酸的电离平衡常数如表。
 | 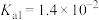 | 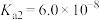 |
 |  |  |
②25℃时某浓度
 溶液的pH=5,该溶液中由水电离的
溶液的pH=5,该溶液中由水电离的 与溶液中的
与溶液中的 之比为
之比为③将少量
 通入
通入 溶液中反应的离子方程式为
溶液中反应的离子方程式为④结合数据说明
 溶液显酸性的原因
溶液显酸性的原因(2)25℃,调节0.10
 二元弱酸
二元弱酸 溶液的pH(忽略溶液体积的变化),溶液中的
溶液的pH(忽略溶液体积的变化),溶液中的 、
、 、
、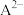 的物质的量分数
的物质的量分数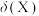 随pH的变化如图所示。[已知:
随pH的变化如图所示。[已知: ]
]
①25℃时,
 的电离常数
的电离常数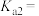
②下列说法不正确的是
A.pH=1.2时,

B.对pH=2.7时的溶液升温,pH减小
C.pH增大时,
 的值逐渐减小
的值逐渐减小D.
 和
和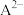 在溶液中能大量共存
在溶液中能大量共存
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常压下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
提示:
(1)温度升高,NH3·H2O的电离平衡向________ (填“左”或“右”)移动,能支持该结论的表中数据是________ (填字母)。
a.电离常数 b.电离度 c.c(OH-) d.c(NH3·H2O)
(2)表中c(OH-)基本不变的原因是__________________________________ 。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是_______ (填字母,下同)。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(4)氨水溶液中,下列做法能使c(NH4+)与c(OH-)比值变大的是________ 。
A.加入固体氯化铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
| 温度/℃ | c(NH3·H2O) /(mol·L-1) | 电离常数 | 电离度/% | c(OH-) /(mol·L-1) |
| 0 | 16.56 | 1.37×10-5 | 9.098 | 1.507×10-2 |
| 10 | 15.16 | 1.57×10-5 | 10.18 | 1.543×10-2 |
| 20 | 13.63 | 1.71×10-5 | 11.2 | 1.527×10-2 |
提示:

(1)温度升高,NH3·H2O的电离平衡向
a.电离常数 b.电离度 c.c(OH-) d.c(NH3·H2O)
(2)表中c(OH-)基本不变的原因是
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(4)氨水溶液中,下列做法能使c(NH4+)与c(OH-)比值变大的是
A.加入固体氯化铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知H2S是一种二元弱酸,回答以下问题:
(1)0.1mol/L NaHS溶液显碱性,则c(S2-)___________ c(H2S)(填“大于” ,“小于” 或“等于” ) 。
(2)已知常温下,CaS饱和溶液中存在平衡:CaS(s) Ca2+(aq)+S2-(aq) ΔH>0。
Ca2+(aq)+S2-(aq) ΔH>0。
①温度升高时,Ksp________ (填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)________ ,原因是__________________________________ (用文字和离子方程式说明)。
(3)若向CaS悬浊液中加入Cu(NO3)2溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式______________ 。
(1)0.1mol/L NaHS溶液显碱性,则c(S2-)
(2)已知常温下,CaS饱和溶液中存在平衡:CaS(s)
 Ca2+(aq)+S2-(aq) ΔH>0。
Ca2+(aq)+S2-(aq) ΔH>0。①温度升高时,Ksp
②滴加少量浓盐酸,c(Ca2+)
(3)若向CaS悬浊液中加入Cu(NO3)2溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式
您最近一年使用:0次



