金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。人们在化工实践中,以富钒炉渣(其中的钒以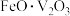 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如图所示。
等)为原料提取金属钒的工艺流程如图所示。

提示:①钒有多种价态,其中+5价最稳定;
② 在碱性条件下可转化为VO
在碱性条件下可转化为VO 。
。
(1)试列举可加快“高温氧化”速率的措施:___________ (填一条)。
(2)“气体Y”和“滤渣1”的化学式分别为___________ 、___________ 。
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为___________ 。
(4)“高温氧化”过程中,若有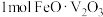 被氧化,则转移的电子数为
被氧化,则转移的电子数为___________ NA。
(5)写出“焙烧”时 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(6)在“高温还原”反应中,氧化钙最终转化为___________ (写化学式)。
(7)用铝热反应也可将 还原为钒,相应的化学方程式为
还原为钒,相应的化学方程式为___________ 。
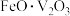 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如图所示。
等)为原料提取金属钒的工艺流程如图所示。
提示:①钒有多种价态,其中+5价最稳定;
②
 在碱性条件下可转化为VO
在碱性条件下可转化为VO 。
。(1)试列举可加快“高温氧化”速率的措施:
(2)“气体Y”和“滤渣1”的化学式分别为
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为
(4)“高温氧化”过程中,若有
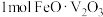 被氧化,则转移的电子数为
被氧化,则转移的电子数为(5)写出“焙烧”时
 发生反应的化学方程式:
发生反应的化学方程式:(6)在“高温还原”反应中,氧化钙最终转化为
(7)用铝热反应也可将
 还原为钒,相应的化学方程式为
还原为钒,相应的化学方程式为
21-22高三上·湖北·阶段练习 查看更多[5]
更新时间:2021-12-21 16:29:19
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeCr2O4,还含有硅、铝等杂质。制备流程如图所示:
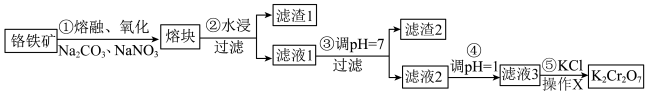
(1) 中Fe为+2价,Cr的化合价为
中Fe为+2价,Cr的化合价为___________ ,步骤①的主要反应为: 
上述反应配平后 与
与 的化学计量数之比为
的化学计量数之比为___________ 。硅、铝等杂质在该步骤变为 、
、 。
。
(2)为了提高步骤②的浸出率,可采取的措施有___________ 。(写两条)
(3)滤渣1主要成分是___________ ,滤渣2的主要成分是___________ 和 。
。
(4)写出步骤④的离子方程式___________ 。该反应的平衡常数 ,滤液③中
,滤液③中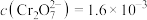 mol⋅L
mol⋅L ,则溶液中
,则溶液中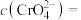
___________ mol⋅L 。
。
(5)向“滤液3”中加入适量KCl,经过操作X后得到 固体。操作X为:
固体。操作X为:___________ ,过滤。有关物质的溶解度如图所示。


(1)
 中Fe为+2价,Cr的化合价为
中Fe为+2价,Cr的化合价为
上述反应配平后
 与
与 的化学计量数之比为
的化学计量数之比为 、
、 。
。(2)为了提高步骤②的浸出率,可采取的措施有
(3)滤渣1主要成分是
 。
。(4)写出步骤④的离子方程式
 ,滤液③中
,滤液③中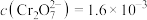 mol⋅L
mol⋅L ,则溶液中
,则溶液中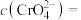
 。
。(5)向“滤液3”中加入适量KCl,经过操作X后得到
 固体。操作X为:
固体。操作X为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
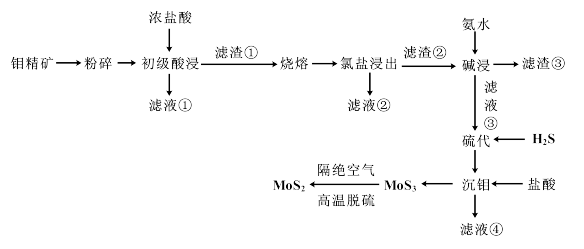
【推荐2】MoS2作为石墨电极的改性剂不仅能弥补石墨低容量的不足,还可以有效解决自身稳定性和导电性不佳的问题。以钼精矿(主要成分为MoS2,含SiO2、CuFeS2、CaCO3、PbS等杂质)为原料生产MoS2的工艺流程如图。
已知:①MoS2中S的化合价为-2价;
②常温下PbCl2不溶于水,但PbCl2可与Cl-反应,生成可溶性络合离子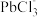 ;
;
③MoS2不溶于水和常见酸碱,“烧熔”时可转化为酸性氧化物MoO3,“硫代”时生成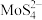 。
。
回答下列问题:
(1)使用浓盐酸进行“初级酸浸”的工艺原理是盐酸与钼精矿中的CaCO3、PbS杂质发生反应,生成CaCl2、PbCl2,其中生成PbCl2的化学方程式为_______ 。
(2)“氯盐浸出”的原理是利用具有强氧化性的FeCl3,在强酸性条件下氧化CuFeS2,使之生成CuCl2和S,该过程的氧化产物与还原产物的物质的量之比为_______ 。
(3)“碱浸”时使用氨水而不使用NaOH溶液的原因是_______ 。
(4)“碱浸”后滤液③的主要成分为_______ (填化学式)。
(5)“初级酸浸”、“碱浸”流程中操作温度不宜过高的原因是_______ 。
(6)产品MoS2中存在极微量的非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+物质的量之比为_______ 。

已知:①MoS2中S的化合价为-2价;
②常温下PbCl2不溶于水,但PbCl2可与Cl-反应,生成可溶性络合离子
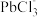 ;
;③MoS2不溶于水和常见酸碱,“烧熔”时可转化为酸性氧化物MoO3,“硫代”时生成
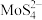 。
。回答下列问题:
(1)使用浓盐酸进行“初级酸浸”的工艺原理是盐酸与钼精矿中的CaCO3、PbS杂质发生反应,生成CaCl2、PbCl2,其中生成PbCl2的化学方程式为
(2)“氯盐浸出”的原理是利用具有强氧化性的FeCl3,在强酸性条件下氧化CuFeS2,使之生成CuCl2和S,该过程的氧化产物与还原产物的物质的量之比为
(3)“碱浸”时使用氨水而不使用NaOH溶液的原因是
(4)“碱浸”后滤液③的主要成分为
(5)“初级酸浸”、“碱浸”流程中操作温度不宜过高的原因是
(6)产品MoS2中存在极微量的非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+物质的量之比为
您最近一年使用:0次
【推荐3】下图中A~J分别代表相关反应的一种物质.已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出.

请填写以下空白:
(1)A的化学式____________ ;
(2)写出反应①②的化学方程式:
①_____________ ,②___________ ;
(3)写出反应③的离子方程式:_______________________ ;
(4)在反应④中,当生成标准状况下2.24 L G时,转移电子数为________ mol。

请填写以下空白:
(1)A的化学式
(2)写出反应①②的化学方程式:
①
(3)写出反应③的离子方程式:
(4)在反应④中,当生成标准状况下2.24 L G时,转移电子数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】2020年5月5日晚18时00分,我国载人空间站货物返回舱试验舱在我国文昌航天发射场点火升空, 5月8日飞船试验船返回舱在东风着陆场预定区域成功着陆,试验取得圆满成功。金属铍(Be)是火箭、航空、宇宙航行的重要材料,工业上以含铍废渣(主要成分是Be和MgF2)为原料制备金属铍的工艺流程如图:

已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有________ 、_______ (任写两项);已知滤液Ⅰ中铍元素的存在形式为H2BeF4,写出“浸出”过程中发生反应的化学方程式:____________ 。
(2)过滤所得滤渣I的主要成分为________ (填化学式)。
(3)该流程中可循环利用的物质是____________________ ;滤渣Ⅱ与浓硫酸发生反应的化学方程式为__________________________________________________ ;已知(NH4)2BeF4易溶于水,且其在水中的溶解度随温度的升高而大幅度增大,从NH4F与滤液Ⅱ发生反应后所得溶液中获得(NH4)2BeF4晶体的“一系列操作”具体是指____________________ 过滤、洗涤、干燥。
(4) “分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为_____________ ;“还原”过程可以用金属镁制备金属铍的原因是__________________________ 。

已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有
(2)过滤所得滤渣I的主要成分为
(3)该流程中可循环利用的物质是
(4) “分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钼(Mo)是一种过渡金属元素,它具有强度高、熔点高、耐腐蚀等优点,被广泛应用于钢铁、石油、化工、电气等领域。钼酸钠晶体(Na2MoO4·2H2O)是一种新型水处理剂。某化学兴趣小组利用废钼催化剂(主要成分为MoS2,含少量Cu2S,FeS2)回收Mo并制备钼酸钠晶体,其主要流程图如图所示:

回答下列问题:
(1)可以提高焙烧效率的措施有____________________________________ (填一条即可),MoS2中的钼元素在空气中焙烧,很容易被氧化成MoO3,若反应中生成0.1molMoO3,反应中转移电子的数目为____________ ;
(2)往固体1中加碳酸钠溶液发生反应的化学方程式为______________________________ ;
(3)操作2为______________________________ ;
(4)制备钼酸钠晶体还可用通过向精制的MoS2中直接加入次氯酸钠溶液与氢氧化钠溶液进行氧化的方法,若氧化过程中,还有硫酸钠生成,则反应的离子方程式为______________ ;
(5)已知钼酸钠溶液中c(MoO42-)=0.40mol•L-1,由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-,当BaMoO4开始沉淀时,CO32-的浓度为__________________ ;[已知:Ksp(BaCO3)=2.6×10-9,Ksp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2 Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为
Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为__________________________________ 。

回答下列问题:
(1)可以提高焙烧效率的措施有
(2)往固体1中加碳酸钠溶液发生反应的化学方程式为
(3)操作2为
(4)制备钼酸钠晶体还可用通过向精制的MoS2中直接加入次氯酸钠溶液与氢氧化钠溶液进行氧化的方法,若氧化过程中,还有硫酸钠生成,则反应的离子方程式为
(5)已知钼酸钠溶液中c(MoO42-)=0.40mol•L-1,由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-,当BaMoO4开始沉淀时,CO32-的浓度为
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2
 Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为
Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
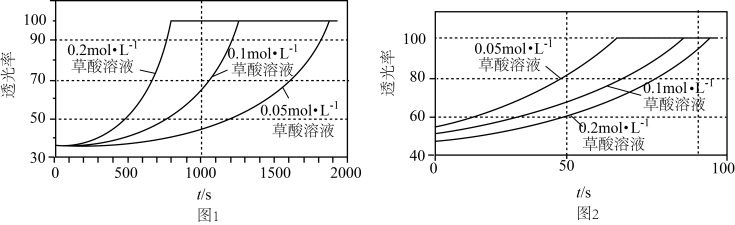
【推荐3】某研究小组为了验证反应物浓度对反应速率的影响,在室温下向2mL0.001mol·L-1KMnO4溶液中分别加入不同浓度的草酸溶液2mL,实验结果如图1;若上述实验中使用的是含20%硫酸的0.001mol·L-1KMnO4溶液,实验结果如图2。回答有关问题:
已知:草酸与高锰酸钾反应的过程可能为:Mn(VII)(VII表示价态,下同) Mn(VI)
Mn(VI) Mn(IV)
Mn(IV) Mn(III)
Mn(III)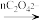 Mn(III)(C2O4)n3-2n2(红色)→Mn(II)+2nCO2
Mn(III)(C2O4)n3-2n2(红色)→Mn(II)+2nCO2
(1)实验时发生总反应的离子方程式为___ 。
(2)由题可知,Mn(II)的作用是___ ;由图2可知,在当前实验条件下,增大草酸的浓度,褪色时间___ (填“变大”、“变小”或“不变”)。
(3)对比图1和图2,该小组同学推测酸化有利于提高该反应的速率。为了验证该推测,设计了系列实验,记录如下(均在室温下进行):
①请完成此实验设计:V5=___ ,V6=___ 。
②设计A号试管实验的目的是___ 。
(4)已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5。
①写出H2C2O4与少量的KOH溶液反应的离子方程式:___ 。
②已知25℃时CH3COOH的电离常数为K=1.75×10-5,则等浓度的草酸溶液和醋酸溶液中,pH较小的是___ 。

已知:草酸与高锰酸钾反应的过程可能为:Mn(VII)(VII表示价态,下同)
 Mn(VI)
Mn(VI) Mn(IV)
Mn(IV) Mn(III)
Mn(III)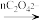 Mn(III)(C2O4)n3-2n2(红色)→Mn(II)+2nCO2
Mn(III)(C2O4)n3-2n2(红色)→Mn(II)+2nCO2(1)实验时发生总反应的离子方程式为
(2)由题可知,Mn(II)的作用是
(3)对比图1和图2,该小组同学推测酸化有利于提高该反应的速率。为了验证该推测,设计了系列实验,记录如下(均在室温下进行):
| 试管编号 | 0.01mol•L-1KMnO4溶液/mL | 0.2mol•L-1 H2C2O4溶液/mL | 蒸馏水/mL | 2.0mol•L-1H2SO4溶液/mL |
| A | 4.0 | 2.0 | 2.0 | 0 |
| B | V1 | V2 | 1.5 | V3 |
| C | V4 | 2.0 | V5 | 1.0 |
| D | V6 | 2.0 | 0 | 2.0 |
①请完成此实验设计:V5=
②设计A号试管实验的目的是
(4)已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5。
①写出H2C2O4与少量的KOH溶液反应的离子方程式:
②已知25℃时CH3COOH的电离常数为K=1.75×10-5,则等浓度的草酸溶液和醋酸溶液中,pH较小的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】某工业矿渣中主要含有Cu2O,还有少部分Al2O3、Fe2O3、SiO2 ,从该矿渣中提取铜的操作流程如下:(已知:Cu2O+2H+═Cu+Cu2++H2O)

(1)固体混合物B与氢氧化钠溶液反应的化学方程式为_______ 。
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是(用涉及反应的离子方程式解释,不必书写Cu2O与盐酸的反应)_______ 、_______ 。检验滤液A中Fe2+的试剂为_______ 。
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为_______(填序号)。
(4)金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程式_______

(1)固体混合物B与氢氧化钠溶液反应的化学方程式为
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是(用涉及反应的离子方程式解释,不必书写Cu2O与盐酸的反应)
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为_______(填序号)。
| A.氢氧化钠溶液 | B.硫酸溶液 | C.氨水 | D.二氧化碳 |
您最近一年使用:0次
【推荐2】某工厂废金属屑的主要成分为Cu、Fe和Al(含有少量Al2O3和Fe2O3)。
I.某化学兴趣小组模拟工业生产设计如图实验流程,用该工厂的废金属屑制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(已知: +CO2+2H2O=Al(OH)3+
+CO2+2H2O=Al(OH)3+ )。
)。

回答下列问题:
(1)化学式:X_______ Y_______
(2)写由操作I中氧化物发生发应的化学方程式_______ 。
II.该小组同学继续对溶液D和制得的绿矾进行实验探究
(3)取溶液D于试管中,滴加几滴KSCN溶液,溶液不变红,为什么?(请用离子方程式解释)_______ 。
(4)取14.0g制得的粗绿矾晶体溶于水,滴加0.10mol/L的酸性高锰酸钾溶液,消耗100mL酸性高锰酸钾溶液,则所制绿矾中铁元素的质量分数为_______ 。
I.某化学兴趣小组模拟工业生产设计如图实验流程,用该工厂的废金属屑制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(已知:
 +CO2+2H2O=Al(OH)3+
+CO2+2H2O=Al(OH)3+ )。
)。
回答下列问题:
(1)化学式:X
(2)写由操作I中氧化物发生发应的化学方程式
II.该小组同学继续对溶液D和制得的绿矾进行实验探究
(3)取溶液D于试管中,滴加几滴KSCN溶液,溶液不变红,为什么?(请用离子方程式解释)
(4)取14.0g制得的粗绿矾晶体溶于水,滴加0.10mol/L的酸性高锰酸钾溶液,消耗100mL酸性高锰酸钾溶液,则所制绿矾中铁元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
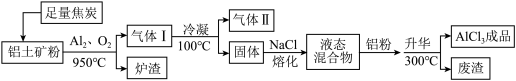
【推荐3】工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
已知:
回答下列问题:
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是______ (只要求写出一种)。
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为_______ 。
(3)气体II的主要成分除了Cl2外,还含有_______ 。气体II常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有_______ 。
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是_______ 。
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl 和Al2Cl
和Al2Cl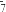 两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为_______ 。

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为
(3)气体II的主要成分除了Cl2外,还含有
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl
 和Al2Cl
和Al2Cl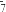 两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
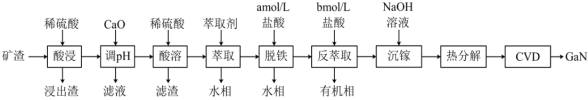
【推荐1】氮化镓(GaN)被称为“终极半导体材料”,工业生产中利用矿渣(主要含铁酸镓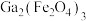 、铁酸锌
、铁酸锌 、
、 )制备GaN的流程如图所示:
)制备GaN的流程如图所示:
已知:①25℃时,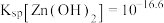 ,
, ,
,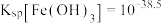 ;
;
②在该工艺条件下 、
、 的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
回答下列问题:
(1)基态Ga原子的核外电子排布式为___________ 。
(2)①“酸浸”时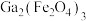 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
②“酸浸”后浸出液中 、
、 浓度分别为
浓度分别为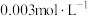 、
、 ,溶液中某离子浓度
,溶液中某离子浓度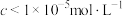 时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为
时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为___________ (忽略溶液体积变化)。
(3)“反萃取”时,所用盐酸的浓度
___________  (选填上表中盐酸的浓度)。
(选填上表中盐酸的浓度)。
(4)①利用CVD(化学气相沉积)技术,将热分解得到的___________ 与 在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物
在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物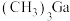 与
与 作为原料,在高温下反应生成GaN,该反应的化学方程式为
作为原料,在高温下反应生成GaN,该反应的化学方程式为___________ 。
(5)GaN的熔点为1700℃,其晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的Ga原子数为___________ 。若晶胞边长为dnm, 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为
___________ 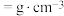 (列出表达式即可)。
(列出表达式即可)。

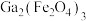 、铁酸锌
、铁酸锌 、
、 )制备GaN的流程如图所示:
)制备GaN的流程如图所示:
已知:①25℃时,
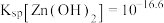 ,
, ,
,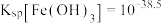 ;
;②在该工艺条件下
 、
、 的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。盐酸浓度/ | 2.0 | 4.0 | 6.0 |
 反萃取率/% 反萃取率/% | 9.4 | 52.1 | 71.3 |
 反萃取率/% 反萃取率/% | 86.9 | 69.1 | 17.5 |
(1)基态Ga原子的核外电子排布式为
(2)①“酸浸”时
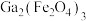 发生反应的离子方程式为
发生反应的离子方程式为②“酸浸”后浸出液中
 、
、 浓度分别为
浓度分别为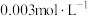 、
、 ,溶液中某离子浓度
,溶液中某离子浓度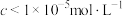 时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为
时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为(3)“反萃取”时,所用盐酸的浓度

 (选填上表中盐酸的浓度)。
(选填上表中盐酸的浓度)。(4)①利用CVD(化学气相沉积)技术,将热分解得到的
 在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物
在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物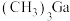 与
与 作为原料,在高温下反应生成GaN,该反应的化学方程式为
作为原料,在高温下反应生成GaN,该反应的化学方程式为(5)GaN的熔点为1700℃,其晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的Ga原子数为
 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为
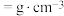 (列出表达式即可)。
(列出表达式即可)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】我国自主发明的“钛战甲”是一种钛合金材料,为实现万米深潜的“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。 是制备钛及其化合物的重要中间体,它为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应。可利用下列装置在实验室制备
是制备钛及其化合物的重要中间体,它为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应。可利用下列装置在实验室制备 (夹持装置略去):
(夹持装置略去):

回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。
(2)装置B中试剂的作用为_______ ,装置C中所盛试剂为_______ 。
(3)先打开装置A中分液漏斗活塞向烧瓶中滴加适量浓盐酸,当观察到_______ 时,再加热装置D中陶瓷管,这样做的目的是_______ 。
(4)冷凝管进水口是_______ (填“a”或“b”)。
(5)装置F中发生反应的离子方程式_______ 。
(6)该实验设计存在的不足之处是_______ 。
 是制备钛及其化合物的重要中间体,它为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应。可利用下列装置在实验室制备
是制备钛及其化合物的重要中间体,它为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应。可利用下列装置在实验室制备 (夹持装置略去):
(夹持装置略去):

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B中试剂的作用为
(3)先打开装置A中分液漏斗活塞向烧瓶中滴加适量浓盐酸,当观察到
(4)冷凝管进水口是
(5)装置F中发生反应的离子方程式
(6)该实验设计存在的不足之处是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】过氧化氢法制备亚氯酸钠(NaClO2)的流程如图1:
已知:①NaClO2常温下稳定,潮湿的NaClO2加热到130℃分解。
②ClO2气体在碱性溶液中会转化为ClO 和ClO
和ClO 。
。
(1)制备ClO2气体的化学方程式为_______ 。
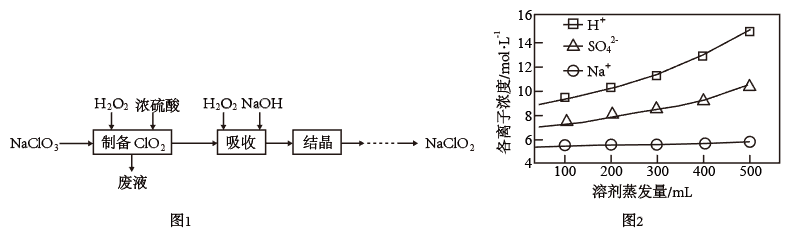
(2)取1L废液,蒸发结晶,测定不同蒸发量下,残留液中各离子的浓度如图2,则析出的晶体为_______ (填化学式)。
(3)吸收时的主要反应为2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O。
①吸收时,需控制反应温度为3℃,可采取的措施为_______ 。
②温度过高,产品的纯度会降低,主要原因是_______ 。
(4)从NaClO2溶液获得产品的可行措施有_______ (填序号)。
a.减压蒸发 b.溶液雾状喷出干燥 c.300℃热空气烘干
(5)准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知ClO +4I-+4H+=2H2O+2I2+Cl-)。取所得混合液的1/10于锥形瓶中,加几滴淀粉溶液,用cmol•L-lNa2S2O3标准液滴定,重复3次,测得平均消耗标准液VmL(已知I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-)。取所得混合液的1/10于锥形瓶中,加几滴淀粉溶液,用cmol•L-lNa2S2O3标准液滴定,重复3次,测得平均消耗标准液VmL(已知I2+2S2O =2I-+S4O
=2I-+S4O ),该样品中NaClO2的纯度为
),该样品中NaClO2的纯度为_______ (用含m、c、V的代数式表示)。

已知:①NaClO2常温下稳定,潮湿的NaClO2加热到130℃分解。
②ClO2气体在碱性溶液中会转化为ClO
 和ClO
和ClO 。
。(1)制备ClO2气体的化学方程式为
(2)取1L废液,蒸发结晶,测定不同蒸发量下,残留液中各离子的浓度如图2,则析出的晶体为
(3)吸收时的主要反应为2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O。
①吸收时,需控制反应温度为3℃,可采取的措施为
②温度过高,产品的纯度会降低,主要原因是
(4)从NaClO2溶液获得产品的可行措施有
a.减压蒸发 b.溶液雾状喷出干燥 c.300℃热空气烘干
(5)准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知ClO
 +4I-+4H+=2H2O+2I2+Cl-)。取所得混合液的1/10于锥形瓶中,加几滴淀粉溶液,用cmol•L-lNa2S2O3标准液滴定,重复3次,测得平均消耗标准液VmL(已知I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-)。取所得混合液的1/10于锥形瓶中,加几滴淀粉溶液,用cmol•L-lNa2S2O3标准液滴定,重复3次,测得平均消耗标准液VmL(已知I2+2S2O =2I-+S4O
=2I-+S4O ),该样品中NaClO2的纯度为
),该样品中NaClO2的纯度为
您最近一年使用:0次



