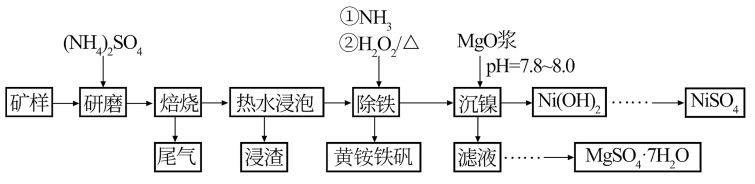
镍及其化合物在工业上有广泛应用,红土镍矿是镍资源的主要来源。以某地红土镍矿[主要成分Mg3Si2O5(OH)4、Fe2MgO4、NiO、FeO、Fe2O3]为原料,采用硫酸铵焙烧法选择性提取镍,可减少其他金属杂质浸出,工艺流程如图所示。
已知:①2[Mg3Si2O5(OH)4]+9(NH4)2SO4 3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
②2Fe2MgO4+15(NH4)2SO4 (NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
(NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
③常温下,NiSO4易溶于水,NiOOH不溶于水。
(1)“焙烧”前将“矿样”与(NH4)2SO4混合研磨的目的是___________ 。
(2)经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与(NH4)2SO4反应生成Fe2(SO4)3,该反应的化学方程式为___________ ,“浸渣"的主要成分除铁的氧化物外还有___________ (填化学式)。
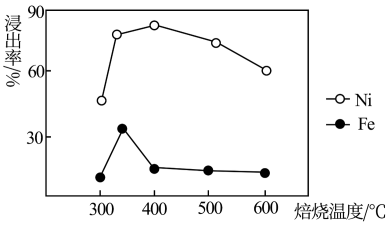
(3)焙烧温度对浸出率的影响如图所示,最佳焙烧温度是___________(填序号)左右。
(4)若残留在浸出液中的铁完全转化为黄铵铁矾除去,“除铁”时通入NH3调节溶液pH的范围是___________ 。该工艺条件下,Ni2+生成Ni(OH)2沉淀,Fe3+生成Fe(OH)3或黄铵铁矾沉淀定,开始沉淀和沉淀完全时的pH如下表:
(5)“沉镍"时pH调为8.0,滤液中Ni2+浓度约为___________ mol/L(100.4≈2.5)。
(6)流程中___________ (填化学式)可循环使用,减少污染。
(7)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式是___________ 。

已知:①2[Mg3Si2O5(OH)4]+9(NH4)2SO4
 3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;②2Fe2MgO4+15(NH4)2SO4
 (NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
(NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑③常温下,NiSO4易溶于水,NiOOH不溶于水。
(1)“焙烧”前将“矿样”与(NH4)2SO4混合研磨的目的是
(2)经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与(NH4)2SO4反应生成Fe2(SO4)3,该反应的化学方程式为
(3)焙烧温度对浸出率的影响如图所示,最佳焙烧温度是___________(填序号)左右。

| A.300℃ | B.350℃ | C.400℃ | D.600℃ |
| 沉淀物 | Ni(OH)2 | Fe(OH)3 | 黄铵铁矾 |
| 开始沉淀时的pH | 7.1 | 2.7 | 1.3 |
| 沉淀完全(c=1×10-5 mol/L)时的pH | 9.2 | 3.7 | 2.3 |
(5)“沉镍"时pH调为8.0,滤液中Ni2+浓度约为
(6)流程中
(7)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式是
2021·云南·一模 查看更多[5]
云南省2021-2022学年高三上学期“3+3+3”高考备考诊断性联考(一)理科综合化学试题宁夏吴忠市2022届高三4月模拟联考(二模)理科综合化学试题(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用) 山东省青岛第二中学2022-2023学年高三上学期第二次月考化学试题
更新时间:2022-01-03 23:49:47
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硫酸镍主要用于电镀、电池、催化剂、印染媒染剂、金属着色剂等领域。以主要成分为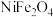 、NiO(杂质为FeO、CaO、
、NiO(杂质为FeO、CaO、 )的矿渣为原料制备
)的矿渣为原料制备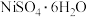 的流程如图所示(已知:镍的+2价状态很稳定):
的流程如图所示(已知:镍的+2价状态很稳定):

回答下列问题:
(1)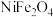 中铁元素的化合价是
中铁元素的化合价是___________ 价;研磨的作用是___________ 。
(2)“焙烧”中FeO会转化为 ,相应的化学方程式为
,相应的化学方程式为___________ ,滤渣1中含有 、
、___________ (填化学式)、 等;“操作X”具体是指
等;“操作X”具体是指___________ 、过滤、洗涤、干燥。
(3)萃取原理可表示为: (水相)+nRH(有机相)
(水相)+nRH(有机相)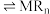 (有机相)+
(有机相)+ (水相)(
(水相)( 为
为 、
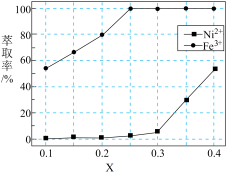
、 )。已知:萃取剂RH的用量对萃取率有影响,RH的体积与被萃取液体积的倍数(X)和萃取率关系如图所示,则X的最佳值为
)。已知:萃取剂RH的用量对萃取率有影响,RH的体积与被萃取液体积的倍数(X)和萃取率关系如图所示,则X的最佳值为___________ ,Y为___________ 试剂(填“强碱性”“强酸性”或“中性”);若矿渣中镍元素含量为a g,萃取前镍的损失率为b,萃取后镍的损失率忽略不计,最终得到c g 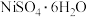 ,则在X取最佳值时,
,则在X取最佳值时, 的萃取率为
的萃取率为___________ (用含a、b、c的代数式表示)。
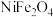 、NiO(杂质为FeO、CaO、
、NiO(杂质为FeO、CaO、 )的矿渣为原料制备
)的矿渣为原料制备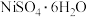 的流程如图所示(已知:镍的+2价状态很稳定):
的流程如图所示(已知:镍的+2价状态很稳定):
回答下列问题:
(1)
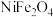 中铁元素的化合价是
中铁元素的化合价是(2)“焙烧”中FeO会转化为
 ,相应的化学方程式为
,相应的化学方程式为 、
、 等;“操作X”具体是指
等;“操作X”具体是指(3)萃取原理可表示为:
 (水相)+nRH(有机相)
(水相)+nRH(有机相)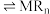 (有机相)+
(有机相)+ (水相)(
(水相)( 为
为 、
、 )。已知:萃取剂RH的用量对萃取率有影响,RH的体积与被萃取液体积的倍数(X)和萃取率关系如图所示,则X的最佳值为
)。已知:萃取剂RH的用量对萃取率有影响,RH的体积与被萃取液体积的倍数(X)和萃取率关系如图所示,则X的最佳值为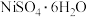 ,则在X取最佳值时,
,则在X取最佳值时, 的萃取率为
的萃取率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】二氧化钛是目前使用最广泛的白色颜料。工业上,以钛铁矿(主要成分为钛酸亚铁[FeTiO3],含有少量SiO2杂质)为原料制备二氧化钛的过程如下图所示。
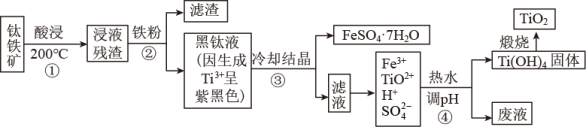
已知:①超过70℃TiO2+易水解;低于0℃ FeSO4·7H2O大量结晶。
②钛的化合价主要有+4价和+3价,其中Ti3+(紫黑色)还原性比Fe2+强
③有关氢氧化物开始沉淀的pH如下:
根据相关信息回答下列问题;
(1)酸浸过程选用的酸是__________ 。
(2)步骤①中生成Fe2+和TiO2+的化学反应方程式为__________ 。
(3)以下相关描述正确的是__________ 。
A 步骤②中加入铁粉,在防止Fe2+转化成Fe3+的同时也将部分TiO2+氧化成了Ti3+
B 步骤③中的降温结晶过程可以选择冰水混合物
C ③中发生了反应Fe3++ Ti3++H2O== Fe2++ TiO2++2H+
D 废液成分中有硫酸,可以循环利用
(4)步④中生成Ti(OH)4的离子方程式为__________ ,选择的pH范围是__________ 。
(5)证明步骤④中Ti (OH)4固体已经洗涤干净的方法是__________ 。
(6)钛酸锂(Li4Ti5O12)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池总反应式为:LiXO2(s)+Li4Ti5O12(s)=Li1-aXO2+Li4+aTi5O12(s),则其负极反应式为__________ 。

已知:①超过70℃TiO2+易水解;低于0℃ FeSO4·7H2O大量结晶。
②钛的化合价主要有+4价和+3价,其中Ti3+(紫黑色)还原性比Fe2+强
③有关氢氧化物开始沉淀的pH如下:
| 氢氧化物 | Ti(OH)4 | Ti(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀时的pH | 0.5 | 3.0 | 1.5 | 7.6 |
根据相关信息回答下列问题;
(1)酸浸过程选用的酸是
(2)步骤①中生成Fe2+和TiO2+的化学反应方程式为
(3)以下相关描述正确的是
A 步骤②中加入铁粉,在防止Fe2+转化成Fe3+的同时也将部分TiO2+氧化成了Ti3+
B 步骤③中的降温结晶过程可以选择冰水混合物
C ③中发生了反应Fe3++ Ti3++H2O== Fe2++ TiO2++2H+
D 废液成分中有硫酸,可以循环利用
(4)步④中生成Ti(OH)4的离子方程式为
(5)证明步骤④中Ti (OH)4固体已经洗涤干净的方法是
(6)钛酸锂(Li4Ti5O12)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池总反应式为:LiXO2(s)+Li4Ti5O12(s)=Li1-aXO2+Li4+aTi5O12(s),则其负极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,如图为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
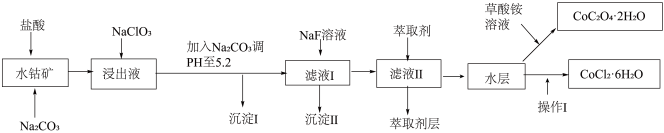
已知:①过滤后的浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;
②沉淀I中只含有两种沉淀;
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中Co2O3发生反应的离子反应方程式为_______ 。
(2)NaClO3在浸出液中的作用_______ 。
(3)加入Na2CO3调pH至5.2,目的是_______ ;萃取剂层含锰元素,则沉淀II的主要成分为MgF2和______ 。

已知:①过滤后的浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;
②沉淀I中只含有两种沉淀;
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3在浸出液中的作用
(3)加入Na2CO3调pH至5.2,目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮氧化物会造成环境污染,我国科学家正着力研究SCR技术(NH3选择性催化还原氮氧化物)对燃煤电厂烟气进行脱硝处理。
(1)写出一种氮氧化物直接排放到空气中造成的环境危害___________ 。
(2)NH3催化还原NO的化学方程式为___________ 。
(3)铁基催化剂在260~300℃范围内实现SCR技术的过程如下:
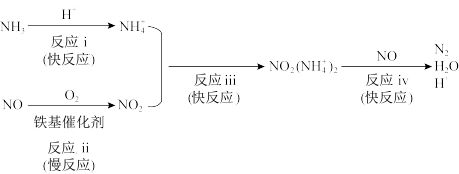
①适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:___________ 。
②向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
 与NO发生反应
与NO发生反应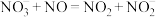 ;
;
 与
与 发生反应ⅲ和反应ⅳ转化为N2;
发生反应ⅲ和反应ⅳ转化为N2;
 与
与 发生反应
发生反应___________ (填离子方程式)转化为N2。
(4)相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的 会明显降低NO脱除率。
会明显降低NO脱除率。
①推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是___________ 。
②持续通入含SO2的烟气。不同温度下,每隔1h测定NO脱除率,结果如下:

相同时间,200℃时NO脱除率低于100℃,原因是___________ 。
(1)写出一种氮氧化物直接排放到空气中造成的环境危害
(2)NH3催化还原NO的化学方程式为
(3)铁基催化剂在260~300℃范围内实现SCR技术的过程如下:

①适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:
②向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
 与NO发生反应
与NO发生反应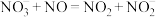 ;
; 与
与 发生反应ⅲ和反应ⅳ转化为N2;
发生反应ⅲ和反应ⅳ转化为N2; 与
与 发生反应
发生反应(4)相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的
 会明显降低NO脱除率。
会明显降低NO脱除率。①推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是
②持续通入含SO2的烟气。不同温度下,每隔1h测定NO脱除率,结果如下:

相同时间,200℃时NO脱除率低于100℃,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。“CuCl-H2O热电循环制氢”经过溶解、电解、热水解和热分解四个步骤,其过程如图所示。
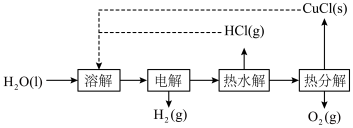
已知:电解池的阳极区为酸性 溶液,阴极区为盐酸,电解过程中
溶液,阴极区为盐酸,电解过程中 转化为
转化为 。
。
(1)分析过程图知,CuCl为制氢总过程中的_______ ,它在制氢过程中的作用是降低该反应的_______ ,加快反应速率。
(2)电解时,阳极的电极反应式为_______ 。
(3) 中基态Cu+的电子排布式为
中基态Cu+的电子排布式为_______ ,其核外电子的空间运动状态有_______ 种。
(4) 中含有配位键,其中提供空轨道的离子为
中含有配位键,其中提供空轨道的离子为_______ 。
(5)H2、O2在水中的溶解度较小,而HCl溶解度却很大的原因是_______ 。

已知:电解池的阳极区为酸性
 溶液,阴极区为盐酸,电解过程中
溶液,阴极区为盐酸,电解过程中 转化为
转化为 。
。(1)分析过程图知,CuCl为制氢总过程中的
(2)电解时,阳极的电极反应式为
(3)
 中基态Cu+的电子排布式为
中基态Cu+的电子排布式为(4)
 中含有配位键,其中提供空轨道的离子为
中含有配位键,其中提供空轨道的离子为(5)H2、O2在水中的溶解度较小,而HCl溶解度却很大的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】2019年10月1日,我国成功举办国庆七十周年阅兵活动。其中阅兵仪式上混合动力车等新能源车辆的亮相,展示了综合国力、国防科技发展水平。同时也说明能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(ii)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)制备合成气:工业生产中为解决合成气中H2过量而 CO 不足的问题,原料气中需添加CO2,发生的反应(iii):CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH= +41.17kJ•mol-1,为了使合成气配比最佳,理论上原料气中二氧化碳与甲烷质量比为_______ 。
(2)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①请写出二氧化碳加氢合成水蒸气和甲醇的热化学方程式____________ 。
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示:
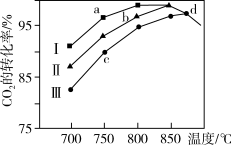
a~d 点中反应一定处于平衡状态的点是____ ;CO2的转化率 a 点比 c 点高的原因是 ____ 。
③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
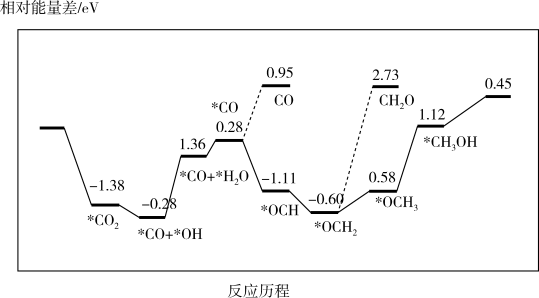
容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为___ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中____ (填字母)的能量变化。
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3D.*OCH3→*CH3OH
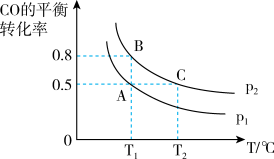
(3)在一容积可变的密闭容器中充入10molCO和20molH2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①比较A、B 两点压强大小PA_______ PB填“>、<、 =”)
②若达到化学平衡状态 A 时,容器的体积为 10 L,如果反应开始时仍充入 10molCO和20molH2,则在平衡状态 B 时,容器的体积V(B)=_______ L;
工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(ii)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)制备合成气:工业生产中为解决合成气中H2过量而 CO 不足的问题,原料气中需添加CO2,发生的反应(iii):CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH= +41.17kJ•mol-1,为了使合成气配比最佳,理论上原料气中二氧化碳与甲烷质量比为
(2)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①请写出二氧化碳加氢合成水蒸气和甲醇的热化学方程式
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示:


a~d 点中反应一定处于平衡状态的点是
③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3D.*OCH3→*CH3OH
(3)在一容积可变的密闭容器中充入10molCO和20molH2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①比较A、B 两点压强大小PA
②若达到化学平衡状态 A 时,容器的体积为 10 L,如果反应开始时仍充入 10molCO和20molH2,则在平衡状态 B 时,容器的体积V(B)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
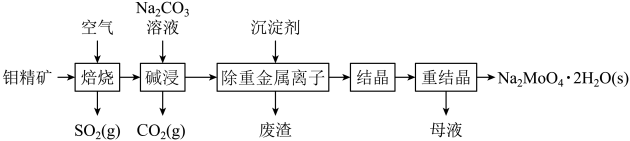
(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是___ ,焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ)。
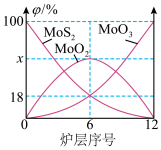
①x=___ 。
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:___ 。
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是___ 。
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是___ %[已知:Ksp(BaCO3)=1×10-9,Ksp(BaMoO4)=4.0×10-8,溶液体积变化忽略不计]。
(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是___ 。
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是___ (填选项字母)。
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸

(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是

①x=
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸
您最近一年使用:0次
【推荐2】碱式氧化镍(NiOOH)可作镍电池的正极材料,现用某废镍原料(主要含Ni、Al、SiO2,少量Cr、FeS等)来制备,其工艺流程如图:

回答下列问题:
(1)“碱浸”时,发生反应的离子反应方程式①___ ,②___ 。
(2)在酸性溶液中 可以转化成
可以转化成 ,用离子方程式表示该转化反应
,用离子方程式表示该转化反应___ ,已知BaCrO4的Ksp=1.2×10-10,要使溶液中 沉淀完全(c(
沉淀完全(c( )≤1×10-5 mol·L-1),溶液中钡离子浓度至少为
)≤1×10-5 mol·L-1),溶液中钡离子浓度至少为___ mol·L-1。

回答下列问题:
(1)“碱浸”时,发生反应的离子反应方程式①
(2)在酸性溶液中
 可以转化成
可以转化成 ,用离子方程式表示该转化反应
,用离子方程式表示该转化反应 沉淀完全(c(
沉淀完全(c( )≤1×10-5 mol·L-1),溶液中钡离子浓度至少为
)≤1×10-5 mol·L-1),溶液中钡离子浓度至少为
您最近一年使用:0次
【推荐3】铅及其化合物在工业生产及日常生活中有非常广泛的用途。
(1)工业上可用PbS与PbSO4反应制备粗铅,反应为PbS+PbSO4 2Pb+2SO2↑。
2Pb+2SO2↑。
已知下列反应的热化学方程式:
Ⅰ.2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH1=a kJ·mol-1
Ⅱ.PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH2= b kJ·mol-1
Ⅲ.PbS(s)+2O2(g)=PbSO4(s) ΔH3=c kJ·mol-1
①反应PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH=_______ (用含a,b,c的代数式表示)。
②反应Ⅲ在一定条件下能自发进行的原因是_______ 。
(2)工业上可通过电解将粗铅精炼,电解液为H2SiF6和PbSiF6的混合溶液。电解时,当c(H2SiF6)过大时,铅产率减小的原因可能是_______ 。(已知:H2SiF6和PbSiF6均为易溶子水的强电解质。)
(3)铅易造成环境污染,水溶液中铅的存在形态与pH关系如图1所示。
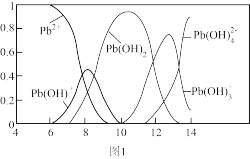
①常温下,向pH=10的含Pb(II)废水滴加氨水至pH=11时,所发生反应的离子方程式为_______ 。
②某工业含有Pb2+的废水,经处理后c(Pb2+)=2×l0-6 mol·L-1,达到排放标准,此溶液的pH不低于_______ 。(已知室温下:Ksp[Pb(OH)2]=2×10-l5)
(4)我国科学家在一种铅的卤化物光电材料中引入稀土铕(Eu3+)盐,可以提升太阳能电池的效率和使用寿命,其作用原理如图2所示。该过程可描述为_______ 。

(1)工业上可用PbS与PbSO4反应制备粗铅,反应为PbS+PbSO4
 2Pb+2SO2↑。
2Pb+2SO2↑。已知下列反应的热化学方程式:
Ⅰ.2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH1=a kJ·mol-1
Ⅱ.PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH2= b kJ·mol-1
Ⅲ.PbS(s)+2O2(g)=PbSO4(s) ΔH3=c kJ·mol-1
①反应PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH=
②反应Ⅲ在一定条件下能自发进行的原因是
(2)工业上可通过电解将粗铅精炼,电解液为H2SiF6和PbSiF6的混合溶液。电解时,当c(H2SiF6)过大时,铅产率减小的原因可能是
(3)铅易造成环境污染,水溶液中铅的存在形态与pH关系如图1所示。

①常温下,向pH=10的含Pb(II)废水滴加氨水至pH=11时,所发生反应的离子方程式为
②某工业含有Pb2+的废水,经处理后c(Pb2+)=2×l0-6 mol·L-1,达到排放标准,此溶液的pH不低于
(4)我国科学家在一种铅的卤化物光电材料中引入稀土铕(Eu3+)盐,可以提升太阳能电池的效率和使用寿命,其作用原理如图2所示。该过程可描述为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】三氯化钪( )可用于制高熔点合金,易溶于水,难溶于无水乙醇,由水溶液中结晶时得六水合物(受热时部分脱氯化氢生成难溶性的氧氯化钪)。制备三氯化钪的装置如图所示。
)可用于制高熔点合金,易溶于水,难溶于无水乙醇,由水溶液中结晶时得六水合物(受热时部分脱氯化氢生成难溶性的氧氯化钪)。制备三氯化钪的装置如图所示。

请回答下列问题:
(1)装置丙中仪器X的名称是_______ 。
(2)装置戊中试剂Y是_______ 。
(3)装置丙中反应的离子方程式是_______ 。
(4)按气流由左至右的顺序,写出装置中各字母接口的连接顺序:e_______ 。
(5)装置甲发生的反应还生成了一种能与血红蛋白结合的有毒气体,写出该反应的化学方程式:_______ ;装置丁的作用是_______ 。
 )可用于制高熔点合金,易溶于水,难溶于无水乙醇,由水溶液中结晶时得六水合物(受热时部分脱氯化氢生成难溶性的氧氯化钪)。制备三氯化钪的装置如图所示。
)可用于制高熔点合金,易溶于水,难溶于无水乙醇,由水溶液中结晶时得六水合物(受热时部分脱氯化氢生成难溶性的氧氯化钪)。制备三氯化钪的装置如图所示。
请回答下列问题:
(1)装置丙中仪器X的名称是
(2)装置戊中试剂Y是
(3)装置丙中反应的离子方程式是
(4)按气流由左至右的顺序,写出装置中各字母接口的连接顺序:e
(5)装置甲发生的反应还生成了一种能与血红蛋白结合的有毒气体,写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用含钴废料(主要成分是Co3O4,还含有Fe、Al、Cu等杂质)为原料回收复合氧化钴的流程如图所示:

(1)“碱溶”所得的溶液中含有的阴离子为___________ 。
(2)“氧化”:加热搅拌条件下加入NaClO3的作用是___________ 。
(3)“除铁”:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式___________ 。
(4)溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10−5 mol∙L−1],控制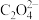 的浓度不小于
的浓度不小于___________ 。(已知:Ksp(CoC2O4)=6.3×10−8)
(5)称取2.940g CoC2O4,在空气中灼烧得1.740g复合氧化钴,则复合氧化钴的化学式为___________ 。

(1)“碱溶”所得的溶液中含有的阴离子为
(2)“氧化”:加热搅拌条件下加入NaClO3的作用是
(3)“除铁”:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式
(4)溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10−5 mol∙L−1],控制
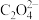 的浓度不小于
的浓度不小于(5)称取2.940g CoC2O4,在空气中灼烧得1.740g复合氧化钴,则复合氧化钴的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】用如图所示装置进行实验(夹持仪器省略)。将液体A逐滴加入到固体B中,回答下列问题:
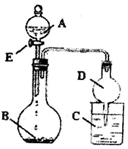
(1)图中D装置在实验中的作用是__________________________________ 。
(2)若A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中的现象为_________________________ ,C中发生反应的化学方程式为 __________________________________________________ 。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现象是_____________________ ;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的化学方程式 ___________________________________ 。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是______________________________ ,C中发生反应的离子方程式为_____________________________________________ 。
(5)常温下,NH4++ H2O NH3·H2O+ H+的化学平衡常数为5×10–10,则NH3·H2O的电离平衡常数K =
NH3·H2O+ H+的化学平衡常数为5×10–10,则NH3·H2O的电离平衡常数K = ____________ 。

(1)图中D装置在实验中的作用是
(2)若A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中的现象为
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现象是
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是
(5)常温下,NH4++ H2O
 NH3·H2O+ H+的化学平衡常数为5×10–10,则NH3·H2O的电离平衡常数K =
NH3·H2O+ H+的化学平衡常数为5×10–10,则NH3·H2O的电离平衡常数K =
您最近一年使用:0次



