研究化学反应中的能量变化具有重要意义。下列说法正确的是
| A.汽车尾气净化器中的反应为2NO(g)+2CO(g)=N2(g)+2CO2(g),该反应在一定条件下能自发进行,说明该反应的ΔH>0 |
B.已知反应2NO2(g) N2O4(g)ΔH<0,升高温度,v逆增大,v正减小,平衡逆向移动 N2O4(g)ΔH<0,升高温度,v逆增大,v正减小,平衡逆向移动 |
| C.C2H5OH(l)的燃烧热的热化学方程式为2C2H5OH(l)+6O2(g)=4CO2(g)+6H2O(g)ΔH=-1367.0kJ·mol-1 |
D.已知:500°C、30MPa下,N2(g)+3H2(g) 2NH3(g)ΔH=-92.4kJ·mol-1将0.5mol N2和2mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ 2NH3(g)ΔH=-92.4kJ·mol-1将0.5mol N2和2mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ |
更新时间:2022-01-15 17:24:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列热化学方程式正确的是
A.已知1 g甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ: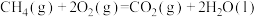  kJ⋅mol-1 kJ⋅mol-1 |
B.12g碳与适量水蒸气反应生成一氧化碳和氢气,需吸收120 kJ的热量:  kJ⋅mol-1 kJ⋅mol-1 |
C.通常状况下,将1g氢气在氯气中完全燃烧,放出92.4 kJ热量: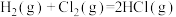  kJ⋅mol-1 kJ⋅mol-1 |
D.已知充分燃烧a g乙炔气体生成1 mol二氧化碳气体和液态水,放出b kJ热量:  kJ⋅mol-1 kJ⋅mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮及其化合物的转化过程如图甲所示,其中图乙为反应①过程中能量变化的曲线图。下列分析合理的是


A. 的电子式为 的电子式为 |
B.反应①的热化学方程式为  |
| C.傕化剂a、b能提高反应①、②的化学反应速率和平衡转化率 |
D.反应②中生成 时转移的电子数为 时转移的电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
A.在一定条件下,将1mol SO2(g)和0.5mol O2(g)置于密闭容器中充分反应生成SO3(g),放出热量79.2kJ,该反应的热化学方程式为 2SO2(g)+O2(g) 2SO3(g) ΔH=-158.4kJ·mol-1 2SO3(g) ΔH=-158.4kJ·mol-1 |
| B.葡萄糖的燃烧热为2800 kJ·mol-1,则C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH=2800 kJ·mol-1 |
| C.已知HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则稀硫酸与氢氧化钠溶液反应生成1mol水时ΔH=-57.3 kJ·mol-1 |
| D.已知稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则稀氨水与稀盐酸反应生成1mol水时放出57.3kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热△H=-57.3 kJ·mol-1,则1 mol硫酸与足量氢氧化钡溶液反应放热为114.6 kJ |
| B.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(1)=2H2(g)+O2(g)反应的△H=+571.6kJ·mol-1 |
| C.反应物的热效应与是否使用催化剂有关 |
| D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g) + 3H2(g) ⇌ 2NH3(g) △H= -38.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.同温同压下,H2(g)+ Cl2(g)=2HCl(g)在光照和点燃条件的△H相同 |
B.500 ℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g), 放热 akJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H= -2a kJ•mol-1 2NH3(g) △H= -2a kJ•mol-1 |
| C.甲烷的标准燃烧热(△H)为-890.3 kJ • mol -1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g) =CO2(g) +2H2O(g) △H=-890.3kJ•mol-1 |
| D.HCl和NaOH反应的中和热△H= -57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3) kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列依据热化学方程式得出的结论正确的是( )
| A.已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H= -483.6kJ•mol-1,则氢气的标准燃烧热为241.8kJ•mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)=2CO(g)△H=b kJ•mol-1,则a>b |
| D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0gNaOH的稀溶液与浓硫酸完全中和,放出大于57.3kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列外界条件的改变,肯定不影响化学反应的平衡状态的是
| A.反应物浓度 | B.反应温度 | C.体系压强 | D.使用催化剂 |
您最近一年使用:0次
【推荐2】对反应aA(g) bB(g)+cC(g),向密闭容器中充入1molA,达平衡时,体系中B的体积分数随温度、压强的变化关系如图所示,下列判断正确的是
bB(g)+cC(g),向密闭容器中充入1molA,达平衡时,体系中B的体积分数随温度、压强的变化关系如图所示,下列判断正确的是

 bB(g)+cC(g),向密闭容器中充入1molA,达平衡时,体系中B的体积分数随温度、压强的变化关系如图所示,下列判断正确的是
bB(g)+cC(g),向密闭容器中充入1molA,达平衡时,体系中B的体积分数随温度、压强的变化关系如图所示,下列判断正确的是
| A.ΔH<0,且M、N两点的化学平衡常数:M>N |
| B.a<b+c且ΔS<0 |
| C.M、N两点A的转化率:M<N |
| D.保持恒温恒容,向P点再充入少量A,达新平衡时B%减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应的方向及判据的说法不正确的是
| A.能自发进行的反应一定是熵增的过程 |
B. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
| C.焓变或熵变不可以单独作为反应自发性的判据 |
| D.冰在室温下自动融化成水,体系混乱度增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中正确的是
| A.能自发进行的化学反应不一定就能发生 |
B. 在室温下不能自发进行,则该反应的 在室温下不能自发进行,则该反应的 |
C.若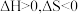 ,化学反应在任何温度下都能自发进行 ,化学反应在任何温度下都能自发进行 |
| D.加入合适的催化剂能降低反应的活化能,从而改变反应的焓变 |
您最近一年使用:0次


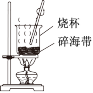


 和
和 制取尿素
制取尿素 ,有关反应的热化学方程式如下:
,有关反应的热化学方程式如下: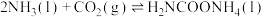
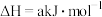
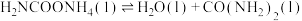
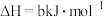
 的
的