向含有AgI固体的饱和溶液中:
(1)加入固体AgNO3,则c(I-)___________ (填“变大”、“变小”或“不变”,下同)。
(2)若改加更多的AgI,则c(Ag+)将___________ 。
(3)若改加AgBr固体,则c(I-)___________ ,而c(Ag+)___________ 。
(1)加入固体AgNO3,则c(I-)
(2)若改加更多的AgI,则c(Ag+)将
(3)若改加AgBr固体,则c(I-)
2021高二·全国·专题练习 查看更多[1]
(已下线)3.4.1 沉淀溶解平衡原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
更新时间:2022-01-18 19:33:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知温度越高,AgI在水中的溶解度越大,现向有AgI固体的AgI饱和溶液中分别进行如下操作,有关离子浓度的变化情况是:
(1)若加入少量水,则c(I-)_______ (填“增大”、“减小”或“不变”)
(2)若加入AgNO3固体,则AgI在水中的溶解度_______ (填“增大”、“减小”或“不变”)
(3)若加入NaCl固体,则AgI的溶度积Ksp_______ (填“增大”、“减小”或“不变”)
(4)若某温度下,AgI的溶度积Ksp=9.0×10-20,则AgI在该温度下的溶解度是_______ (AgI饱和溶液的密度可近似为1g·mL-1)。
(1)若加入少量水,则c(I-)
(2)若加入AgNO3固体,则AgI在水中的溶解度
(3)若加入NaCl固体,则AgI的溶度积Ksp
(4)若某温度下,AgI的溶度积Ksp=9.0×10-20,则AgI在该温度下的溶解度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列盐的三大守恒:
(1)Na2C2O4溶液中,1电荷守恒___________ 。2物料守恒___________ 。3质子守恒___________ 。
(2)Na2CO3溶液中,1电荷守恒___________ 。2物料守恒___________ 。3质子守恒___________ 。
(3)将足量的AgCl(s)分别添加到下述四种溶液中,所得溶液c(Ag+)由大到小的顺序是___________ 。
A.10 mL 0.4mol•L-1的盐酸 B.10 mL 0.3mol•L-1 MgCl2溶液
C.10 mL 0.5mol•L-1 NaCl溶液 D.10 mL 0.1mol•L-1 AlCl3溶液
(1)Na2C2O4溶液中,1电荷守恒
(2)Na2CO3溶液中,1电荷守恒
(3)将足量的AgCl(s)分别添加到下述四种溶液中,所得溶液c(Ag+)由大到小的顺序是
A.10 mL 0.4mol•L-1的盐酸 B.10 mL 0.3mol•L-1 MgCl2溶液
C.10 mL 0.5mol•L-1 NaCl溶液 D.10 mL 0.1mol•L-1 AlCl3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】草酸(H2C2O4)是一种二元弱酸,广泛分布于动植物体中。
(1)人体内草酸累积过多是导致结石(主要成分是草酸钙)形成的原因之一。有研究发现,EDTA(一种能结合金属离子的试剂)在一定条件下可以有效溶解结石,用化学平衡原理解释其原因:_______________ 。
(2)已知:0.1 mol·L-1KHC2O4溶液呈酸性。下列说法正确的是_______ (填字母序号)。
a. 0.1 mol·L-1KHC2O4溶液中:c(K+) + c(H+) = c(HC2O4-) + 2c(C2O42-) + c(OH-)
b. 0.1 mol·L-1KHC2O4溶液中:c(K+) > c(HC2O4-) > c(C2O42-) > c(H2C2O4)
c. 浓度均为0.1 mol·L-1KHC2O4和K2C2O4的混合溶液中:2c(K+) = c(HC2O4-) + c(C2O42-)
d. 0.1 mol/L KHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+) > c(Na+)
(3)利用草酸制备草酸亚铁晶体(FeC2O4·xH2O)的流程及组分测定方法如下:
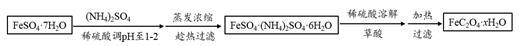
已知:i. pH>4时,Fe2+易被氧气氧化
ii. 几种物质的溶解度(g /100g H2O)如下
①用稀硫酸调溶液pH至1~2的目的是:_____________ ,______________ 。
②趁热过滤的原因是:_______________ 。
③氧化还原滴定法常用于测定草酸亚铁晶体的摩尔质量(M)。称取a g草酸亚铁晶体溶于稀硫酸中,用b mol·L-1的高锰酸钾标准液滴定,到达滴定终点时,消耗高锰酸钾VmL,则M =__________ 。(已知:部分反应产物为Mn2+、Fe3+、CO2)
(1)人体内草酸累积过多是导致结石(主要成分是草酸钙)形成的原因之一。有研究发现,EDTA(一种能结合金属离子的试剂)在一定条件下可以有效溶解结石,用化学平衡原理解释其原因:
(2)已知:0.1 mol·L-1KHC2O4溶液呈酸性。下列说法正确的是
a. 0.1 mol·L-1KHC2O4溶液中:c(K+) + c(H+) = c(HC2O4-) + 2c(C2O42-) + c(OH-)
b. 0.1 mol·L-1KHC2O4溶液中:c(K+) > c(HC2O4-) > c(C2O42-) > c(H2C2O4)
c. 浓度均为0.1 mol·L-1KHC2O4和K2C2O4的混合溶液中:2c(K+) = c(HC2O4-) + c(C2O42-)
d. 0.1 mol/L KHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+) > c(Na+)
(3)利用草酸制备草酸亚铁晶体(FeC2O4·xH2O)的流程及组分测定方法如下:
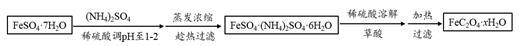
已知:i. pH>4时,Fe2+易被氧气氧化
ii. 几种物质的溶解度(g /100g H2O)如下
| FeSO4·7H2O | (NH4)2SO4 | FeSO4·(NH4)2SO4·6H2O | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
①用稀硫酸调溶液pH至1~2的目的是:
②趁热过滤的原因是:
③氧化还原滴定法常用于测定草酸亚铁晶体的摩尔质量(M)。称取a g草酸亚铁晶体溶于稀硫酸中,用b mol·L-1的高锰酸钾标准液滴定,到达滴定终点时,消耗高锰酸钾VmL,则M =
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Na2CO3和NaHCO3是中学化学中常见的物质,在生产生活中有重要的用途
(1)常温下,0.1mol/L碳酸钠溶液pH约为12。原因是_____ (用离子方程式表示)。
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因________ 。
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度______ PbSO4(填“大于”或“小于”)。
②用离子方程式解释Na2CO3的作用________ 。
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大。原因是________ 。
(4)25℃时,在10mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示:
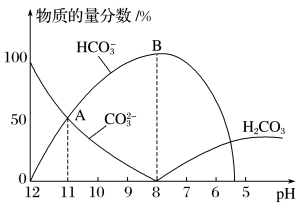
①请写出OAB段的离子方程式________ 。
②当pH=7时,溶液中主要含有哪些离子________ 。(除H+和OH-外)
(1)常温下,0.1mol/L碳酸钠溶液pH约为12。原因是
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度
②用离子方程式解释Na2CO3的作用
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大。原因是
(4)25℃时,在10mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示:

①请写出OAB段的离子方程式
②当pH=7时,溶液中主要含有哪些离子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电解质水溶液中存在电离平衡,水解平衡、沉淀溶解平衡。请回答下列问题:
(1)常温下,部分弱酸的电离平衡常数如表:
①等浓度 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是___________ (写化学式)。
②等浓度的 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为___________ 。
(2)室温下,用 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。___________ (填“甲基橙”或“酚酞”)作指示剂。
②室温下, 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为___________ 
③b点所示的溶液中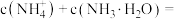
___________ (用溶液的其它离子浓度表示)。
(3)工业上向锅炉里注入所得到的 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。当把水垢中 完全转化时,混合溶液中的
完全转化时,混合溶液中的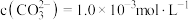 ,则
,则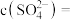
___________  (保留小数点后一位)。
(保留小数点后一位)。
已知: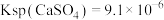 ,
,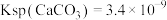
(1)常温下,部分弱酸的电离平衡常数如表:
| 弱酸 |  |  |  |
| 电离平衡常数 | 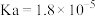 | 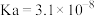 | 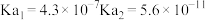 |
 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是②等浓度的
 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为(2)室温下,用
 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。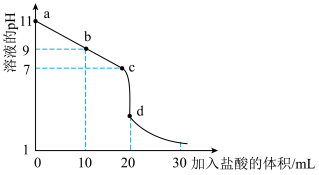
②室温下,
 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为
③b点所示的溶液中
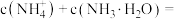
(3)工业上向锅炉里注入所得到的
 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: 完全转化时,混合溶液中的
完全转化时,混合溶液中的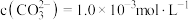 ,则
,则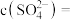
 (保留小数点后一位)。
(保留小数点后一位)。已知:
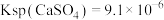 ,
,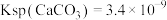
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】沉淀溶解平衡在生产、科研和环保等领域有着许多应用。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是______ 。(已知lg5=0.7)
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
①写出步骤2中溶液变为红色的离子方程式:____________________ 。
②步骤3中现象a是____________________________ 。
③用化学平衡原理解释步骤4中的实验现象:_________________________________ 。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
| 操作步骤 | 现象 |
| 步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液 | 溶液变为红色 |
| 步骤3:向步骤2的溶液中继续加入5滴3 mol·L-1 AgNO3溶液 | 现象a,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变为红色的离子方程式:
②步骤3中现象a是
③用化学平衡原理解释步骤4中的实验现象:
您最近一年使用:0次



