电解质水溶液中存在电离平衡,水解平衡、沉淀溶解平衡。请回答下列问题:
(1)常温下,部分弱酸的电离平衡常数如表:
①等浓度 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是___________ (写化学式)。
②等浓度的 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为___________ 。
(2)室温下,用 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。___________ (填“甲基橙”或“酚酞”)作指示剂。
②室温下, 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为___________ 
③b点所示的溶液中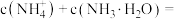
___________ (用溶液的其它离子浓度表示)。
(3)工业上向锅炉里注入所得到的 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。当把水垢中 完全转化时,混合溶液中的
完全转化时,混合溶液中的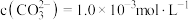 ,则
,则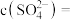
___________  (保留小数点后一位)。
(保留小数点后一位)。
已知: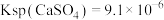 ,
,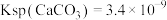
(1)常温下,部分弱酸的电离平衡常数如表:
| 弱酸 |  |  |  |
| 电离平衡常数 | 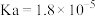 | 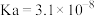 | 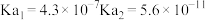 |
 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是②等浓度的
 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为(2)室温下,用
 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。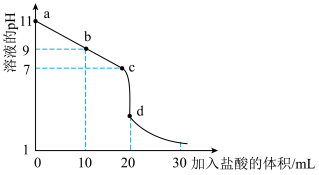
②室温下,
 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为
③b点所示的溶液中
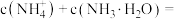
(3)工业上向锅炉里注入所得到的
 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: 完全转化时,混合溶液中的
完全转化时,混合溶液中的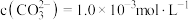 ,则
,则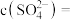
 (保留小数点后一位)。
(保留小数点后一位)。已知:
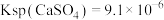 ,
,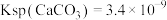
更新时间:2024-02-22 21:29:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】低碳经济是以低能耗、低污染、低排放为基础的经济模式。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)现用300mL 0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:_______ 。
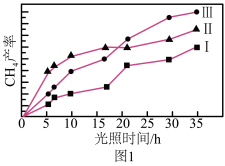
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,紫外线照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图1所示。在0~15h内,对反应催化效果最好的催化剂是_______ 。(填序号)
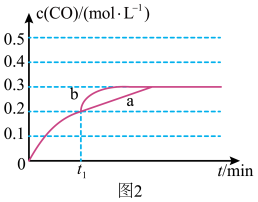
(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g)△H=+41.2kJ•mol﹣1,已知c(CO)随反应时间t的变化曲线a如图2所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是_______ 。
(4)如图3是利用甲烷燃料电池给C电极上镀金属铜,则乙池中选择的电解质溶液为_______ ,A电极的电极反应式为_______ ,若C电极增重0.96g,则B电极上消耗O2的物质的质量为_______ 。

(1)现用300mL 0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,紫外线照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图1所示。在0~15h内,对反应催化效果最好的催化剂是

(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g)△H=+41.2kJ•mol﹣1,已知c(CO)随反应时间t的变化曲线a如图2所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是

(4)如图3是利用甲烷燃料电池给C电极上镀金属铜,则乙池中选择的电解质溶液为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有常温下浓度均为 的下列五种溶液:
的下列五种溶液:
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
(1)这5种溶液pH由大到小的顺序是__________ (填序号)。
(2)②中各离子浓度由大到小的顺序是__________ 。
(3)向③中通入少量氨气,此时 的值
的值__________ (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积__________ ④的体积(填“大于”“小于”或“等于”)。
(5)常温下,向 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为__________ ,若将所得悬浊液的pH值调整为4,则溶液中 的浓度为
的浓度为__________  (已知常温下
(已知常温下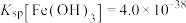 。
。
 的下列五种溶液:
的下列五种溶液:①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液(1)这5种溶液pH由大到小的顺序是
(2)②中各离子浓度由大到小的顺序是
(3)向③中通入少量氨气,此时
 的值
的值(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)常温下,向
 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为 的浓度为
的浓度为 (已知常温下
(已知常温下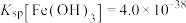 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知溶液中只存在OH-、H+、Na+、CH3COO-四种离子,试回答下列问题:
(1)若溶液中只溶解了一种溶质,则该溶质是___________ ,溶液中c(H+)_____ c(OH-)(填“>”、“=”或“<”)。
(2)若溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则该溶液中的溶质为_____________ ,若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则该溶液中溶质为_________________ 。
(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,且恰好呈中性,则混合前c(NaOH)__________ c(CH3COOH),混合前碱中c(OH-)和酸中c(H+)的关系c(OH-)__________ c(H+)(填“>”,“=”或“<”)。
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则该溶液中的溶质为
(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,且恰好呈中性,则混合前c(NaOH)
您最近一年使用:0次
【推荐1】Ⅰ.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。
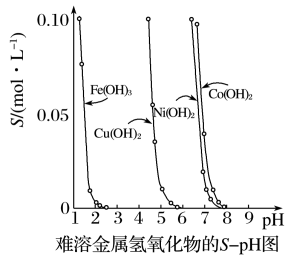
(1)pH=3时溶液中铜元素的主要存在形式是___ (写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___ 。
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___ 。
(4)已知一些难溶物的溶度积常数如表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___ 除去它们。
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:
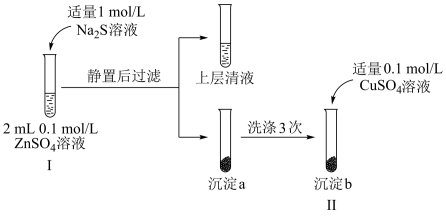
(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:___ 。
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释___ 。
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明___ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:

(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:
| 难溶电解质 | 颜色 | Ksp的数值(18~25℃) |
| ZnS | 白色 | 1.6×10-24 |
| CuS | 黑色 | 1.3×10-36 |
| FeS | 黑色 | 6.3×10-18 |
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为___________ 。
(2)含等物质的量的 和
和 的溶液物料守恒式为
的溶液物料守恒式为___________ 。
(3)向2 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:___________ 。
(4)向 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知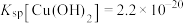 ,则溶液中
,则溶液中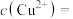
______  。
。
(5)某溶液只含 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入_________ ,然后再加入________ ,调节pH范围为_______ 。
(1)泡沫灭火剂包括
 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为(2)含等物质的量的
 和
和 的溶液物料守恒式为
的溶液物料守恒式为(3)向2
 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:(4)向
 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知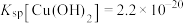 ,则溶液中
,则溶液中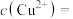
 。
。(5)某溶液只含
 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入| 金属离子 |  |  |  | |
 | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知常温下,Ksp(PbSO4)=1.1×10-8,Ksp(PbCO3)=3.3×10-14,Ksp(PbS)=3.4×10-28。
(1)写出PbSO4溶解平衡的离子方程式______ 。
(2)常温下,溶解度:PbSO4_____ (填“>”“<”或“=”)PbCO3。
(3)从PbSO4固体中回收铅,关键步骤是制备硝酸铅。简单叙述由PbSO4制备Pb(NO3)2的操作原理______ 。
(4)处理废水中的Pb2+宜选择的试剂是______ (填字母)。
A.Na2SO4 B.Na2CO3 C.Na2S
(5)向浓度相等的Na2SO4和Na2CO3溶液中滴加Pb(NO3)2溶液,同时产生两种沉淀时,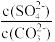 =
=____ 。
(1)写出PbSO4溶解平衡的离子方程式
(2)常温下,溶解度:PbSO4
(3)从PbSO4固体中回收铅,关键步骤是制备硝酸铅。简单叙述由PbSO4制备Pb(NO3)2的操作原理
(4)处理废水中的Pb2+宜选择的试剂是
A.Na2SO4 B.Na2CO3 C.Na2S
(5)向浓度相等的Na2SO4和Na2CO3溶液中滴加Pb(NO3)2溶液,同时产生两种沉淀时,
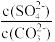 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:_______ ;农业上用石膏(CaSO4·2H2O)降低其碱性的反应原理:_______ 。
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m_______ (填“>”“<”或“=”)n。
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=_______ 。
(4)25℃时,将a mol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ (填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=_______ 。
(5)已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K=
Fe3++3H2O的平衡常数K=_______ 。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(4)25℃时,将a mol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(5)已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+
 Fe3++3H2O的平衡常数K=
Fe3++3H2O的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.常温下,有浓度均为 的下列4种溶液:
的下列4种溶液:
① 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 溶液
溶液
(1)这4种溶液 由大到小的顺序是
由大到小的顺序是_____ (填标号),其中②由水电离的 浓度为
浓度为_____ 。④的水解常数
_____ 。
(2)①中各离子浓度由大到小的顺序是_____ 。
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③_____ ④(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(4)25℃时,测得 和
和 混合溶液的
混合溶液的 ,则
,则 约为
约为_____ 。
Ⅱ.
(5)已知:常温下;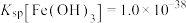 ,(在溶液中某离子完全沉淀时,认为该离子浓度小于
,(在溶液中某离子完全沉淀时,认为该离子浓度小于 )
)
① 的溶度积常数表达式
的溶度积常数表达式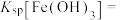
_____ 。
② 完全沉淀的
完全沉淀的 为
为_____ 。
(6) 可用于污水处理的沉淀剂。已知:25℃时,
可用于污水处理的沉淀剂。已知:25℃时, 的电离常数
的电离常数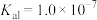 ,
,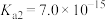 ,反应
,反应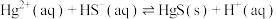 的平衡常数
的平衡常数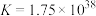 ,则
,则
_____ 。
 的下列4种溶液:
的下列4种溶液:①
 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 溶液
溶液 |  |  |
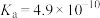 | 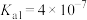  | 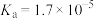 |
 由大到小的顺序是
由大到小的顺序是 浓度为
浓度为
(2)①中各离子浓度由大到小的顺序是
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
 ”“
”“ ”或“
”或“ ”)。
”)。(4)25℃时,测得
 和
和 混合溶液的
混合溶液的 ,则
,则 约为
约为Ⅱ.
(5)已知:常温下;
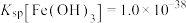 ,(在溶液中某离子完全沉淀时,认为该离子浓度小于
,(在溶液中某离子完全沉淀时,认为该离子浓度小于 )
)①
 的溶度积常数表达式
的溶度积常数表达式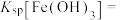
②
 完全沉淀的
完全沉淀的 为
为(6)
 可用于污水处理的沉淀剂。已知:25℃时,
可用于污水处理的沉淀剂。已知:25℃时, 的电离常数
的电离常数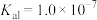 ,
,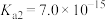 ,反应
,反应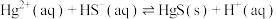 的平衡常数
的平衡常数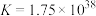 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】亚硫酸盐是一类很早即在世界范围内广泛使用的食品添加剂,可作为食品漂白剂,防腐剂;可抑制非酶褐变和酶促褐变,防止食品褐变,使水果不至黑变,还能防止鲜虾生成黑斑;在酸性介质中,还是十分有效的抗菌剂。
(1)亚硫酸钠中,阴离子的空间结构为___________ 。
(2)常温下, 溶液呈碱性,原因是
溶液呈碱性,原因是___________ (用离子方程式表示)。
(3)常温下,已知 溶液中含硫粒子的浓度之和为
溶液中含硫粒子的浓度之和为 ,向
,向 溶液中加入
溶液中加入 ,溶液中含硫粒子的物质的量分数与溶液的关系如图所示。
,溶液中含硫粒子的物质的量分数与溶液的关系如图所示。
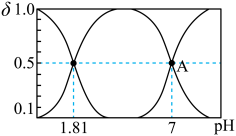
①A点溶液中离子浓度大小关系为___________ 。
②常温下, 溶液呈
溶液呈___________ 性,原因是___________ 。
(4)工业废水中的亚硫酸盐过量排放和不恰当的处理方法会引发严重的环境问题,如水体富营养化、水生生物死亡等。工厂废水排放前,可以先用氧化性工业废水(以含酸性 溶液为例)进行处理,原理是
溶液为例)进行处理,原理是___________ (用离子方程式表示)。常温处理后,再调节 使
使 浓度不高于
浓度不高于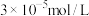 即可排放,调节
即可排放,调节 应不低于
应不低于___________ 。[已知Ksp[Cr(OH)3]=3×10-32]
(1)亚硫酸钠中,阴离子的空间结构为
(2)常温下,
 溶液呈碱性,原因是
溶液呈碱性,原因是(3)常温下,已知
 溶液中含硫粒子的浓度之和为
溶液中含硫粒子的浓度之和为 ,向
,向 溶液中加入
溶液中加入 ,溶液中含硫粒子的物质的量分数与溶液的关系如图所示。
,溶液中含硫粒子的物质的量分数与溶液的关系如图所示。
①A点溶液中离子浓度大小关系为
②常温下,
 溶液呈
溶液呈(4)工业废水中的亚硫酸盐过量排放和不恰当的处理方法会引发严重的环境问题,如水体富营养化、水生生物死亡等。工厂废水排放前,可以先用氧化性工业废水(以含酸性
 溶液为例)进行处理,原理是
溶液为例)进行处理,原理是 使
使 浓度不高于
浓度不高于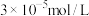 即可排放,调节
即可排放,调节 应不低于
应不低于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填写下列相关内容:
(1)实验表明,液氨也能像水那样进行自耦电离(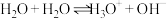 ),写出液氨自耦电离的方程式
),写出液氨自耦电离的方程式___________ 。
(2)室温下,在48mL 的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈
的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈___________ (填“酸性”、“碱性”或“中性”)。
(3)常温下, 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是___________ (填序号,下同),pH由大到小的顺序是___________ 。
①HNO3 ②H2SO4 ③CH3COOH(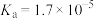 ) ④
) ④ (
( ) ⑤NaOH ⑥
) ⑤NaOH ⑥
(4)某温度时,0.1mol/L的NaOH溶液的pH是11,在此温度下,将 的盐酸溶液
的盐酸溶液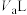 与
与 的NaOH溶液
的NaOH溶液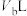 混合,所得混合液为中性,若
混合,所得混合液为中性,若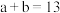 ,则
,则
___________ 。
(5)H2A在水溶液中的电离如下: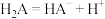 ,
, ,
,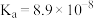 向H2A溶液中滴加少量氨水,该反应的离子方程式为
向H2A溶液中滴加少量氨水,该反应的离子方程式为___________ 。
(6)已知甲酸在一定条件下发生此反应: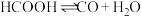 ,正反应速率方程为:
,正反应速率方程为: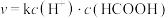 ,k为反应速率常数。
,k为反应速率常数。 温度下,HCOOH电离平衡常数为
温度下,HCOOH电离平衡常数为 ,当HCOOH平衡浓度为xmol/L时,
,当HCOOH平衡浓度为xmol/L时, 浓度为
浓度为___________ mol/L,此时反应速率
___________  (用含
(用含 、x和k的代数式表示)。
、x和k的代数式表示)。
(1)实验表明,液氨也能像水那样进行自耦电离(
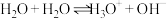 ),写出液氨自耦电离的方程式
),写出液氨自耦电离的方程式(2)室温下,在48mL
 的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈
的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈(3)常温下,
 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是①HNO3 ②H2SO4 ③CH3COOH(
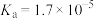 ) ④
) ④ (
( ) ⑤NaOH ⑥
) ⑤NaOH ⑥
(4)某温度时,0.1mol/L的NaOH溶液的pH是11,在此温度下,将
 的盐酸溶液
的盐酸溶液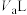 与
与 的NaOH溶液
的NaOH溶液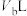 混合,所得混合液为中性,若
混合,所得混合液为中性,若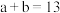 ,则
,则
(5)H2A在水溶液中的电离如下:
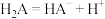 ,
, ,
,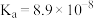 向H2A溶液中滴加少量氨水,该反应的离子方程式为
向H2A溶液中滴加少量氨水,该反应的离子方程式为(6)已知甲酸在一定条件下发生此反应:
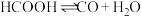 ,正反应速率方程为:
,正反应速率方程为: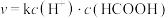 ,k为反应速率常数。
,k为反应速率常数。 温度下,HCOOH电离平衡常数为
温度下,HCOOH电离平衡常数为 ,当HCOOH平衡浓度为xmol/L时,
,当HCOOH平衡浓度为xmol/L时, 浓度为
浓度为
 (用含
(用含 、x和k的代数式表示)。
、x和k的代数式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)25℃时,等浓度的三种溶液,酸性最强的是___________ ,一般情况下,当温度升高时,Ka ___________ (填“增大”、“减小”或“不变”);
(2)室温下,某溶液中存在着CH3COOH(aq)+ (aq)
(aq) CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=
CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=___________ 。(用Ka、K1或K2表示)
(3)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是___________ (填序号)
a.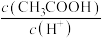 b.
b.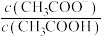 c.
c.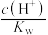 d.
d.
(4)泡沫灭火器(里面装饱和NaHCO3溶液和Al2(SO4)3溶液)的工作原理(用离子方程式表示)___________ 。
(5)证明ClO-结合质子的能力强于HCO (写出相应反应离子方程式并注明过量少量)
(写出相应反应离子方程式并注明过量少量)___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)25℃时,等浓度的三种溶液,酸性最强的是
(2)室温下,某溶液中存在着CH3COOH(aq)+
 (aq)
(aq) CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=
CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=(3)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
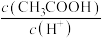 b.
b.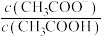 c.
c.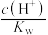 d.
d.
(4)泡沫灭火器(里面装饱和NaHCO3溶液和Al2(SO4)3溶液)的工作原理(用离子方程式表示)
(5)证明ClO-结合质子的能力强于HCO
 (写出相应反应离子方程式并注明过量少量)
(写出相应反应离子方程式并注明过量少量)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
(1)已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-15
H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11
CH3COOH:Ka=1.8×10-5
NH3·H2O:Kb=1.8×10-5
①常温下,0.1mol·L-1Na2S溶液和0.1mol·L-1Na2CO3溶液,碱性更强的是_______ 。
②25℃时,CH3COONH4溶液显_______ 性。
(2)能证明Na2SO3溶液中存在SO +H2O⇌HSO
+H2O⇌HSO +OH-水解平衡的事实是
+OH-水解平衡的事实是_______ (填字母,下同)。
A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去
B.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去
C.滴入酚酞溶液变红,再加氯水后红色褪去
(3)已知:Ka(HClO2)=1.1×10-2,Ka(CH3COOH)=1.8×10-5。25℃时,浓度均为0.1mol·L-1的NaClO2溶液和CH3COONa溶液中c(ClO )
)_______ (填“>”、“<”或“=”)c(CH3COO-)。若要使两溶液的pH相等应_______ 。
a.向NaClO2溶液中加适量水
b.向NaClO2溶液中加适量NaOH
c.向CH3COONa溶液中加CH3COONa固体
d.向CH3COONa溶液中加适量的水
(4)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是_______ (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是_______ 。
(1)已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-15
H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11
CH3COOH:Ka=1.8×10-5
NH3·H2O:Kb=1.8×10-5
①常温下,0.1mol·L-1Na2S溶液和0.1mol·L-1Na2CO3溶液,碱性更强的是
②25℃时,CH3COONH4溶液显
(2)能证明Na2SO3溶液中存在SO
 +H2O⇌HSO
+H2O⇌HSO +OH-水解平衡的事实是
+OH-水解平衡的事实是A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去
B.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去
C.滴入酚酞溶液变红,再加氯水后红色褪去
(3)已知:Ka(HClO2)=1.1×10-2,Ka(CH3COOH)=1.8×10-5。25℃时,浓度均为0.1mol·L-1的NaClO2溶液和CH3COONa溶液中c(ClO
 )
)a.向NaClO2溶液中加适量水
b.向NaClO2溶液中加适量NaOH
c.向CH3COONa溶液中加CH3COONa固体
d.向CH3COONa溶液中加适量的水
(4)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是
您最近一年使用:0次



