金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,以达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如下图。
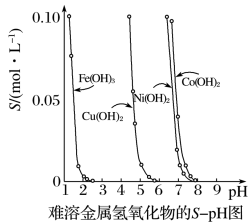
(1)pH=3时溶液中铜元素的主要存在形式是___________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___________ 。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,___________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___________ 。
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式___________ 。
(5)已知一些难溶物的溶度积常数如下表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___________ 除去它们。(选填序号)
A.NaOH B.FeS C.Na2S

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式
(5)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
11-12高二上·辽宁锦州·期末 查看更多[13]
(已下线)2010—2011学年辽宁省北镇高中高二上学期期末考试化学试卷(已下线)同步君 选修4 第3章第4节 难溶电解质的溶解平衡高中化学人教版 选修四 第三章 水溶液中的离子反应 第四节 难溶电解质的溶解平衡 难溶电解质的溶解平衡甘肃省高台县第一中学2018-2019学年高二上学期期中考试化学试题人教版高二化学选修4 第三章 第四节 难溶电解质的溶解平衡练习题(已下线)2019年11月24日《每日一题》高二化学人教版(选修4)—— 每周一测鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节综合训练高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节综合训练人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 作业帮选择性必修1 专题3 第四单元综合训练(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题四川省绵阳市盐亭中学2021-2022学年高二下学期第三次月考化学试题
更新时间:2022-01-17 00:24:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中可以使0.1mol/L CH3COOH溶液中 值增大的措施是
值增大的措施是_____
A.加水稀释 B.加入少量CH3COONa固体
C.加入少量冰醋酸气体 D.通入少量HCl
(2)t℃时,水的离子积常数KW=1×10-12。该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液等体积混合后溶液呈中性,则a+b=___________ 。
(3)常温下,有等pH的三种溶液:a.NaHCO3 b.NaClO c.CH3COONa,三种溶液浓度由大到小的顺序为:_______________ (填序号)
(4)已知25℃时,Ksp(AgCl)= 1.8×10-10,现将足量氯化银分别放入:
a.100mL 蒸馏水中 b.100mL 0.2mol/L AgNO3 溶液中
c.100mL 0.1mol/L氯化铝溶液中 d.100mL 0.1mol/L盐酸溶液中
充分搅拌后,相同温度下银离子浓度由大到小的顺序是______________ (填序号);b中氯离子浓度为_____________ mol/L
(1)下列方法中可以使0.1mol/L CH3COOH溶液中
 值增大的措施是
值增大的措施是A.加水稀释 B.加入少量CH3COONa固体
C.加入少量冰醋酸气体 D.通入少量HCl
(2)t℃时,水的离子积常数KW=1×10-12。该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液等体积混合后溶液呈中性,则a+b=
(3)常温下,有等pH的三种溶液:a.NaHCO3 b.NaClO c.CH3COONa,三种溶液浓度由大到小的顺序为:
(4)已知25℃时,Ksp(AgCl)= 1.8×10-10,现将足量氯化银分别放入:
a.100mL 蒸馏水中 b.100mL 0.2mol/L AgNO3 溶液中
c.100mL 0.1mol/L氯化铝溶液中 d.100mL 0.1mol/L盐酸溶液中
充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向含有AgI固体的饱和溶液中:
(1)加入固体AgNO3,则c(I-)___________ (填“变大”、“变小”或“不变”,下同)。
(2)若改加更多的AgI,则c(Ag+)将___________ 。
(3)若改加AgBr固体,则c(I-)___________ ,而c(Ag+)___________ 。
(1)加入固体AgNO3,则c(I-)
(2)若改加更多的AgI,则c(Ag+)将
(3)若改加AgBr固体,则c(I-)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学在生产生活中有着广泛的应用,请回答下列问题:
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化______ (填“能”或“不能”)用勒夏特列原理解释。
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:______ 。
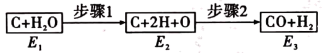
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为______ (填离子符号),再加碱调节至pH为______ 时,铁刚好沉淀完全(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱至pH为6时,锌开始沉淀。若上述过程不加H2O2后果是______ 。(已知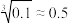 ,lg2
,lg2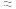 0.3)
0.3)
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:
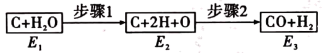
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为
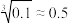 ,lg2
,lg2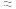 0.3)
0.3)| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp的近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知沉淀溶解平衡在生产、科研和环保等领域具有广泛的应用,请回答下列问题。
(1)工业上处理废水时,Na2S和FeS均可用于除去废水中的Hg2+,试解释原因(用离子方程式表示)___________ ;___________ 。
(2)某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则BaSO4的溶解度___________ (填“增大”“减小”或“不变”,下同),Ksp________ ,c(Ba2+)___________ 。
(3)25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.7×10-13, Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和Cr ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为
,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为___________ 。
(4)洗涤AgCl沉淀表面的可溶性杂质,最好 选用________ 洗涤。(填写序号)
A.蒸馏水 B.AgNO3溶液 C.稀盐酸
(1)工业上处理废水时,Na2S和FeS均可用于除去废水中的Hg2+,试解释原因(用离子方程式表示)
(2)某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则BaSO4的溶解度
(3)25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.7×10-13, Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和Cr
 ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为
,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为(4)洗涤AgCl沉淀表面的可溶性杂质,
A.蒸馏水 B.AgNO3溶液 C.稀盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】含有 的废水毒性较大,某工厂废水中含5.0×10-3mol
的废水毒性较大,某工厂废水中含5.0×10-3mol L-1的
L-1的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:
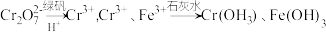
(1)若处理后的废水中残留的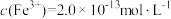 ,则残留的Cr3+的浓度为
,则残留的Cr3+的浓度为_________________ 。
(已知: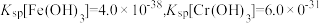 )。
)。
(2)已知室温时, 。在0.1mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是
。在0.1mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是_______________ (已知lg2=0.3)
 的废水毒性较大,某工厂废水中含5.0×10-3mol
的废水毒性较大,某工厂废水中含5.0×10-3mol L-1的
L-1的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理: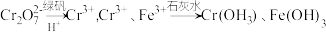
(1)若处理后的废水中残留的
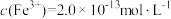 ,则残留的Cr3+的浓度为
,则残留的Cr3+的浓度为(已知:
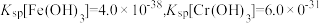 )。
)。(2)已知室温时,
 。在0.1mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是
。在0.1mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知:Ksp[Fe(OH)2]=8×10-16,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=4×10-17,回答下列问题:
(1)Fe(OH)3溶解平衡常数表达式Ksp[Fe(OH)3]=_______ 。
(2)向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是_______ 。常温下,若使0.4 mol·L-1的ZnCl2溶液中的Zn2+开始沉淀,应加入NaOH溶液调整溶液的pH为_______ 。
(3)要除去ZnCl2酸性溶液中混有的少量Fe2+,应先向混合溶液中加入适量_______ 溶液,再加入_______ (填下列选项序号)调节溶液的pH,最后过滤。
a. NH3·H2O b. Na2CO3 c. ZnO d. ZnCO3
(1)Fe(OH)3溶解平衡常数表达式Ksp[Fe(OH)3]=
(2)向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是
(3)要除去ZnCl2酸性溶液中混有的少量Fe2+,应先向混合溶液中加入适量
a. NH3·H2O b. Na2CO3 c. ZnO d. ZnCO3
您最近一年使用:0次



