化学在生产生活中有着广泛的应用,请回答下列问题:
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化______ (填“能”或“不能”)用勒夏特列原理解释。
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:______ 。
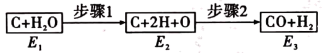
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为______ (填离子符号),再加碱调节至pH为______ 时,铁刚好沉淀完全(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱至pH为6时,锌开始沉淀。若上述过程不加H2O2后果是______ 。(已知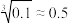 ,lg2
,lg2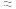 0.3)
0.3)
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:
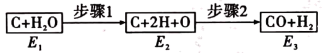
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为
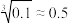 ,lg2
,lg2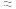 0.3)
0.3)| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp的近似值 | 10-17 | 10-17 | 10-39 |
更新时间:2021-02-02 08:35:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】含铁化合物是重要的基础材料。
请问答:
(1)已知: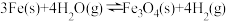
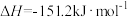 ,
,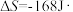
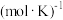 。
。 。当
。当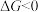 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为___________ K。
(2)高炉炼铁中发生的基本反应之一为:

①在1100℃时,K=0.263,若此时测得高炉中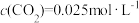 ,
,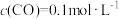 ,判断反应速率
,判断反应速率 (正)
(正)___________  (逆),理由是
(逆),理由是___________ 。
②下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使FeO还原为
B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
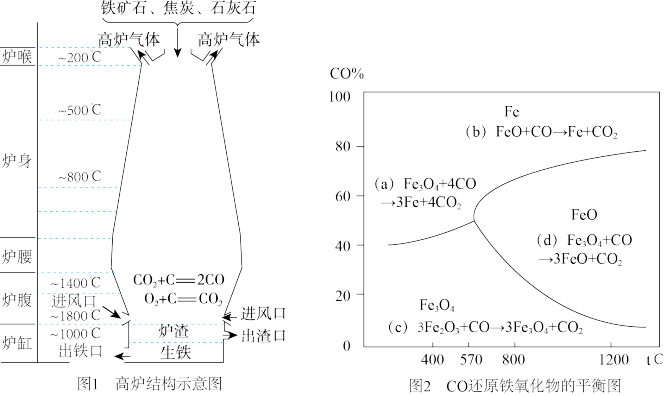
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是___________ (选填:a、b、c、d)。
④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是___________ 。
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是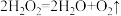 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①___________ ;②___________ 。
请问答:
(1)已知:
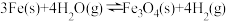
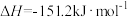 ,
,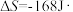
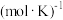 。
。 。当
。当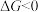 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为(2)高炉炼铁中发生的基本反应之一为:


①在1100℃时,K=0.263,若此时测得高炉中
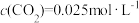 ,
,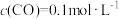 ,判断反应速率
,判断反应速率 (正)
(正) (逆),理由是
(逆),理由是②下列说法不正确的是
A.须采用高温高压的反应条件使FeO还原为

B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是

④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到
 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:| 还原剂 | 600℃ | 700℃ | 800℃ | 900℃ | 1000℃ | 1100℃ | 1200℃ |
| H2 | 4.18 | 3.34 | 2.94 | 2.60 | 2.32 | 2.30 | 2.25 |
| CO | 1.66 | 2.50 | 2.90 | 3.24 | 3.52 | 3.54 | 3.59 |
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是
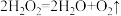 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应为________ 热反应,且m+n________ p(填“>”、“=”或“<”)。
以下各题填“增大”、“减小”或“不变”
(2)若加入催化剂,平衡时气体混合物的总物质的量________ 。
(3)若体积不变加入B,则A的转化率________ ,B的转化率________ 。
(4)减压时,A的质量分数________ ;增压时,B的质量分数________ 。
(5)若升高温度,则B的浓度________ ,平衡时B、C的浓度之比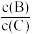 将
将________ 。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)达到新平衡时混合物颜色________ ;若压强不变,则加入C达到新平衡时混合物颜色________ 。(填“变深”、“变浅”或“不变”)
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的正反应为
以下各题填“增大”、“减小”或“不变”
(2)若加入催化剂,平衡时气体混合物的总物质的量
(3)若体积不变加入B,则A的转化率
(4)减压时,A的质量分数
(5)若升高温度,则B的浓度
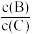 将
将(6)若B是有色物质,A、C均无色,则加入C(体积不变)达到新平衡时混合物颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】自然界的矿物,岩石的成因和变化收到许多条件的影响。地壳内每增加1km,压强增大约25000-30000kPa。在地壳内SiO2和HF存在一下平衡:SiO2(s) +4HF(g)  SiF4(g)+ 2H2O(g) +148.9kJ。
SiF4(g)+ 2H2O(g) +148.9kJ。
(1)写出H2O的电子式:___________ ,SiF4的结构式:____________
(2)在地壳深处容易有___________ 气体逸出,在地壳浅处容易有___________ 沉积。该反应的平衡常数表达式为:K=_______________ 。如果上述反应的平衡常数K值变大,该反应_______ (选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,______ (选填编号)。
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为______ 。
 SiF4(g)+ 2H2O(g) +148.9kJ。
SiF4(g)+ 2H2O(g) +148.9kJ。(1)写出H2O的电子式:
(2)在地壳深处容易有
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知沉淀溶解平衡在生产、科研和环保等领域具有广泛的应用,请回答下列问题。
(1)工业上处理废水时,Na2S和FeS均可用于除去废水中的Hg2+,试解释原因(用离子方程式表示)___________ ;___________ 。
(2)某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则BaSO4的溶解度___________ (填“增大”“减小”或“不变”,下同),Ksp________ ,c(Ba2+)___________ 。
(3)25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.7×10-13, Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和Cr ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为
,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为___________ 。
(4)洗涤AgCl沉淀表面的可溶性杂质,最好 选用________ 洗涤。(填写序号)
A.蒸馏水 B.AgNO3溶液 C.稀盐酸
(1)工业上处理废水时,Na2S和FeS均可用于除去废水中的Hg2+,试解释原因(用离子方程式表示)
(2)某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则BaSO4的溶解度
(3)25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.7×10-13, Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和Cr
 ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为
,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液,最先产生沉淀的阴离子为(4)洗涤AgCl沉淀表面的可溶性杂质,
A.蒸馏水 B.AgNO3溶液 C.稀盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知常温下,FeS的Ksp=6.25×10-18,ZnS的Ksp=1.2×10-23,H2S的饱和溶液中c(H+)与c(S2-)之间存在如下关系:c2(H+)·c(S2-)=1.0×10-22。试回答下列有关问题:
(1)向ZnS的饱和溶液中:
①加入少量固体Na2S,则溶液中c(S2-)_______ (填“变大”、“变小”或“不变”,下同);
②加入ZnS固体,则溶液中c(S2-)_______ ;
③加入FeS固体,则溶液中c(Zn2+)_______ 。
(2)在常温下,将适量的FeS投入到氢硫酸饱和溶液中,欲使溶液中c(Fe2+)达到0.01 mol/L,应调节溶液的pH=_______ (已知:lg2=0.3)。
(1)向ZnS的饱和溶液中:
①加入少量固体Na2S,则溶液中c(S2-)
②加入ZnS固体,则溶液中c(S2-)
③加入FeS固体,则溶液中c(Zn2+)
(2)在常温下,将适量的FeS投入到氢硫酸饱和溶液中,欲使溶液中c(Fe2+)达到0.01 mol/L,应调节溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知温度越高,AgI在水中的溶解度越大,现向有AgI固体的AgI饱和溶液中分别进行如下操作,有关离子浓度的变化情况是:
(1)若加入少量水,则c(I-)_______ (填“增大”、“减小”或“不变”)
(2)若加入AgNO3固体,则AgI在水中的溶解度_______ (填“增大”、“减小”或“不变”)
(3)若加入NaCl固体,则AgI的溶度积Ksp_______ (填“增大”、“减小”或“不变”)
(4)若某温度下,AgI的溶度积Ksp=9.0×10-20,则AgI在该温度下的溶解度是_______ (AgI饱和溶液的密度可近似为1g·mL-1)。
(1)若加入少量水,则c(I-)
(2)若加入AgNO3固体,则AgI在水中的溶解度
(3)若加入NaCl固体,则AgI的溶度积Ksp
(4)若某温度下,AgI的溶度积Ksp=9.0×10-20,则AgI在该温度下的溶解度是
您最近一年使用:0次



