痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下;
①HUr(尿酸,aq)⇌Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6)
②NaUr(s) ⇌Ur-(aq)+Na+(aq)
(1)37 ℃时,1.0 L水中最多可溶解8.0×10-3 mol尿酸钠,此温度下尿酸钠的Ksp为_______ 。
(2)关节炎发作多在脚趾和手指的关节处,这说明温度降低时,尿酸钠的Ksp_______ (填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是_______ (填“放热”或“吸热”)反应。
(3)37 ℃时,某尿酸结石病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3 mol·L-1,其中尿酸分子的浓度为5.0×10-4 mol·L-1,该病人尿液的c(H+)为_______ ,pH_______ 7(填“>”、“<”或“=”)。
①HUr(尿酸,aq)⇌Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6)
②NaUr(s) ⇌Ur-(aq)+Na+(aq)
(1)37 ℃时,1.0 L水中最多可溶解8.0×10-3 mol尿酸钠,此温度下尿酸钠的Ksp为
(2)关节炎发作多在脚趾和手指的关节处,这说明温度降低时,尿酸钠的Ksp
(3)37 ℃时,某尿酸结石病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3 mol·L-1,其中尿酸分子的浓度为5.0×10-4 mol·L-1,该病人尿液的c(H+)为
2021高二·全国·专题练习 查看更多[3]
(已下线)专题3 溶液中的离子反应 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡第三章 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用
更新时间:2022-01-17 10:00:46
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】水的离子积常数与温度有关,回答下列问题:
(1) 时,测得纯水中
时,测得纯水中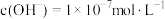 ,则t
,则t___________  (填“>”“<”或“=”),该温度下,
(填“>”“<”或“=”),该温度下,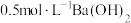 溶液的
溶液的
___________ 。
(2) 时,浓度相同的
时,浓度相同的 和
和 的混合溶液中,
的混合溶液中,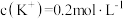 ,则溶液中
,则溶液中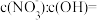
___________ 。
(3) 时,
时, 的某强酸和
的某强酸和 的某强碱按体积比
的某强碱按体积比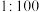 混合后,溶液恰好呈中性,则
混合后,溶液恰好呈中性,则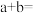
___________ 。
(1)
 时,测得纯水中
时,测得纯水中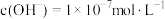 ,则t
,则t (填“>”“<”或“=”),该温度下,
(填“>”“<”或“=”),该温度下,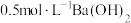 溶液的
溶液的
(2)
 时,浓度相同的
时,浓度相同的 和
和 的混合溶液中,
的混合溶液中,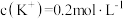 ,则溶液中
,则溶液中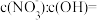
(3)
 时,
时, 的某强酸和
的某强酸和 的某强碱按体积比
的某强碱按体积比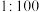 混合后,溶液恰好呈中性,则
混合后,溶液恰好呈中性,则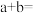
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知水在25 ℃和95 ℃时的电离平衡曲线如图所示。
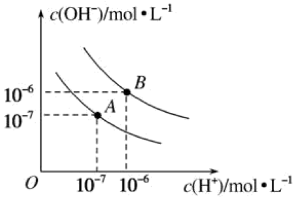
(1)25 ℃时水的电离平衡曲线应为_______ (填“A”或“B”)。25 ℃时,将pH=9的 NaOH 溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则 NaOH 溶液与 H2SO4溶液的体积比为 _______ 。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是_______ 。
(3)在曲线 A 所对应的温度下,pH=2的 HCl溶液和pH=11的某BOH 溶液中,若水的电离程度分别用α1、α2表示,则α1_______ α2(填“大于”“小于”“等于”“无法确定”)
(4)在曲线B所对应的温度下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=_______
(5)已知 HClO 的 Ka=2.98×10-8,CH3COOH 的 Ka=1.75×10-5,下列有关说法不正确的是

(1)25 ℃时水的电离平衡曲线应为
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(3)在曲线 A 所对应的温度下,pH=2的 HCl溶液和pH=11的某BOH 溶液中,若水的电离程度分别用α1、α2表示,则α1
(4)在曲线B所对应的温度下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=
(5)已知 HClO 的 Ka=2.98×10-8,CH3COOH 的 Ka=1.75×10-5,下列有关说法不正确的是
| A.在pH=2的醋酸溶液中加入少量0.01mol·L-1的稀盐酸,溶液的pH 不变 |
| B.在pH=2的醋酸溶液中加少量水,能促进醋酸的电离平衡,但是溶液的pH 会变大 |
| C.100mL pH=2的新制氯水中:n(OH- )+n(ClO-)+n(HClO)=0.001mol |
| D.由电离平衡常数分析,CH3COOH 溶液的pH 一定比 HClO 溶液的pH 小 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知水在25℃和95℃时, 水的电离平衡曲线如图所示:

(1)在25℃时, 水的电离平衡曲线应为_______ (填“A"或“B");95℃时水的离子积 Kw=_______ 。
(2)25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为_______ 。
(3)曲线B对应温度下,pH=2的盐酸溶液和pH=11的氢氧化钠溶液按体积比9:1混合,溶液的pH=_______ 。
(4)常温下,将一小块金属钠投入100mL水中,收集到产生气体的体积为1.12 L(标准状况下),忽略其他因素,此时溶液体积仍为100mL,反应后溶液的pH=_______ 。

(1)在25℃时, 水的电离平衡曲线应为
(2)25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为
(3)曲线B对应温度下,pH=2的盐酸溶液和pH=11的氢氧化钠溶液按体积比9:1混合,溶液的pH=
(4)常温下,将一小块金属钠投入100mL水中,收集到产生气体的体积为1.12 L(标准状况下),忽略其他因素,此时溶液体积仍为100mL,反应后溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
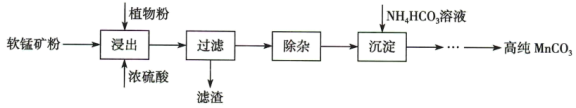
【推荐1】高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为 ,含少量
,含少量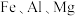 等杂质元素)制备高纯碳酸锰的实验过程如图示,其中植物粉的作用是作还原剂。
等杂质元素)制备高纯碳酸锰的实验过程如图示,其中植物粉的作用是作还原剂。
计算:室温下,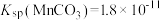 ,
,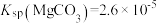 ,已知离子浓度小于
,已知离子浓度小于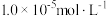 时,表示该离子沉淀完全。若净化液中的
时,表示该离子沉淀完全。若净化液中的 ,试计算说明
,试计算说明 的存在
的存在_______ (填“会”或“不会”)影响 的纯度。
的纯度。
 ,含少量
,含少量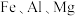 等杂质元素)制备高纯碳酸锰的实验过程如图示,其中植物粉的作用是作还原剂。
等杂质元素)制备高纯碳酸锰的实验过程如图示,其中植物粉的作用是作还原剂。
计算:室温下,
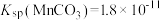 ,
,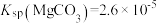 ,已知离子浓度小于
,已知离子浓度小于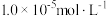 时,表示该离子沉淀完全。若净化液中的
时,表示该离子沉淀完全。若净化液中的 ,试计算说明
,试计算说明 的存在
的存在 的纯度。
的纯度。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9,解答下列问题:
(1)向等浓度的碳酸钠、硫酸钠的混合溶液中逐滴加入氯化钡溶液,最先出现的沉淀是_____ 。
(2)某同学设想用下列流程得到BaCl2溶液:
BaSO4 BaCO3
BaCO3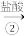 BaCl2
BaCl2
则①的离子方程式为_____ ,该反应的平衡常数K=_____ 。
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,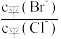 =
=_____ 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=1.8×10-10]
(1)向等浓度的碳酸钠、硫酸钠的混合溶液中逐滴加入氯化钡溶液,最先出现的沉淀是
(2)某同学设想用下列流程得到BaCl2溶液:
BaSO4
 BaCO3
BaCO3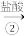 BaCl2
BaCl2则①的离子方程式为
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
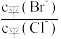 =
=
您最近一年使用:0次
【推荐3】下列说法正确的是________ 。
①难溶电解质的溶度积Ksp越小,则它的溶解度越小
②任何难溶物在水中都存在沉淀溶解平衡,溶解度大小都可以用Ksp表示
③AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
④沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
⑤AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
⑥在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
⑦向2.0 mL浓度均为0.1 mol/L的KCl、KI混合溶液中滴加1~2滴0.01 mol/L AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小
⑧饱和石灰水中加入生石灰,若温度不变,则溶液中Ca2+的物质的量不变
⑨向饱和AgCl水溶液中加入盐酸,Ksp值变大
⑩AgCl的Ksp=1.80×10-10,将0.002mol·L-1的NaCl和0.002mol·L-1的AgNO3溶液等体积混合,有AgCl沉淀生成
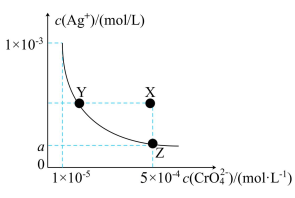
⑪在T℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示,T℃时,在Y点和Z点,Ag2CrO4的Ksp相等
⑫25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.6×10-9,向BaSO4的悬浊液中加入Na2CO3的浓溶液,BaSO4不可能转化为BaCO3
①难溶电解质的溶度积Ksp越小,则它的溶解度越小
②任何难溶物在水中都存在沉淀溶解平衡,溶解度大小都可以用Ksp表示
③AgCl悬浊液中存在平衡:AgCl(s)
 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小④沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
⑤AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
⑥在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
⑦向2.0 mL浓度均为0.1 mol/L的KCl、KI混合溶液中滴加1~2滴0.01 mol/L AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小
⑧饱和石灰水中加入生石灰,若温度不变,则溶液中Ca2+的物质的量不变
⑨向饱和AgCl水溶液中加入盐酸,Ksp值变大
⑩AgCl的Ksp=1.80×10-10,将0.002mol·L-1的NaCl和0.002mol·L-1的AgNO3溶液等体积混合,有AgCl沉淀生成
⑪在T℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示,T℃时,在Y点和Z点,Ag2CrO4的Ksp相等

⑫25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.6×10-9,向BaSO4的悬浊液中加入Na2CO3的浓溶液,BaSO4不可能转化为BaCO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度[S/(mol/L)]如图。
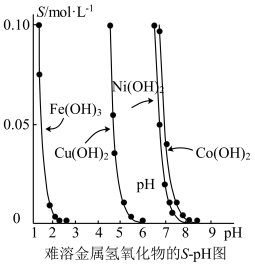
(1)pH=3时溶液中铜元素的主要存在形式是_______ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为_______ 。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含的少量的Co2+杂质,_______ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_______ 。
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式_______ 。
(5)已知常温下一些难溶物的溶度积常数如表:
常温下,饱和HgS溶液中c(Hg2+)=_______ mol·L-1,某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的_______ 除去它们(选填序号)。
A.NaOH B.FeS C.Na2S

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含的少量的Co2+杂质,
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式
(5)已知常温下一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
常温下,饱和HgS溶液中c(Hg2+)=
A.NaOH B.FeS C.Na2S
您最近一年使用:0次
【推荐2】如图所示,横轴为溶液的pH,纵轴为Zn2+或ZnO22-物质的量浓度的对数。回答下列问题:
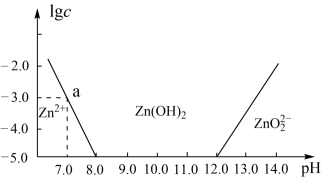
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为__________ 。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=________________ 。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是________ 。

(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知在25 ℃的水溶液中,AgX、AgY、AgZ均难溶于水,但存在溶解平衡。当达到平衡时,溶液中离子浓度的乘积是一个常数(此常数用Ksp表示,Ksp和水的Kw相似)。
如:AgX(s) Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
AgY(s) Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
AgZ(s) Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量/1 L溶液表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为___________ 。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)___________ (填“增大”、“减小”或“不变”)。
(3)在25 ℃时,若取0.188 g的AgY(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为___________ 。
(4)由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:___________ 。
如:AgX(s)
 Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag+(aq)+X-(aq) Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10AgY(s)
 Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag+(aq)+Y-(aq) Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12AgZ(s)
 Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag+(aq)+Z-(aq) Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量/1 L溶液表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)
(3)在25 ℃时,若取0.188 g的AgY(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为
(4)由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知25℃时:H2CO3:Ka1=4.5×10-7、Ka2=4.7×10-11;HClO:Ka=4.0×10-8、lg2=0.3;Ksp(BaSO4)=1.0×10-10、Ksp(BaCO3)=2.6×10-9。
(1)0.4 mol/LHClO溶液的pH=_______ 。
(2)0.4 mol/LNaClO溶液的pH=_______ 。向该溶液中通入少量CO2,发生反应的离子方程式为_______ 。
(3)1.0 L水中投入0.1 mol BaSO4,得到BaSO4的悬浊液,向该悬浊液中投入Na2CO3固体使BaSO4全部转化为BaCO3,理论上需Na2CO3_______ mol(忽略过程中溶液体积的变化)。
(1)0.4 mol/LHClO溶液的pH=
(2)0.4 mol/LNaClO溶液的pH=
(3)1.0 L水中投入0.1 mol BaSO4,得到BaSO4的悬浊液,向该悬浊液中投入Na2CO3固体使BaSO4全部转化为BaCO3,理论上需Na2CO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知: 在水溶液中参与反应时,是以
在水溶液中参与反应时,是以 的形式参与反应,
的形式参与反应, 的电离常数,
的电离常数,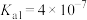 ,
,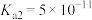 ;
;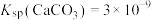 。证明:
。证明: 通入
通入 溶液中,不会发生反应
溶液中,不会发生反应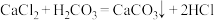
__________ 。
 在水溶液中参与反应时,是以
在水溶液中参与反应时,是以 的形式参与反应,
的形式参与反应, 的电离常数,
的电离常数,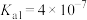 ,
,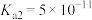 ;
;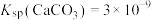 。证明:
。证明: 通入
通入 溶液中,不会发生反应
溶液中,不会发生反应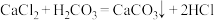
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】草酸即乙二酸,是一种有机二元酸,在工业上有重要的应用。草酸在100℃时开始升华,157℃时大量升华,并开始分解。常温下,相关数据如表所示:
(1)常温下,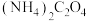 ,溶液的pH
,溶液的pH__________ 7(填“>”“<”或“=”)。
(2)用惰性电极电解饱和草酸溶液可制得乙醛酸( ),阴极的电极反应式为
),阴极的电极反应式为_______ 。
(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸 草酸钠晶体
草酸钠晶体
①75%酒精的作用是____________________________________ 。
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:____________________________________________ 。
(4)已知某温度下 的
的 为
为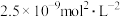 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为__________ 。
| 电离方程式 | 电离常数 |
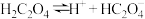 |  |
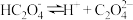 | 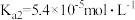 |
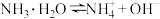 | 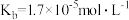 |
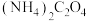 ,溶液的pH
,溶液的pH(2)用惰性电极电解饱和草酸溶液可制得乙醛酸(
 ),阴极的电极反应式为
),阴极的电极反应式为(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸
 草酸钠晶体
草酸钠晶体①75%酒精的作用是
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的
 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:(4)已知某温度下
 的
的 为
为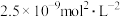 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次



