某小组通过实验探究NO的某些性质。
(1)从氮元素的价态角度分析,NO有_____ 性。
(2)以Cu和HNO3为原料制备NO,反应的化学方程式为______ 。
(3)设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性Na2SO3溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性Na2SO3溶液会发生氧化还原反应,NO被还原为N2O 。
。
ⅱ.Ag+与N2O 反应生成黄色沉淀。
反应生成黄色沉淀。
①检验SO 的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,
的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,_____ (填操作和实验现象)。
②某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和Na2SO4溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,无明显变化。
实验Ⅲ:取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,_____ (填实验现象)。
上述实验证明NO有氧化性。
实验Ⅱ的目的是_____ 。
③写出NO与碱性Na2SO3溶液反应的离子方程式______ 。
④从电极反应角度分析NO与碱性Na2SO3溶液的反应。
还原反应:2NO+2e-=N2O
氧化反应:_____ 。
实验Ⅳ:用排水法收集两瓶NO,将其分别倒扣在饱和Na2SO3溶液和加有NaOH的饱和Na2SO3溶液中,后者集气瓶中液面上升更快。
根据上述实验所得结论:_____ 。
(4)某同学结合所学知识设计处理工业废气中SO2和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的SO2,反应的化学方程式是_____ 。
②再向生成的溶液中加入一定量_____ ,以此溶液来吸收NO气体。
(1)从氮元素的价态角度分析,NO有
(2)以Cu和HNO3为原料制备NO,反应的化学方程式为
(3)设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性Na2SO3溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性Na2SO3溶液会发生氧化还原反应,NO被还原为N2O
 。
。ⅱ.Ag+与N2O
 反应生成黄色沉淀。
反应生成黄色沉淀。①检验SO
 的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,
的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,②某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和Na2SO4溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,无明显变化。
实验Ⅲ:取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,
上述实验证明NO有氧化性。
实验Ⅱ的目的是
③写出NO与碱性Na2SO3溶液反应的离子方程式
④从电极反应角度分析NO与碱性Na2SO3溶液的反应。
还原反应:2NO+2e-=N2O

氧化反应:
实验Ⅳ:用排水法收集两瓶NO,将其分别倒扣在饱和Na2SO3溶液和加有NaOH的饱和Na2SO3溶液中,后者集气瓶中液面上升更快。
根据上述实验所得结论:
(4)某同学结合所学知识设计处理工业废气中SO2和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的SO2,反应的化学方程式是
②再向生成的溶液中加入一定量
21-22高三上·北京石景山·期末 查看更多[3]
北京市第十七中学2021-2022学年高三下学期5月模拟考试化学试题(已下线)二轮拔高卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)北京市石景山区2021-2022学年高三上学期期末考试化学试题
更新时间:2022-01-17 12:47:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某强酸性溶液X可能含有Al3+、Ba2+、 、Fe2+、Fe3+、
、Fe2+、Fe3+、 、
、 、
、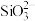 、
、 中的一种或几种,取该溶液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
中的一种或几种,取该溶液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
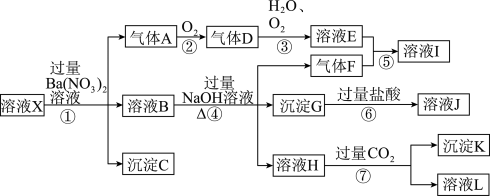
(1)由强酸性条件即可判断溶液X中一定不存在的离子有________ 。
(2)溶液X中,关于 的判断一定正确的是
的判断一定正确的是________ (填字母)。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为________ 。
(4)转化⑥发生反应产生的现象为________ 。
(5)转化④中生成H的离子方程式为________ 。
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为________ 。
(7)对于不能确定是否存在的离子,可以另取溶液X,加入下列溶液中的一种,根据现象即可判断,该试剂最好是________ (填序号)。
①氯水和KSCN的混合溶液 ②KSCN溶液 ③石蕊试剂 ④KMnO4溶液
 、Fe2+、Fe3+、
、Fe2+、Fe3+、 、
、 、
、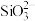 、
、 中的一种或几种,取该溶液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
中的一种或几种,取该溶液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
(1)由强酸性条件即可判断溶液X中一定不存在的离子有
(2)溶液X中,关于
 的判断一定正确的是
的判断一定正确的是a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为
(4)转化⑥发生反应产生的现象为
(5)转化④中生成H的离子方程式为
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为
(7)对于不能确定是否存在的离子,可以另取溶液X,加入下列溶液中的一种,根据现象即可判断,该试剂最好是
①氯水和KSCN的混合溶液 ②KSCN溶液 ③石蕊试剂 ④KMnO4溶液
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
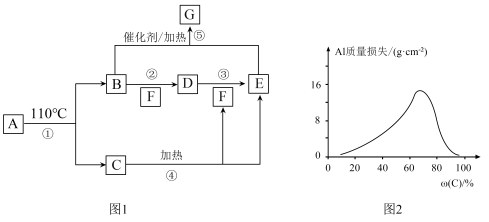
【推荐2】A~G的转化关系如图1所示(部分产物略去),其中E为红棕色气体,G为单质。常温下,将Al片浸在不同质量分数的C溶液中,经过相同时间的腐蚀后,Al片的质量损失情况如图2所示。
(1)A、B的化学式依次为_____ 、_____ 。
(2)实验室中常用_____ 检验B,现象是_____ 。
(3)反应④、⑤的化学方程式依次为_____ 、_____ 。
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为_____ 。
(5)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68 LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5 mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是_____ mL。
(1)A、B的化学式依次为
(2)实验室中常用
(3)反应④、⑤的化学方程式依次为
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为
(5)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68 LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5 mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是___________(填代号)
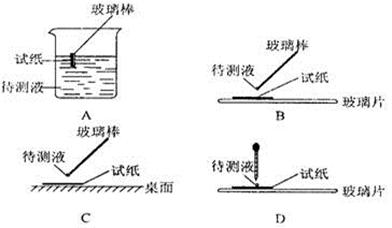
(2)根据上述实验判断原溶液中肯定存在的离子是______________________,肯定不存在的离子是______________________。
(3)写出与②实验有关的离子方程式:
_____________________________________________________________
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是___________(填代号)

(2)根据上述实验判断原溶液中肯定存在的离子是______________________,肯定不存在的离子是______________________。
(3)写出与②实验有关的离子方程式:
_____________________________________________________________
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】磷酸二氢钾(KH2PO4)是一种重要的化工产品,工业上常用作缓冲剂和培养剂,农业上常用作复合肥料。以氟磷灰石[主要成分为Ca5F(PO4)3,还含有少量的Fe2O3、A12O3等杂质]为原料制备KH2PO4晶体的一种流程如下:
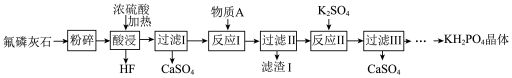
回答下列问题:
(1)“酸浸”过程中生成磷酸的化学方程式为________ ,若用盐酸代替硫酸,磷酸的产率会明显提高,原因是___ ,该过程所用的仪器不能采用二氧化硅陶瓷材料,其主要原因是_____________ (用化学方程式表示)。
(2)已知物质A为CaCO3,其作用是调节溶液pH,则“废渣I”的主要成分为__________ 。
(3) “反应II ”的化学方程式为_______ 。
(4)将获得的KH2PO4晶体进行进一步提纯的方法名称为____ 。
(5)若用1000kg质量分数为50.4%的氟磷灰石来制取磷酸二氢钾晶体,其产率为80%,则生产出的磷酸二氢钾晶体的质量为_____ kg.已知摩尔质量M【Ca5F(PO4)3】=504g/mol,M(KH2PO4)=136 g/mol。

回答下列问题:
(1)“酸浸”过程中生成磷酸的化学方程式为
(2)已知物质A为CaCO3,其作用是调节溶液pH,则“废渣I”的主要成分为
(3) “反应II ”的化学方程式为
(4)将获得的KH2PO4晶体进行进一步提纯的方法名称为
(5)若用1000kg质量分数为50.4%的氟磷灰石来制取磷酸二氢钾晶体,其产率为80%,则生产出的磷酸二氢钾晶体的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】钴酸锂电池应用广泛,电池正极材料主要含有LiCoO2、导电剂乙炔黑、铝箔及少量Fe,可通过下列实验方法回收钴、锂。
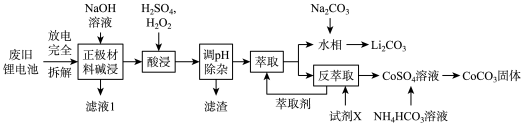
几种金属离子沉淀完全(离子浓度为10-5mo/L)的pH如下表:
回答下列问题:
(1)LiCoO2中,Co元素的化合价为________ ,滤液I的主要成分是_________ 。
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是_________ 。“调节pH”除去的离子主要有Al3+和_________ 。
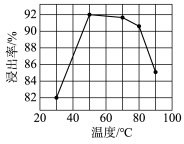
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时漫出率下降的原因是___________ 。
(4)“萃取”和“反萃取”可简单表示为:Co2++2(HA)2 Co(HA2)2+2H+。则反萃取过程加入的试剂X是
Co(HA2)2+2H+。则反萃取过程加入的试剂X是_____________ 。
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为____________ 。
(6)工业上用Li2CO3粗品制备高纯Li2CO3可采用如下方法将Li2CO3溶于盐酸,加入如图所示的电解槽,电解后向LiOH溶液中加入稍过量的NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
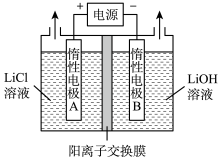
①电解槽中阳极的电极反应式是__________________ 。
②向LiOH溶液中加入稍过量的NH4HCO3溶液时,发生反应的化学方程式为__________ 。

几种金属离子沉淀完全(离子浓度为10-5mo/L)的pH如下表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
| 溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
(1)LiCoO2中,Co元素的化合价为
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时漫出率下降的原因是

(4)“萃取”和“反萃取”可简单表示为:Co2++2(HA)2
 Co(HA2)2+2H+。则反萃取过程加入的试剂X是
Co(HA2)2+2H+。则反萃取过程加入的试剂X是(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为
(6)工业上用Li2CO3粗品制备高纯Li2CO3可采用如下方法将Li2CO3溶于盐酸,加入如图所示的电解槽,电解后向LiOH溶液中加入稍过量的NH4HCO3溶液,过滤、烘干得高纯Li2CO3。

①电解槽中阳极的电极反应式是
②向LiOH溶液中加入稍过量的NH4HCO3溶液时,发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
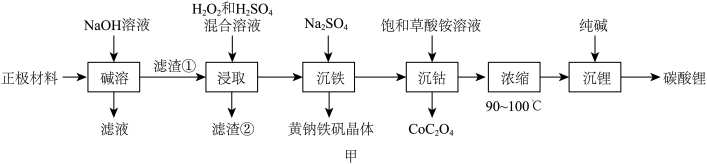
【推荐3】一种从废旧电池的正极材料(含铝箔、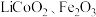 及少量不溶于酸、碱的导电剂)中回收多种金属的工艺流程如图甲所示:
及少量不溶于酸、碱的导电剂)中回收多种金属的工艺流程如图甲所示:
已知:①黄钠铁矾晶体稳定,颗粒大、易沉降。
②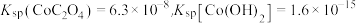 。
。
回答下列问题:
(1)碱溶:碱溶前,常使用丙酮浸泡正极材料,作用是___________ ;从经济效益的角度考虑,可向碱溶后所得滤液中通入过量 ,其目的是
,其目的是___________ (用化学方程式表示)。
(2)浸取时也可用盐酸代替 和
和 的混合溶液,但缺点是
的混合溶液,但缺点是___________ 。
(3)沉铁:
①沉铁时采用的“黄钠铁矾法”与传统的调pH的“氢氧化物沉淀法”相比,金属离子的损失少,原因是___________ 。
②控制不同的条件可以得到不同的沉淀,所得沉淀与温度和pH的关系如图乙所示(阴影部分表示黄钠铁矾稳定存在的区域),据图,在25℃时,调节溶液的pH=4,此时溶液中
___________ ,该温度下,若要制得黄钠铁矾晶体需控制溶液的pH范围为___________ (填序号){已知25℃,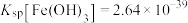 }。
}。
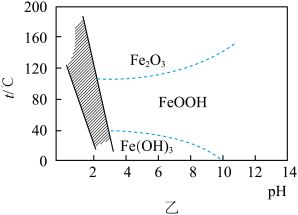
a、0~1
b、1~2.5
c、2.5~3.0
③称取2.425g黄钠铁矾晶体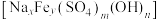 ,加盐酸完全溶解后,配制成100.00mL溶液;量取25.00mL溶液,加入过量的KI溶液,充分反应,消耗
,加盐酸完全溶解后,配制成100.00mL溶液;量取25.00mL溶液,加入过量的KI溶液,充分反应,消耗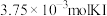 ,另取25.00mL溶液,加入足量
,另取25.00mL溶液,加入足量 溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g。则沉铁时反应的离子方程式为
溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g。则沉铁时反应的离子方程式为___________ 。
(4)沉钴:沉钴时使用饱和草酸铵溶液,与饱和草酸钠溶液相比效果更好的原因是___________ 。
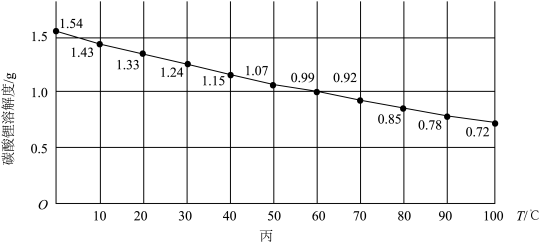
(5)沉锂:碳酸锂溶解度随温度变化曲线如图丙,“沉锂”后得到碳酸锂固体的实验操作为___________ 。
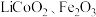 及少量不溶于酸、碱的导电剂)中回收多种金属的工艺流程如图甲所示:
及少量不溶于酸、碱的导电剂)中回收多种金属的工艺流程如图甲所示:
已知:①黄钠铁矾晶体稳定,颗粒大、易沉降。
②
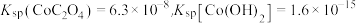 。
。回答下列问题:
(1)碱溶:碱溶前,常使用丙酮浸泡正极材料,作用是
 ,其目的是
,其目的是(2)浸取时也可用盐酸代替
 和
和 的混合溶液,但缺点是
的混合溶液,但缺点是(3)沉铁:
①沉铁时采用的“黄钠铁矾法”与传统的调pH的“氢氧化物沉淀法”相比,金属离子的损失少,原因是
②控制不同的条件可以得到不同的沉淀,所得沉淀与温度和pH的关系如图乙所示(阴影部分表示黄钠铁矾稳定存在的区域),据图,在25℃时,调节溶液的pH=4,此时溶液中

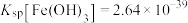 }。
}。
a、0~1
b、1~2.5
c、2.5~3.0
③称取2.425g黄钠铁矾晶体
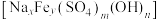 ,加盐酸完全溶解后,配制成100.00mL溶液;量取25.00mL溶液,加入过量的KI溶液,充分反应,消耗
,加盐酸完全溶解后,配制成100.00mL溶液;量取25.00mL溶液,加入过量的KI溶液,充分反应,消耗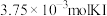 ,另取25.00mL溶液,加入足量
,另取25.00mL溶液,加入足量 溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g。则沉铁时反应的离子方程式为
溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g。则沉铁时反应的离子方程式为(4)沉钴:沉钴时使用饱和草酸铵溶液,与饱和草酸钠溶液相比效果更好的原因是
(5)沉锂:碳酸锂溶解度随温度变化曲线如图丙,“沉锂”后得到碳酸锂固体的实验操作为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】电池级CoSO4可用于制备CoCO3和CoC2O4等钴盐。一种以粗Co(OH)3渣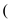 含有Fe2O3、SiO2、CuO、CaO、MgO、ZnO等杂质
含有Fe2O3、SiO2、CuO、CaO、MgO、ZnO等杂质 为原料制备电池级CoSO4·7H2O的工艺流程如图所示:
为原料制备电池级CoSO4·7H2O的工艺流程如图所示:
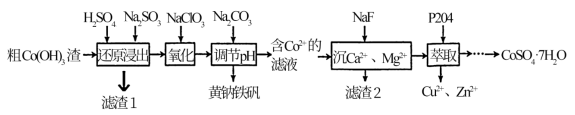
已知:黄钠铁矾[NaFe3(SO4)2(OH)6]为淡黄色难溶物,是一种过滤性、洗涤性较好的复式硫酸盐。
回答下列问题:
(1)黄钠铁矾[NaFe3(SO4)2(OH)6]中铁元素的化合价为___________ 。
(2)欲提高钴元素的浸出率,可以采取的措施有___________ 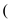 任写一种
任写一种 。
。
(3)滤渣1的主要成分是___________ (填化学式)。
(4)写出“还原浸出”过程中Co(OH)3发生反应的化学方程式___________ 。
(5)Na2SO3用量、浸出终点pH对钴浸出率的影响分别如图1、图2所示:
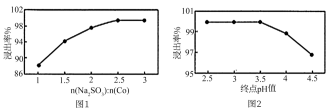
则较为适宜的控制条件是___________ 。
(6)“氧化”过程中的还原产物为ClO2,该过程的主要反应的离子方程式为___________ ,为证明加入的NaClO3已足量,可以取适量溶液于洁净的试管,加入___________ 溶液,根据产生的现象进行判断。
 含有Fe2O3、SiO2、CuO、CaO、MgO、ZnO等杂质
含有Fe2O3、SiO2、CuO、CaO、MgO、ZnO等杂质 为原料制备电池级CoSO4·7H2O的工艺流程如图所示:
为原料制备电池级CoSO4·7H2O的工艺流程如图所示:
已知:黄钠铁矾[NaFe3(SO4)2(OH)6]为淡黄色难溶物,是一种过滤性、洗涤性较好的复式硫酸盐。
回答下列问题:
(1)黄钠铁矾[NaFe3(SO4)2(OH)6]中铁元素的化合价为
(2)欲提高钴元素的浸出率,可以采取的措施有
 任写一种
任写一种 。
。(3)滤渣1的主要成分是
(4)写出“还原浸出”过程中Co(OH)3发生反应的化学方程式
(5)Na2SO3用量、浸出终点pH对钴浸出率的影响分别如图1、图2所示:

则较为适宜的控制条件是
(6)“氧化”过程中的还原产物为ClO2,该过程的主要反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】化合物X由三种短周期元素组成,某学习小组按如下流程进行实验:
实验I
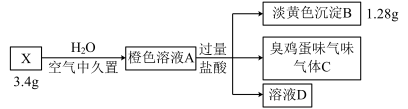
实验II
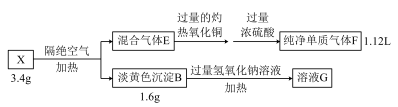
已知:E到F的过程中热的氧化铜变红,浓硫酸增重3.6g。单质气体F是空气中的重要组成成分,体积已折算成标准状况下的体积。
请回答:
(1)X的组成元素是___________ ,X的化学式是___________ 。
(2)写出X→橙色溶液A所发生的化学反应方程式___________ 。
(3)写出B→G的离子方程式___________ 。
(4)设计实验检验溶液D中的阳离子___________ 。
实验I

实验II

已知:E到F的过程中热的氧化铜变红,浓硫酸增重3.6g。单质气体F是空气中的重要组成成分,体积已折算成标准状况下的体积。
请回答:
(1)X的组成元素是
(2)写出X→橙色溶液A所发生的化学反应方程式
(3)写出B→G的离子方程式
(4)设计实验检验溶液D中的阳离子
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
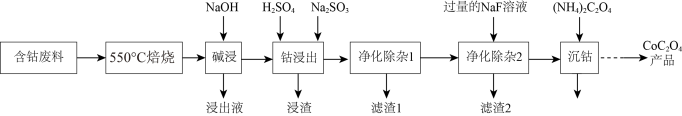
【推荐3】草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、ZnO、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是_______ 。
(2)“浸出液”的主要成分是_______ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_______ 。
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是_______ ,H2O2的作用是_______ (用离子方程式表示)。
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:_______ 。
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:
您最近一年使用:0次



