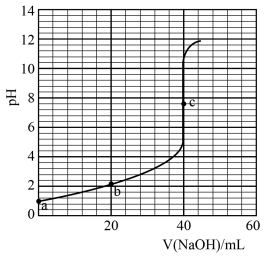
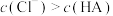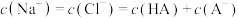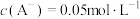用0.1mol/L NaOH溶液滴定10mL 0.1mol/L盐酸,利用电导率传感器可绘制滴定过程中的电导率曲线如下图所示。下列说法错误的是
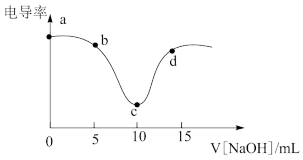

| A.电导率最低点c点就是酸碱中和滴定的终点 |
| B.由图所知,随着NaOH溶液增加,溶液pH先变小后变大 |
C.b、c、d点都存在: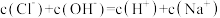 |
| D.a点电导率最大是因为此时溶液中导电微粒浓度最高 |
2022·广西柳州·二模 查看更多[5]
(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)湖南省郴州市第一中学2023届高三下学期第七次月考化学试题黑龙江省佳木斯市第一中学2022届高三下学期验收测试化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)广西柳州市2022届高三第二次模拟考试理科综合化学试题
更新时间:2022-01-30 22:43:01
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
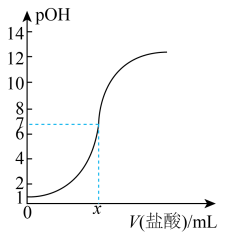
【推荐1】室温时,实验室用一定浓度的盐酸标准液滴定20 mL一定浓度的氢氧化钠溶液,加入盐酸的体积与所滴溶液的pOH( 浓度的负常用对数)变化关系如图,下列有关说法正确的是
浓度的负常用对数)变化关系如图,下列有关说法正确的是
 浓度的负常用对数)变化关系如图,下列有关说法正确的是
浓度的负常用对数)变化关系如图,下列有关说法正确的是
| A.滴定前溶液的pH等于1 |
B.若盐酸标准液的浓度为0.01 mol⋅L ,则 ,则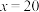 |
C.若盐酸标准液的浓度为0.1 mol⋅L ,滴定终点(反应恰好完全)时,少滴了一滴(1 mL约为25滴)盐酸,则溶液的pH约等于10 ,滴定终点(反应恰好完全)时,少滴了一滴(1 mL约为25滴)盐酸,则溶液的pH约等于10 |
| D.滴定过程中眼睛一定要始终平视滴定管的凹液面 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】 溶液可用于测定溶液中
溶液可用于测定溶液中 的含量,实验方案如下:
的含量,实验方案如下:
步骤1:准确量取 溶液
溶液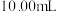 ,稀释至
,稀释至 ;
;
步骤2:量取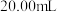 稀释后的
稀释后的 溶液于锥形瓶中,调节溶液的
溶液于锥形瓶中,调节溶液的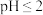 ,加入足量的
,加入足量的 晶体,摇匀,在暗处静置30分钟(已知反应产物为
晶体,摇匀,在暗处静置30分钟(已知反应产物为 、
、 );
);
步骤3:以淀粉溶液作指示剂,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: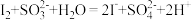 )。
)。
下列说法正确的是
 溶液可用于测定溶液中
溶液可用于测定溶液中 的含量,实验方案如下:
的含量,实验方案如下:步骤1:准确量取
 溶液
溶液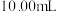 ,稀释至
,稀释至 ;
;步骤2:量取
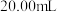 稀释后的
稀释后的 溶液于锥形瓶中,调节溶液的
溶液于锥形瓶中,调节溶液的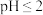 ,加入足量的
,加入足量的 晶体,摇匀,在暗处静置30分钟(已知反应产物为
晶体,摇匀,在暗处静置30分钟(已知反应产物为 、
、 );
);步骤3:以淀粉溶液作指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: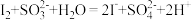 )。
)。下列说法正确的是
A. 中 中 元素化合价为 元素化合价为 |
B.步骤2反应的离子方程式为 |
C.滴定终点的现象:滴加最后半滴 溶液时,溶液刚好由无色变为蓝色,且 溶液时,溶液刚好由无色变为蓝色,且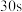 不恢复原色 不恢复原色 |
D.原 溶液的物质的量浓度为 溶液的物质的量浓度为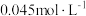 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在10mL0.1mol·L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系错误的是
| A.c(Na+)>c(Ac-)>c(H+)>c(OH-) |
| B.c(Na+)>c(Ac-)>c(OH-)>c(H+) |
| C.c(Na+)>c(Ac-)>c(HAc) |
| D.c(Na+)+c(H+)=c(Ac-)+c(OH-) |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】室温下,向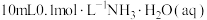 中逐滴加入
中逐滴加入 ,已知
,已知 。下列说法正确的是
。下列说法正确的是
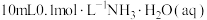 中逐滴加入
中逐滴加入 ,已知
,已知 。下列说法正确的是
。下列说法正确的是A. 时,由水电离出的 时,由水电离出的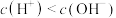 |
B. 时, 时, |
C. 时, 时,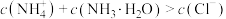 |
D. 时, 时,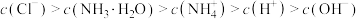 |
您最近半年使用:0次

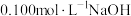 溶液分别滴定
溶液分别滴定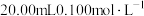 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
 时,滴定醋酸消耗
时,滴定醋酸消耗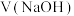 小于20mL
小于20mL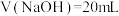 时,两份溶液中
时,两份溶液中
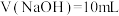 时,醋酸溶液中:
时,醋酸溶液中: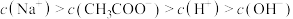
 HCl和
HCl和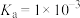 )混合溶液20mL,用
)混合溶液20mL,用