下列说法中正确的是
A.相同温度下,将 的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸pH略大 的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸pH略大 |
B.常温下,某溶液水电离出的 为 为 ,该溶液的pH可能为1或13 ,该溶液的pH可能为1或13 |
| C.难溶电解质在水中达到溶解平衡时,加少量水后溶液中离子浓度减小 |
D.向氨水中加入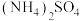 固体,溶液中 固体,溶液中 增大 增大 |
更新时间:2022-02-08 10:07:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液:Na+、Cu2+、 、Cl- 、Cl- |
B. =1×10-12的溶液:K+、Na+、 =1×10-12的溶液:K+、Na+、 、 、 |
C.使甲基橙呈红色的溶液:Ba2+、 、Cl-、ClO- 、Cl-、ClO- |
D.能溶解Al(OH)3的溶液:Na+、 、 、 、CH3COO- 、CH3COO- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
| A.c(H+)=1×10-7mol·L-1的溶液一定是中性溶液 |
| B.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下溶液中其c(H+)c(OH-)=1×10-14 |
| C.向水中加入少量固体NaHSO4,水的电离平衡逆向移动,Kw减小 |
| D.将水加热,Kw增大,pH不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】对 0.1 mol·L-1 醋酸溶液在25 ℃下的稀释过程,不正确的是
| A.醋酸的电离平衡常数不变 | B.溶液中c(H+)减小 |
| C.c(H+)/c(CH3COOH)增大 | D.醋酸溶液中所有离子的浓度均减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列化学用语或图示不正确的是
A.由 和 和 形成离子键的过程: 形成离子键的过程: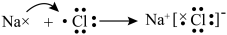 |
B.常温时, 氨水的 氨水的 的原因: 的原因: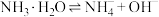 |
C. 分子中 分子中 键的形成: 键的形成: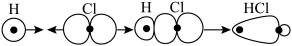 |
D.反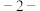 丁烯的结构简式: 丁烯的结构简式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,向10mL0.2000mol/LNaOH溶液中滴加0.2000mol/L的一元酸HA,溶液pH的变化曲线如图所示 忽略溶液混合过程中体积变化
忽略溶液混合过程中体积变化 。已知H2CO3Ka1=4.4×10-7,Ka2=4.7×10-11,下列说法正确的是
。已知H2CO3Ka1=4.4×10-7,Ka2=4.7×10-11,下列说法正确的是


 忽略溶液混合过程中体积变化
忽略溶液混合过程中体积变化 。已知H2CO3Ka1=4.4×10-7,Ka2=4.7×10-11,下列说法正确的是
。已知H2CO3Ka1=4.4×10-7,Ka2=4.7×10-11,下列说法正确的是


| A.HA为弱酸,电离平衡常数的数量级约为10−9 |
| B.b点所示溶液中c(A−)>c(HA) |
| C.pH=7时,c(Na+)=c(A−)+c(HA) |
| D.室温下,以酚酞为指示剂进行滴定,若氢氧化钠吸收少量CO2,恰好完全反应时消耗该HA溶液的体积仍为10 mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是( )
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| B.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| C.25 ℃时Ksp(AgCl)=1.8×10-10,向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度增大 |
| D.为确定二元酸H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于沉淀溶解平衡的判断正确的是
| A.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
B.向饱和 水溶液中加入 水溶液中加入 固体, 固体,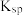 值变大 值变大 |
C.向 悬浊液中滴加 悬浊液中滴加 溶液,生成红褐色沉淀 溶液,生成红褐色沉淀 |
D.含有 和 和 固体的悬浊液: 固体的悬浊液: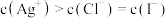 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】查阅资料可知:t ℃时,可用Na2S沉淀X2+、Y2+、Z2+(用M2+表示),所需S2-最低浓度的对数值lg c(S2-)与lg c(M2+)的关系如图所示。下列说法正确的是


| A.三种离子对应的硫化物中Ksp(XS)最小,约为1×10-20 |
| B.将ZS固体加入水中,部分溶解,继续加入少量水,固体量减小,溶液中c(S2-)增大 |
C.YS、XS的饱和溶液中: 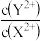 =1×1020 =1×1020 |
| D.在c(X2+)=c(Z2+)=c(Y2+)=1×10-5 mol·L-1的混合溶液中逐滴加入1×10-4 mol·L-1的Na2S溶液,最先沉淀的是YS |
您最近一年使用:0次



