设NA是阿伏加德罗常数的值,下列说法正确的是
| A.2.8gFe与水蒸气充分反应转移的电子数目为0.1NA |
| B.等物质的量乙烯和乙醇完全燃烧,消耗O2都为3NA |
| C.密闭容器中1molH2与1molI2制备HI,增加2NA个H—I键 |
| D.4g由H218O与D216O组成的混合物中所含中子数为2NA |
更新时间:2022-02-25 21:37:28
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】NA为阿伏加 德罗常数的值。下列叙述正确的是
| A.标准状况下,6.72L SO3所含的氧原子数目为0.9NA |
| B.含0.4mol HCl的浓盐酸与足量二氧化锰共热反应,生成Cl2的分子数为0.1NA |
| C.密闭容器中1mol N2与4mol H2充分反应,形成的N—H键数为6NA |
| D.标准状况下 22.4L CH4 和 C2H4的混合气体所含氢原子数为 4NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】若标准状况下11.2 L氧气含有n个氧原子,则阿伏加 德罗常数的数值可表示为 ( )
| A.4n | B.3n | C.2n | D.n |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列数据或事实所呈现的规律不能用元素周期律解释的是( )
| A. | 化学方程式 | K | B. | 最高价含氧酸 | 酸性强弱 | ||
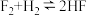 | 1.8×1036 | HClO4 | 强酸 | ||||
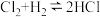 | 9.7×1012 | H3PO4 | 中强酸 | ||||
 | 5.6×107 | H2SiO3 | 弱酸 | ||||
| C. | 气态氢化物 | 分解温度/℃ | D. | 共价键 | 键能/kJ·mol-1 | ||
| H2O | >2000 | C-C | 347 | ||||
| H2S | ≈300 | C=C | 620 | ||||
| H2Se | ≈160 | CC | 812 | ||||
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】工业合成氨的反应为:N2+3H2 2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是
2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是
 2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是
2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是A.达到平衡时,反应速率 (正)= (正)= (逆)=0 (逆)=0 |
| B.当N2、H2、NH3的浓度比为1∶3∶2时,说明反应达到平衡 |
| C.使用催化剂可同时加快正、逆反应速率,提高生产效率 |
| D.若在密闭容器加入1mol N2和足量H2,最多能生成2mol NH3 |
您最近一年使用:0次
【推荐3】N2(g)+3H2(g)⇌2NH3(g),∆H=-akJ·mol-1反应过程中的能量变化如图所示(图中 E1表示无催化剂时正反应活化能的数值,E2表示无催化剂时逆反应活化能的数值)。下列说法错误的是


| A.升高温度可提高 N2、H2、NH3的活化分子百分数 |
| B.a = E2-E1 |
| C.恒温恒压条件下通氦气的瞬间,单位体积内 N2的活化分子数减小 |
| D.将 1molN2(g) 和 3molH2(g) 置于密闭容器中充分反应放出 akJ 的热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】在酸性条件下,黄铁矿 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是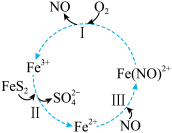
| A.黄铁矿催化氧化中NO作催化剂 |
B.反应Ⅰ的离子方程式为 |
| C.反应Ⅲ是非氧化还原反应 |
D.反应Ⅱ中若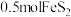 被还原,转移电子的物质的量为 被还原,转移电子的物质的量为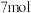 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】用下列方法均可以制得氧气:①2KClO3=2KCl+3O2 ②2Na2O2+2H2O=4NaOH+O2↑③2HgO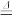 2Hg+O2④2KMnO4
2Hg+O2④2KMnO4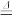 K2MnO4+MnO2+O2若要制得相同质量的氧气,则在反应过程中转移的电子数之比为
K2MnO4+MnO2+O2若要制得相同质量的氧气,则在反应过程中转移的电子数之比为
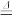 2Hg+O2④2KMnO4
2Hg+O2④2KMnO4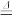 K2MnO4+MnO2+O2若要制得相同质量的氧气,则在反应过程中转移的电子数之比为
K2MnO4+MnO2+O2若要制得相同质量的氧气,则在反应过程中转移的电子数之比为| A.3:2:1:4 | B.1:1:1:1 | C.2:1:2:2 | D.1:2:1:1 |
您最近一年使用:0次

 为蓝色,
为蓝色, 为淡黄色,已知能发生如下反应:
为淡黄色,已知能发生如下反应:



 溶液中滴加酸性
溶液中滴加酸性 溶液,溶液颜色由蓝色变为淡黄色
溶液,溶液颜色由蓝色变为淡黄色 的酸性溶液中滴加
的酸性溶液中滴加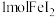 溶液充分反应,转移
溶液充分反应,转移 电子
电子

