2SO2+O2 2SO3是接触法制硫酸工艺中的一个重要反应,下列关于该反应的说法错误的是
2SO3是接触法制硫酸工艺中的一个重要反应,下列关于该反应的说法错误的是
 2SO3是接触法制硫酸工艺中的一个重要反应,下列关于该反应的说法错误的是
2SO3是接触法制硫酸工艺中的一个重要反应,下列关于该反应的说法错误的是| A.增加SO2的浓度能加快该反应的速率 |
| B.反应过程中SO2能全部转化为SO3 |
| C.降低体系温度会减慢该反应的速率 |
| D.使用催化剂能改变反应的速率 |
更新时间:2022-03-08 21:54:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验及其结论都正确的是
| 实验 | 结论 | |
| A | 分别向 的酸性 的酸性 和 和 的酸性 的酸性 溶液中滴加 溶液中滴加 的草酸溶液 的草酸溶液 ,用秒表记录褪色时间 ,用秒表记录褪色时间 | 反应物的浓度越大,反应速率越快 |
| B | 室温下,用 试纸测定浓度均为 试纸测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| C | 等体积、 的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性HA比HB弱 |
| D | 向某钠盐中滴加浓盐酸,将产生的气体通入品红溶液 | 根据品红溶液褪色判断该钠盐为 或 或 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验装置、试剂选用或操作正确的是

A.用图甲装置收集 | B.用图乙装置制备、干燥并收集 |
C.用图丙装置制备 固体 固体 | D.用图丁装置探究浓度对反应速率的影响 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,0.2 mol·L-1的盐酸30mL分别与下列Na2CO3溶液混合,再加水稀释到100mL,其中最初产生CO2的速率最快的是
| A.20mL0.3 mol·L-1Na2CO3 | B.10mL0.4 mol·L-1Na2CO3 |
| C.25mL0.4 mol·L-1Na2CO3 | D.15mL0.5 mol·L-1Na2CO3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将2mL 0.1mol·L -1 FeCl3溶液和2mL 0.01mol·L -1 KSCN溶液混合,发生如下反应:FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
 Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液| A.②③ | B.③ | C.②④ | D.①③④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】臭氧分解过程如图所示,下列说法正确的是
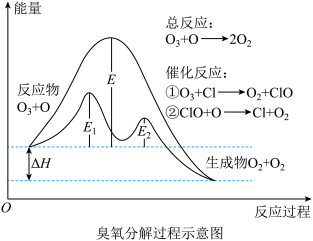

| A.催化反应①②均为放热反应 |
B.决定 分解反应速率的是催化反应② 分解反应速率的是催化反应② |
C. 是催化反应①对应的正反应的活化能, 是催化反应①对应的正反应的活化能,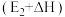 是催化反应②对应的逆反应的活化能 是催化反应②对应的逆反应的活化能 |
| D.温度升高,总反应的正反应速率增加,逆反应速率减小。 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各示意图与对应的表述正确的是
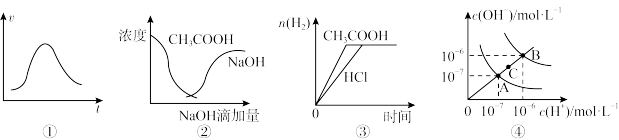

| A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 |
| B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图 |
| C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】用如图装置进行铜与稀硝酸反应的实验。开始反应阶段几乎不产生气泡,约2分钟后,铜表面产生无色气泡,5分钟后产生气体逐渐变快,溶液变为蓝色,液面上方气体变为浅红棕色。

下列分析合理的是

下列分析合理的是
A.铜与稀硝酸反应生成的气体为 和 和 |
| B.根据实验现象推测,铜与稀硝酸反应时可能吸收热量 |
C.根据实验现象推测, 或 或 可能为铜与稀硝酸反应的催化剂 可能为铜与稀硝酸反应的催化剂 |
| D.当试管中的反应停止后,向试管中加入稀硫酸,铜丝表面一定无现象 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某实验小组学习化学反应速率后,联想到 分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
 分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是| 编号 | 温度 | 反应物 | 催化剂 |
| 甲 | 25℃ | 试管中加入 溶液 溶液 |  蒸馏水 蒸馏水 |
| 乙 | 25℃ | 试管中加入 溶液 溶液 |  溶液 溶液 |
| 丙 | 40℃ | 试管中加入 溶液 溶液 |  蒸馏水 蒸馏水 |
A.实验甲中发生的反应 |
| B.实验甲和乙的实验目的是探究催化剂对反应速率的影响 |
| C.实验甲和丙的实验目的是温度越高,反应速率越快 |
D.实验乙中 的反应速率大于 的反应速率大于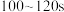 的反应速率,不考虑实验测量误差,二者速率存在差异的主要原因是随着反应的进行 的反应速率,不考虑实验测量误差,二者速率存在差异的主要原因是随着反应的进行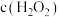 减少 减少 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列对催化剂的理解错误的是
| A.改变反应达到平衡所需的时间 | B.改变反应的活化能 |
| C.改变活化分子百分数 | D.改变反应物的平衡转化率 |
您最近半年使用:0次

 。反应过程中的部分数据如下表所示,下列说法正确的是
。反应过程中的部分数据如下表所示,下列说法正确的是 气氛下乙苯催化脱氢生成苯乙烯的一种反应历程如图所示,下列说法错误的是
气氛下乙苯催化脱氢生成苯乙烯的一种反应历程如图所示,下列说法错误的是


