以赤铁矿(主要成分为Fe2O3,含少量Al2O3)为原料制备无水FeCl2的工艺流程如下。下列说法错误的是
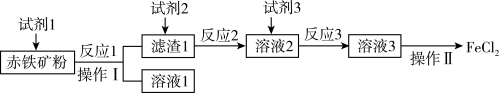

| A.试剂1可用NaOH溶液 |
| B.鉴别溶液2中金属阳离子可用KSCN溶液 |
| C.反应3为化合反应 |
| D.将溶液3蒸干可制得无水FeCl2 |
21-22高三下·湖北·阶段练习 查看更多[6]
湖北省七市(州)2021-2022学年高三下学期3月联合统一调研测试化学试题(已下线)卷05 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)山东省济南大学城实验高中2021-2022学年高三3月阶段性调研化学试题(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)二轮专题强化练 专题8 常见无机物性质的转化(已下线)题型29 以工艺流程为载体考查铁及其化合物之间的转化
更新时间:2022-03-10 15:31:37
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】向200ml 0.1mol/L的FeCl2溶液中加入适量的NaOH溶液,使Fe2+恰好完全沉淀,过滤,小心加热沉淀,直到水分蒸干,再灼烧到质量不再变化,此时固体的质量为
| A.1.14g | B.1.6g | C.2.82g | D.4.36g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究小组设计如下实验制备硫酸亚铁铵。
步骤1:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入 溶液,加热、过滤、洗涤、干燥、称量,质量为
溶液,加热、过滤、洗涤、干燥、称量,质量为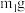 。
。
步骤2: 的制备。将上述铁屑加入到
的制备。将上述铁屑加入到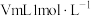 的稀硫酸中,充分反应后过滤并用少量热水洗涤沉淀。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量为
的稀硫酸中,充分反应后过滤并用少量热水洗涤沉淀。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量为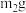 。
。
步骤3:硫酸亚铁铵的制备。计算并称取所需质量的 ,加入“步骤2”的蒸发血中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥。
,加入“步骤2”的蒸发血中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥。
步骤3中准确称取 的质量为
的质量为
步骤1:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入
 溶液,加热、过滤、洗涤、干燥、称量,质量为
溶液,加热、过滤、洗涤、干燥、称量,质量为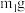 。
。步骤2:
 的制备。将上述铁屑加入到
的制备。将上述铁屑加入到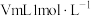 的稀硫酸中,充分反应后过滤并用少量热水洗涤沉淀。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量为
的稀硫酸中,充分反应后过滤并用少量热水洗涤沉淀。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量为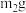 。
。步骤3:硫酸亚铁铵的制备。计算并称取所需质量的
 ,加入“步骤2”的蒸发血中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥。
,加入“步骤2”的蒸发血中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥。步骤3中准确称取
 的质量为
的质量为A. | B.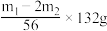 | C.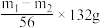 | D.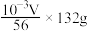 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】8.34 g FeSO4·7H2O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。下列说法不正确的是
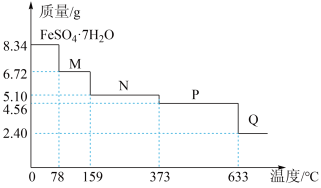

| A.温度为78 ℃时,固体物质M的化学式为FeSO4·4H2O |
| B.取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |
C.在隔绝空气的条件下,M得到P的化学方程式为FeSO4·4H2O FeSO4+4H2O FeSO4+4H2O |
| D.温度为380 ℃时,固体物质P的化学式为FeSO4·H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验过程中,观察不到 颜色变化的是
| A.二氧化硫通入品红溶液中 | B.氢氧化钾溶液中滴加稀盐酸 |
| C.乙烯通入溴的四氯化碳溶液中 | D.氯化铁溶液中滴入 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】向一定量的FeO,Fe,Fe3O4的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现. 若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
| A.11.2 g | B.5.6 g | C.2.8 g | D.1.4g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列各组离子在给定条件下能大量共存的是
A.无色透明的水溶液中:K+、Ba2+、Cl-、 |
B.有 存在的溶液中:Na+、Mg2+、Ba2+、I- 存在的溶液中:Na+、Mg2+、Ba2+、I- |
C.使酚酞试液变红的溶液:K+、Cl-、 、Fe3+ 、Fe3+ |
D.在pH=1中: 、Na+、 、Na+、 、Cl- 、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用NA表示阿伏加 德罗常数的值,下列说法正确的是
| A.l mol/L Na2CO3溶液中,阴离子总数小于NA |
| B.常温下,10 mL pH=1的醋酸溶液中含有的氢离子数大于0.001NA |
| C.电解精炼铜时,若阳极质量减少64 g,则转移到阴极的电子数不一定等于2NA |
| D.相同体积、相同物质的量浓度的CH3COONa溶液和NaCl溶液所含离子数目相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验能够达到相应实验目的的是


| A.利用装置甲制取乙炔并检验乙炔的还原性 |
| B.利用装置乙制取少量乙烯 |
| C.利用装置丙验证苯中是否有碳碳双键 |
| D.利用装置丁可蒸干CuCl2饱和溶液制备无水CuCl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氮化钡( Ba3N2)是一种重要的化学试剂。高温下,向氢化钡(BaH2)中通入氮气反应生成氮化钡,在实验室可用如图装置制备(每个装置只用一次)。已知: Ba3N2遇水反应; BaH2在潮湿空气中能自燃,遇水反应。下列说法不正确的是
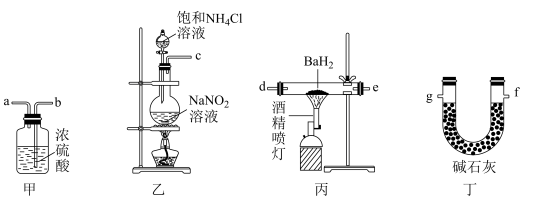

| A.实验时,先点燃装置丙中的酒精喷灯,后点燃装置乙中的酒精灯 |
| B.该实验装置中缺少尾气处理装置 |
| C.按气流方向,装置的连接顺序可为c→b→a→d→e→g |
| D.装置甲中的浓硫酸和装置丁中的碱石灰均可防止水蒸气进入装置丙中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】叠氮酸钠(NaN3)是重要的化工原料。以甲醇、亚硝酸钠等为原料制备NaN3流程如图。已知水合肼(N2H4·H2O)不稳定,具有强还原性。下列描述错误的是
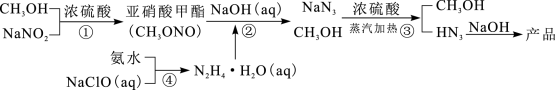

| A.反应①和反应③中浓硫酸作用不同 |
| B.反应②中氧化剂和还原剂的化学计量数比为1:1 |
| C.整个过程中CH3OH物质的量不变,可循环利用 |
| D.反应④应将氨水逐滴滴入NaClO溶液中制备水合肼 |
您最近一年使用:0次

 Cu2S+2FeS+SO2,其简单流程如图所示,下列说法正确的是
Cu2S+2FeS+SO2,其简单流程如图所示,下列说法正确的是


