能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
(1)工业合成氨反应 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知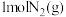 完全反应生成
完全反应生成 可放出92kJ热量。如果将
可放出92kJ热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量_______ (填“大于”“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成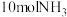 。
。
①反应过程中形成的化学键是_______ (填写“离子键”或“共价键”)。
②一定条件下,能说明该反应进行到最大限度的是_______ (填字母)。
a. 的转化率达到最大值
的转化率达到最大值
b. 、
、 和
和 的体积分数之比为1:3:2
的体积分数之比为1:3:2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
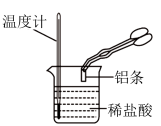
(3)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化,请根据你掌握的反应原理判断,反应后溶液的温度_______ (填“升高”或“降低”),反应物的能量_______ 产物的能量(填写“高于”、“低于”)。
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
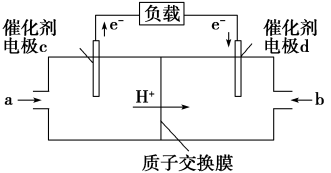
①则电极d是_______ (填“正根”或“负极”),电极c的电极反应式为_______ 。
②若线路中转移 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(1)工业合成氨反应
 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知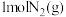 完全反应生成
完全反应生成 可放出92kJ热量。如果将
可放出92kJ热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成
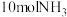 。
。①反应过程中形成的化学键是
②一定条件下,能说明该反应进行到最大限度的是
a.
 的转化率达到最大值
的转化率达到最大值b.
 、
、 和
和 的体积分数之比为1:3:2
的体积分数之比为1:3:2c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化,请根据你掌握的反应原理判断,反应后溶液的温度

(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①则电极d是
②若线路中转移
 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为
更新时间:2022-04-16 21:55:59
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为: N2(g)+3H2(g) 2NH3(g) ΔH= - 92.4 kJ·mol-1。
2NH3(g) ΔH= - 92.4 kJ·mol-1。
I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应。
(1)测得反应放出的热量_________ 92.4kJ(填“小于”,“大于”或“等于”)。
(2)当反应达到平衡时,N2和H2的浓度比是_________ ;N2和H2的转化率比是___________ 。
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量____ 。(填“变大”、“变小”或“不变”)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将____ (填“正向”、“逆向”或“不”)移动。
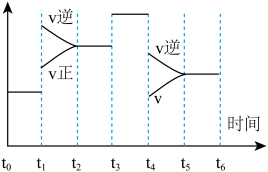
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。
(5)t1时刻,体系中发生变化的条件是_______ 。
A.增大压强B.升高温度C.减小压强D.降低温度 E.加入正催化剂
(6)下列时间段中,氨的百分含量最高的是_______ 。
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
 2NH3(g) ΔH= - 92.4 kJ·mol-1。
2NH3(g) ΔH= - 92.4 kJ·mol-1。I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应。
(1)测得反应放出的热量
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。

(5)t1时刻,体系中发生变化的条件是
A.增大压强B.升高温度C.减小压强D.降低温度 E.加入正催化剂
(6)下列时间段中,氨的百分含量最高的是
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定条件下,在体积为5L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图所示。已知达到平衡后,降低温度,A的体积分数将减小。请回答下列问题。

(1)该反应的化学方程式为_______ 。
(2)该反应的△H___________ 0(填“>”“<”或“=”)。
(3)该反应的反应速率v随时间t的变化关系如图所示:

①在 时刻改变的外界条件是
时刻改变的外界条件是_______ 。
②在恒温恒容密闭容器中发生该反应,下列能作为达到平衡状态的判断依据是_______ 。
A.体系压强不变 B.气体的平均摩尔质量保持不变
C.气体的密度保持不变 D.A的消耗速率等于B的生成速率

(1)该反应的化学方程式为
(2)该反应的△H
(3)该反应的反应速率v随时间t的变化关系如图所示:

①在
 时刻改变的外界条件是
时刻改变的外界条件是②在恒温恒容密闭容器中发生该反应,下列能作为达到平衡状态的判断依据是
A.体系压强不变 B.气体的平均摩尔质量保持不变
C.气体的密度保持不变 D.A的消耗速率等于B的生成速率
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 是一种廉价的碳资源,其综合利用具有重要意义。在容积为
是一种廉价的碳资源,其综合利用具有重要意义。在容积为 的恒容密闭容器中,充入
的恒容密闭容器中,充入 和
和 ,一定条件下发生反应得到
,一定条件下发生反应得到 和
和 ,测得反应物X和
,测得反应物X和 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。

(1) 内,甲醇反应速率
内,甲醇反应速率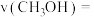
_______ 。(小数点后保留三位有效数字) 。
。
(2)该反应的化学方程式为_______ 。
(3)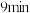 时,
时, 的转化率为
的转化率为_______ 。
(4)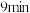 后,保持其他条件不变,向容器中再通入
后,保持其他条件不变,向容器中再通入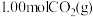 和
和 ,则该反应的速率将
,则该反应的速率将_______ 。(填“增大”、“减小”或“不变”)。
(5)下列可以作为该反应已达到平衡的判据是_______(填标号)。
 是一种廉价的碳资源,其综合利用具有重要意义。在容积为
是一种廉价的碳资源,其综合利用具有重要意义。在容积为 的恒容密闭容器中,充入
的恒容密闭容器中,充入 和
和 ,一定条件下发生反应得到
,一定条件下发生反应得到 和
和 ,测得反应物X和
,测得反应物X和 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。
(1)
 内,甲醇反应速率
内,甲醇反应速率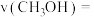
 。
。(2)该反应的化学方程式为
(3)
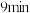 时,
时, 的转化率为
的转化率为(4)
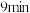 后,保持其他条件不变,向容器中再通入
后,保持其他条件不变,向容器中再通入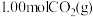 和
和 ,则该反应的速率将
,则该反应的速率将(5)下列可以作为该反应已达到平衡的判据是_______(填标号)。
| A.气体的总压强不变 | B. |
C. 与 与 的浓度相同 的浓度相同 | D.容器内气体的密度不变 |
您最近一年使用:0次
【推荐1】汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。为了模拟反应2NO(g)+2CO(g) N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
(1)前2s内的平均反应速率v(N2)=___ 。
(2)反应达到平衡时CO的转化率为___ 。
(3)下列条件的改变能使上述反应的速率加快的是___ (填字母)。
(4)能说明上述反应达到平衡状态的是___ (填字母)。
(5)平衡时容器内压强为P平,开始时压强为P始,则P平∶P始=__ 。
 N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(mol·L-1) | 10.0 | 8.0 | 7.0 | 6.2 | 4.0 | 4.0 |
| c(CO)/(mol·L-1) | 8.0 | 6.0 | 5.0 | 4.2 | 2.0 | 2.0 |
(2)反应达到平衡时CO的转化率为
(3)下列条件的改变能使上述反应的速率加快的是
| A.降低温度 | B.充入He | C.移走部分CO | D.使用催化剂 |
| A.n(CO2)=2n(N2) | B.混合气体的平均相对分子质量不变 |
| C.气体密度不变 | D.容器内气体压强不变 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物被广泛应用于工业、航天、医药等领域。请回答下列问题:
(1)氨气可作为脱硝剂。在恒温恒容的密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: 。该反应达到平衡状态的标志是___________(填序号)。
。该反应达到平衡状态的标志是___________(填序号)。
(2)一定条件下,在5L密闭容器内,发生反应: ,
, 的物质的量随时间变化的情况如表:
的物质的量随时间变化的情况如表:
①0~2s内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为___________  ;5s时,
;5s时, 的转化率为
的转化率为___________ 。
②为加快反应速率,可以采取的措施是___________ (填序号)。
a.恒容时充入He(g)
b.恒压时充入He(g)
c.恒容时充入 (g)
(g)
(3)已知: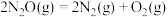 。不同温度
。不同温度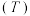 下,
下, 分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度 减小一半时所需的时间),则
减小一半时所需的时间),则
___________ (填“>”“=”或“<”) 。若温度为
。若温度为 、起始压强为
、起始压强为 ,则反应至
,则反应至 时,体系压强
时,体系压强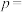
___________ kPa(用 表示)。
表示)。

(1)氨气可作为脱硝剂。在恒温恒容的密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: 。该反应达到平衡状态的标志是___________(填序号)。
。该反应达到平衡状态的标志是___________(填序号)。A.反应速率 |
| B.容器内压强不再变化 |
C.容器内 |
D.12molN—H键断裂的同时生成5molN N键 N键 |
 ,
, 的物质的量随时间变化的情况如表:
的物质的量随时间变化的情况如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
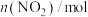 | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为 ;5s时,
;5s时, 的转化率为
的转化率为②为加快反应速率,可以采取的措施是
a.恒容时充入He(g)
b.恒压时充入He(g)
c.恒容时充入
 (g)
(g)(3)已知:
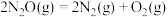 。不同温度
。不同温度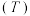 下,
下, 分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度 减小一半时所需的时间),则
减小一半时所需的时间),则
 。若温度为
。若温度为 、起始压强为
、起始压强为 ,则反应至
,则反应至 时,体系压强
时,体系压强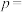
 表示)。
表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

(1)写出该反应的化学方程式________________________________ 。
(2)计算反应开始到10s,用X表示的反应速率是______________ 。
(3)下列叙述中能说明上述反应达到平衡状态的是______________ 。
a.当X与Y的反应速率之比为1:1
b.混合气体中X的质量分数保持不变
c.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v正(Y)与用Z表示的逆反应速率v逆(Z)的关系式是_________________ 。
(5)为使该反应的反应速率增大,可采取的措施是_______ 。
a.适当降低温度 b.扩大容器的体积 c.充入一定量Z

(1)写出该反应的化学方程式
(2)计算反应开始到10s,用X表示的反应速率是
(3)下列叙述中能说明上述反应达到平衡状态的是
a.当X与Y的反应速率之比为1:1
b.混合气体中X的质量分数保持不变
c.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v正(Y)与用Z表示的逆反应速率v逆(Z)的关系式是
(5)为使该反应的反应速率增大,可采取的措施是
a.适当降低温度 b.扩大容器的体积 c.充入一定量Z
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)原电池是把_______ 能转化为_______ 能的装置
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_______ ,A是_______ 。
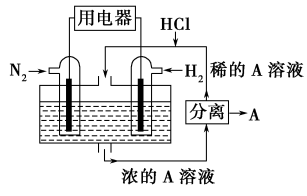
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向_______ (填“从a到b”或“从b到a”),负极发生反应的物质是_______ ,该电极电极反应式为_______ 。

(1)原电池是把
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是

(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是一套电化学实验装置,图中C、D均为铂电极,G是灵敏电流计,其指针总是偏向电源正极。回答下列问题:
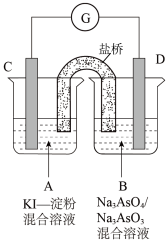
(1)向烧杯B中加入适量较浓的硫酸,发现G的指针向右偏移。则电极C是原电池的_______ (填“正极”或“负极”),电极C上的电极反应式为_______ ,烧杯A中的主要实验现象是_______ 。
(2)一段时间后,再向烧杯B中加入适量质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总反应的离子方程式为 ,此时电极D为
,此时电极D为_______ (填“正极”或“负极”),其电极反应方程式为_______ 。
(3)再过一段时间后,实验装置中的化学反应已经达到化学平衡状态,则此时G的指针指向_______ (填“右边”“左边”或“0刻度”),理由是_______ 。

(1)向烧杯B中加入适量较浓的硫酸,发现G的指针向右偏移。则电极C是原电池的
(2)一段时间后,再向烧杯B中加入适量质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总反应的离子方程式为
 ,此时电极D为
,此时电极D为(3)再过一段时间后,实验装置中的化学反应已经达到化学平衡状态,则此时G的指针指向
您最近一年使用:0次
【推荐1】下列五种物质中,①Ar ②CO2 ③SiO2 ④Ba(OH)2 ⑤K2S,含有共价键的物质有________ (填序号)。分别写出CO2、Ba(OH)2的电子式 ________ 、________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按下列要求填空。
Ⅰ.有下列物质:①Cl2②Na2O2③NaOH④HCl⑤H2O2⑥MgF2⑦NH4Cl
(1)只含共价键的物质是_______ (填序号,下同)。
(2)由离子键和非极性键构成的物质是_______ 。
(3)写出⑤的电子式_______ 。
Ⅱ.下列变化中:①蔗糖溶于水②硫酸氢钾熔化③氨气液化④NaCl溶于水⑤Na2O2溶于水⑥HBr溶于水
(4)只有离子键被破坏的是_______ ,只有共价键被破坏的是_______ 。
(5)既有离子键被破坏,又有共价键被破坏的是_______ 。
Ⅲ.有下列微粒或物质:
① 、
、 、
、 ②石墨、金刚石③35Cl2、37Cl2④
②石墨、金刚石③35Cl2、37Cl2④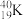 、
、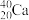 、
、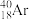
(6)互为同位素的是_______ 。
(7)互为同素异形体的是_______ 。
Ⅰ.有下列物质:①Cl2②Na2O2③NaOH④HCl⑤H2O2⑥MgF2⑦NH4Cl
(1)只含共价键的物质是
(2)由离子键和非极性键构成的物质是
(3)写出⑤的电子式
Ⅱ.下列变化中:①蔗糖溶于水②硫酸氢钾熔化③氨气液化④NaCl溶于水⑤Na2O2溶于水⑥HBr溶于水
(4)只有离子键被破坏的是
(5)既有离子键被破坏,又有共价键被破坏的是
Ⅲ.有下列微粒或物质:
①
 、
、 、
、 ②石墨、金刚石③35Cl2、37Cl2④
②石墨、金刚石③35Cl2、37Cl2④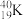 、
、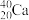 、
、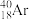
(6)互为同位素的是
(7)互为同素异形体的是
您最近一年使用:0次


 向
向 个电子,则锌片质量减轻
个电子,则锌片质量减轻

