氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的关键环节。
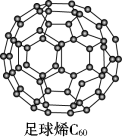
I.C60可用作储存氢气的材料,结构如下图所示。
(1)继C60后,科学家合成了Si60、N60,三者结构相似。下列说法正确的是_______(填序号)
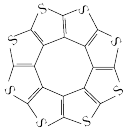
II.最近科学家对一种新型储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如下图所示),每个平面小上下最多可吸附10个H2分子。
(2)C16S8与H2间以_______ (填微粒间作用力类型)结合。
(3)C16S8中C-S键的共用电子对偏向于S,举出一个事实,说明硫的非金属性比碳强(用化学方程式表示):_______ 。
III.LiBH4是储氢材料,已知其由Li+和BH 构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
(4)锂位于元素周期表的_______ 。
(5)由元素周期律能得到_______。(填序号)。
(6)LiBH4中不存在的作用力有_______(填序号)。
(7)氢化锂(LiH)是离子化合物,写出其电子式_______ ,LiH中负离子半径大于正离子半径,其原因是_______ 。
(8)若该反应中释放67.2LH2(标况下),则转移的电子数为_______ 个。
I.C60可用作储存氢气的材料,结构如下图所示。

(1)继C60后,科学家合成了Si60、N60,三者结构相似。下列说法正确的是_______(填序号)
| A.C60、Si60、N60都属于共价晶体 |
| B.C60、Si60、N60分子内共用电子对数目相同 |
| C.由于N-N键能小于N≡N,故N60的稳定性弱于N2 |
| D.由于C-C键长小于Si-Si键,所以C60熔沸点低于Si60 |
II.最近科学家对一种新型储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如下图所示),每个平面小上下最多可吸附10个H2分子。

(2)C16S8与H2间以
(3)C16S8中C-S键的共用电子对偏向于S,举出一个事实,说明硫的非金属性比碳强(用化学方程式表示):
III.LiBH4是储氢材料,已知其由Li+和BH
 构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。(4)锂位于元素周期表的
(5)由元素周期律能得到_______。(填序号)。
| A.碱性:LiOH<NaOH | B.与水反应的剧烈程度:Li<Na |
| C.溶解度:LiOH<NaOH | D.密度:Li<Na |
| A.离子键 | B.共价键 | C.金属键 | D.分子间作用力 |
(8)若该反应中释放67.2LH2(标况下),则转移的电子数为
21-22高一下·上海杨浦·期中 查看更多[4]
上海市控江中学2021-2022学年高一下学期期中考试化学试题(已下线)第四章《物质结构 元素周期律》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测(已下线)第二章分子结构与性质(B卷)
更新时间:2022-04-23 20:59:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是___ ,氧化性最强的单质是___ ,还原性最强的单质是______ 。
(2)最高价氧化物的水化物碱性最强的化合物是___ ,酸性最强的化合物是___ ,呈两性的化合物是____ 。
(3)G与H的气态氢化物稳定性:___ >__ ,说明相应的非金属性:___ >___ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ||||||||
| 2 | D | E | G | I | ||||
| 3 | A | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的化合物是
(3)G与H的气态氢化物稳定性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A,C同周期,B,C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________ 、B:________ 、C:________ 、D:________ 、E:________ 。
(2)用电子式表示离子化合物A2B的形成过程:______________________ 。
(3)写出下列物质的电子式:
①D元素形成的单质:_______________________________________________ 。
②E与B形成的化合物:_____________________________________________ 。
③A,B,E形成的化合物:___________________________________________ 。
④D与E形成的化合物:______________________________________________ 。
⑤C,D,E形成的离子化合物:________________________________________ 。
(1)写出五种元素的元素符号:A:
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
①D元素形成的单质:
②E与B形成的化合物:
③A,B,E形成的化合物:
④D与E形成的化合物:
⑤C,D,E形成的离子化合物:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分
回答下列有关问题:
(1)写出元素符号 :①_______ ,⑤_______ ,⑦_______ 。
(2)表中所列元素中,最活泼的金属元素是_____ (填元素符号 ,下同),最活泼的非金属元素是______ ,最不活泼的元素是______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是________ (填化学式 ,下同),碱性最强的是_________ ,呈两性的是_________ 。
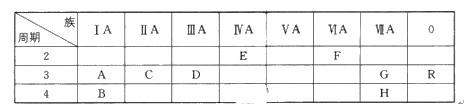
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列有关问题:
(1)写出
(2)表中所列元素中,最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。完成下列填空:
。完成下列填空:
(1)写出 的电子式:
的电子式:_______ 。
(2) 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是_______ 。
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是_______ (填写化学式),所涉及的5种元素中,原子半径最大的是_______ (填写元素符号)。
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: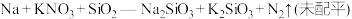 。
。
(4)写出配平后完整的化学方程式_______ 。
(5)结合金属钠的化学性质,说明汽车安全气囊中填充 、
、 的目的
的目的_______ 。
(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的 质量是
质量是_______ (N-14 Na-23)。
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。完成下列填空:
。完成下列填空:(1)写出
 的电子式:
的电子式:(2)
 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是(3)汽车安全气囊填充物的三种物质中属于共价化合物的是
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: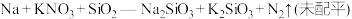 。
。(4)写出配平后完整的化学方程式
(5)结合金属钠的化学性质,说明汽车安全气囊中填充
 、
、 的目的
的目的(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的
 质量是
质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二氧化硫是造成大气污染的主要有害气体之一,二氧化硫尾气处理的方法之一是采用钠一钙联合处理法。
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是_______ (用元素符号填写)。
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:_______________________________________ 。
(3)NaOH的电子式为______________ 。
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式______________ 。
(5)钠一钙联合处理法的优点有________________ 。(任写一点即可)
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:
(3)NaOH的电子式为
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式
(5)钠一钙联合处理法的优点有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.高温时,2NO2(g) 2NO(g)+ O2(g)。根据下列数据计算,当1molNO2分解时,反应会
2NO(g)+ O2(g)。根据下列数据计算,当1molNO2分解时,反应会______ (填“吸收”或“放出”)_____ kJ能量。

Ⅱ.下列物质中:①Na2 O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O2 ⑧Cl2 ⑨NH4Cl,是离子化合物的是
O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O2 ⑧Cl2 ⑨NH4Cl,是离子化合物的是_____________ ,是共价化合物的是_____________ ,含有非极性共价键的物质是_____________ ;Na2O2的电子式:_____________ .N2的结构式:_____________ .
 2NO(g)+ O2(g)。根据下列数据计算,当1molNO2分解时,反应会
2NO(g)+ O2(g)。根据下列数据计算,当1molNO2分解时,反应会
Ⅱ.下列物质中:①Na2
 O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O2 ⑧Cl2 ⑨NH4Cl,是离子化合物的是
O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O2 ⑧Cl2 ⑨NH4Cl,是离子化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在碱金属元素中,锂的金属性最弱,其原因是_______________________________________ 。锂在氧气中燃烧所得产物的化学键类型是________________ 。
(2)在周期表中,锂的性质与镁相似,预测锂在氮气中燃烧的化学方程式:__________________________ 。碳酸锂、硫酸锂的溶解性依次为__________ 、__________ (填“易溶”“微溶”或“难溶”)。
(3)锂在自然界中存在的主要形式为锂辉石(LiAlSi2O6)、锂云母[Li2F2Al2(SiO3)3]等。锂辉石(LiAlSi2O6)中化合价最高的元素和锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素组成的化合物的电子式_________ ,它是____________ (填“离子化合物”或“共价化合物”)。常温常压下,它呈_____ 态,原因是_____________________ 。
(4)四氢硼锂(LiBH4)、四氢铝锂(LiAlH4)都是重要还原剂,在有机合成中用途广泛。比较半径:r(Li+)_____ r(H—),(填“>”“<”或“=”)理由是_____________________________ 。
(2)在周期表中,锂的性质与镁相似,预测锂在氮气中燃烧的化学方程式:
(3)锂在自然界中存在的主要形式为锂辉石(LiAlSi2O6)、锂云母[Li2F2Al2(SiO3)3]等。锂辉石(LiAlSi2O6)中化合价最高的元素和锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素组成的化合物的电子式
(4)四氢硼锂(LiBH4)、四氢铝锂(LiAlH4)都是重要还原剂,在有机合成中用途广泛。比较半径:r(Li+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】富硒酵母、二氧化硅、硫黄等食品添加剂用于食品生产中,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,34Se在元素周期表中的位置为___________ 。
(2)下列说法正确的是___________(填字母)。
(3)短周期元素d、e、f、g、h都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
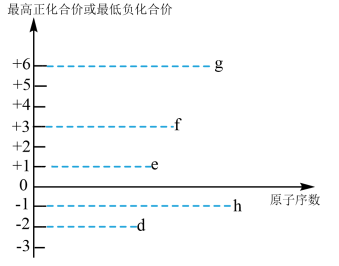
①g的最简单氢化物中含有的化学键类型为___________ (填字母)。
A.离子键 B.非极性共价键 C.极性共价键
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为___________ 。
③e和d组成的淡黄色固体的电子式为___________ 。
④写出一种比较e、f两种元素金属性的方法___________ 。
(1)富硒酵母是一种新型添加剂,34Se在元素周期表中的位置为
(2)下列说法正确的是___________(填字母)。
| A.稳定性:H2Se>H2S>H2O | B.36S与74Se的中子数之和为60 |
| C.酸性:H2SeO4>H2SO4>HClO4 | D.还原性:S2>Se2﹣ |
(3)短周期元素d、e、f、g、h都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:

①g的最简单氢化物中含有的化学键类型为
A.离子键 B.非极性共价键 C.极性共价键
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为
③e和d组成的淡黄色固体的电子式为
④写出一种比较e、f两种元素金属性的方法
您最近一年使用:0次
【推荐1】用Cl2消毒饮用水已有百年历史,近年发现这种方法可能对人体有害。世界环保联盟推荐采用广谱高效消毒剂ClO2。ClO2是黄绿色易爆物,沸点9.90℃。制备ClO2的方法之一表述为:
(1)[ ]KClO3 +[ ] HCl(浓)→[ ] KCl +[ ]ClO2↑+[ ]Cl2↑+[ ]
请完成该化学方程式并配平(未知物化学式和系数填入框内)______________
(2)盐酸在反应中显示出来的性质是_______ (填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1molCl2,则转移的电子的物质的量为_________ mol.
(4)与传统消毒剂Cl2比较,ClO2消毒的效率(以单位质量得到的电子数表示)是Cl2的__ 倍。
(1)[ ]KClO3 +[ ] HCl(浓)→[ ] KCl +[ ]ClO2↑+[ ]Cl2↑+[ ]
请完成该化学方程式并配平(未知物化学式和系数填入框内)
(2)盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1molCl2,则转移的电子的物质的量为
(4)与传统消毒剂Cl2比较,ClO2消毒的效率(以单位质量得到的电子数表示)是Cl2的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.煤炭中的硫以 的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
① ;
;
②_______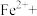 _______
_______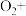 _______H+
_______H+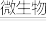 _______
_______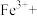 _______;
_______;
③ ;
;
④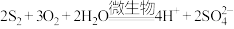 。
。
已知: 中的硫元素为-1价。
中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②的离子方程式配平并补充完整________ 。
(2)反应③中的还原剂是_______ 。
(3)观察上述反应,硫元素最终转化为_______ 从煤炭中分离出来。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化培烧的化学反应为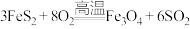 、
、 。若
。若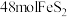 完全反应耗用氧气2934.4L(标准状况),则反应产物中
完全反应耗用氧气2934.4L(标准状况),则反应产物中 与
与 的物质的量之比为
的物质的量之比为_______ 。
Ⅱ.高炉炼铁是冶炼铁的主要方法。
(5)高炉炼铁的尾气中通常含有较多的 气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收
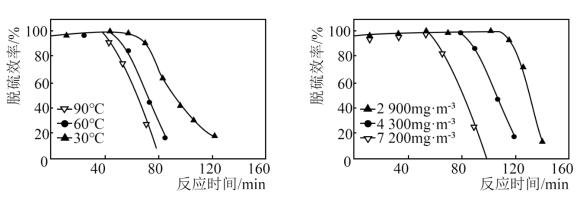
气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收 气体,脱硫效率、尾气中
气体,脱硫效率、尾气中 的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是
的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是_______ ℃;选择合适的质量浓度,经测定40min内共处理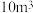 废气,则40min内平均脱硫速率为
废气,则40min内平均脱硫速率为_______ 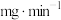 。
。
Ⅲ.完成下列问题
(6)工业上用黄铜矿( )冶炼铜,副产品中也有
)冶炼铜,副产品中也有 ,冶炼铜的化学反应为
,冶炼铜的化学反应为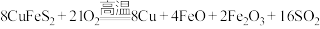 。当
。当 中Fe的化合价为+2价,反应中被还原的元素是
中Fe的化合价为+2价,反应中被还原的元素是_______ (填元素符号)。当生成0.8mol铜时,该反应转移的电子数是_______ 。
 的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为①
 ;
;②_______
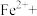 _______
_______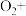 _______H+
_______H+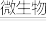 _______
_______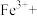 _______;
_______;③
 ;
;④
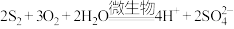 。
。已知:
 中的硫元素为-1价。
中的硫元素为-1价。回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②的离子方程式配平并补充完整
(2)反应③中的还原剂是
(3)观察上述反应,硫元素最终转化为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化培烧的化学反应为
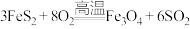 、
、 。若
。若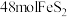 完全反应耗用氧气2934.4L(标准状况),则反应产物中
完全反应耗用氧气2934.4L(标准状况),则反应产物中 与
与 的物质的量之比为
的物质的量之比为Ⅱ.高炉炼铁是冶炼铁的主要方法。
(5)高炉炼铁的尾气中通常含有较多的
 气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收
气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收 气体,脱硫效率、尾气中
气体,脱硫效率、尾气中 的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是
的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是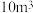 废气,则40min内平均脱硫速率为
废气,则40min内平均脱硫速率为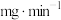 。
。
Ⅲ.完成下列问题
(6)工业上用黄铜矿(
 )冶炼铜,副产品中也有
)冶炼铜,副产品中也有 ,冶炼铜的化学反应为
,冶炼铜的化学反应为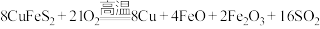 。当
。当 中Fe的化合价为+2价,反应中被还原的元素是
中Fe的化合价为+2价,反应中被还原的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铜是生物必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式_____________________________ 。
(2)为了保护环境和节约资源,通常先用 和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式
和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式__________________________ 。
(3)工业上以黄铜矿为原料,采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应: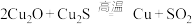 ,该反应的氧化剂是
,该反应的氧化剂是________ ;当生成 时,反应中转移的电子为
时,反应中转移的电子为______  。
。
(4)研究性学习小组用“间接碘量法”测定某试样中 (不含能与I-反应的氧化性杂质)的含量,取
(不含能与I-反应的氧化性杂质)的含量,取 试样配成
试样配成 溶液,每次取
溶液,每次取 ,滴加
,滴加 溶液后有白色碘化物沉淀生成,写出该反应的离子方程式
溶液后有白色碘化物沉淀生成,写出该反应的离子方程式__________________________ 。
(5)继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫化硫酸钠标准溶液滴定,发生反应的化学方程式为: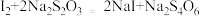 ,平均消耗
,平均消耗 的
的 溶液
溶液 。则试样中
。则试样中 的质量分数为
的质量分数为______________________ 。
(1)写出铜与稀硝酸反应的化学方程式
(2)为了保护环境和节约资源,通常先用
 和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式
和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式(3)工业上以黄铜矿为原料,采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应:
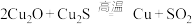 ,该反应的氧化剂是
,该反应的氧化剂是 时,反应中转移的电子为
时,反应中转移的电子为 。
。(4)研究性学习小组用“间接碘量法”测定某试样中
 (不含能与I-反应的氧化性杂质)的含量,取
(不含能与I-反应的氧化性杂质)的含量,取 试样配成
试样配成 溶液,每次取
溶液,每次取 ,滴加
,滴加 溶液后有白色碘化物沉淀生成,写出该反应的离子方程式
溶液后有白色碘化物沉淀生成,写出该反应的离子方程式(5)继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫化硫酸钠标准溶液滴定,发生反应的化学方程式为:
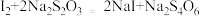 ,平均消耗
,平均消耗 的
的 溶液
溶液 。则试样中
。则试样中 的质量分数为
的质量分数为
您最近一年使用:0次