一种制取电池级二氧化锰的工艺流程如下图:
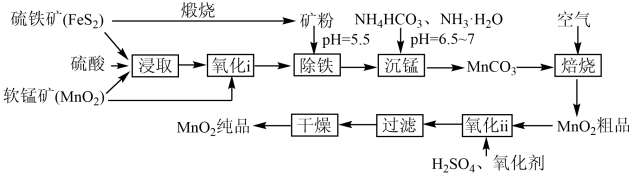
回答下列问题:
(1)“浸取”过程有硫单质生成,写出该过程中主要反应的化学方程式_______ 。
(2)“氧化ⅰ”过程软锰矿的作用是_______ 。“氧化ⅱ”过程中,将Mn(Ⅱ)转化为Mn(Ⅳ)的最适宜氧化剂是_______ (填标号)。
a. b.
b. c.
c.
(3)工业上煅烧硫铁矿产生的 气体可以用石灰乳吸收。常温下,测得
气体可以用石灰乳吸收。常温下,测得 与水形成的浊液pH为9,若忽略
与水形成的浊液pH为9,若忽略 的第二步水解,则
的第二步水解,则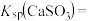
_______ (保留三位有效数字)[已知:室温下亚硫酸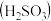 的电离平衡常数
的电离平衡常数 ,
, ]
]
(4)“沉锰”过程 转化为
转化为 的离子方程式为
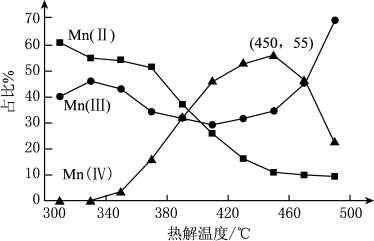
的离子方程式为_______ 。在一定空气流速下,相同时间内“焙烧” ,产物中不同价态Mn的占比随热解温度的变化如图。“焙烧”过程中涉及如下化学反应:
,产物中不同价态Mn的占比随热解温度的变化如图。“焙烧”过程中涉及如下化学反应:
①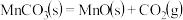
②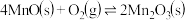

③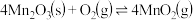

为了增大产物中 的占比,可以采用的措施是
的占比,可以采用的措施是_______ (答出两条)。将制备获得的电池级二氧化锰用于构建水系锌锰电池,其工作原理为: ,放电时正极的电极反应式为
,放电时正极的电极反应式为_______ 。
(5)用氧化还原法测定 纯品纯度(杂质不参与下列反应):称取
纯品纯度(杂质不参与下列反应):称取 样品0.1000g,试样经过过氧化钠碱熔后,得到
样品0.1000g,试样经过过氧化钠碱熔后,得到 溶液,配成溶液经加热煮沸除去过氧化物,酸化溶液,此时
溶液,配成溶液经加热煮沸除去过氧化物,酸化溶液,此时 歧化为
歧化为 和
和 ,过滤除去
,过滤除去 ,用
,用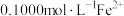 标准溶液滴定
标准溶液滴定 ,用去37.00mL,则样品中
,用去37.00mL,则样品中 的质量分数为
的质量分数为_______ (保留3位有效数字)。

回答下列问题:
(1)“浸取”过程有硫单质生成,写出该过程中主要反应的化学方程式
(2)“氧化ⅰ”过程软锰矿的作用是
a.
 b.
b. c.
c.
(3)工业上煅烧硫铁矿产生的
 气体可以用石灰乳吸收。常温下,测得
气体可以用石灰乳吸收。常温下,测得 与水形成的浊液pH为9,若忽略
与水形成的浊液pH为9,若忽略 的第二步水解,则
的第二步水解,则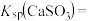
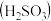 的电离平衡常数
的电离平衡常数 ,
, ]
](4)“沉锰”过程
 转化为
转化为 的离子方程式为
的离子方程式为 ,产物中不同价态Mn的占比随热解温度的变化如图。“焙烧”过程中涉及如下化学反应:
,产物中不同价态Mn的占比随热解温度的变化如图。“焙烧”过程中涉及如下化学反应:
①
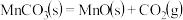
②
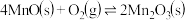

③
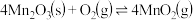

为了增大产物中
 的占比,可以采用的措施是
的占比,可以采用的措施是 ,放电时正极的电极反应式为
,放电时正极的电极反应式为(5)用氧化还原法测定
 纯品纯度(杂质不参与下列反应):称取
纯品纯度(杂质不参与下列反应):称取 样品0.1000g,试样经过过氧化钠碱熔后,得到
样品0.1000g,试样经过过氧化钠碱熔后,得到 溶液,配成溶液经加热煮沸除去过氧化物,酸化溶液,此时
溶液,配成溶液经加热煮沸除去过氧化物,酸化溶液,此时 歧化为
歧化为 和
和 ,过滤除去
,过滤除去 ,用
,用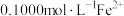 标准溶液滴定
标准溶液滴定 ,用去37.00mL,则样品中
,用去37.00mL,则样品中 的质量分数为
的质量分数为
2022·山东济宁·二模 查看更多[4]
山东省济宁市2022届高三第二次模拟考试化学试题湖北省武汉市第二中学2022届高三5月全仿真模拟考试(一)化学试题湖南省长沙市长沙县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)微专题17 热点金属及其化合物制备流程(V、Cr、Mn、Co、Ni)-备战2023年高考化学一轮复习考点微专题
更新时间:2022-04-29 11:34:10
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高压氢还原法可直接从溶液中提取金属。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu粉的工艺流程如图。
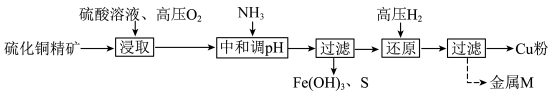
(1)浸取前,通常将硫化铜精矿粉碎的目的是_________ 。
(2)写出通入高压O2时硫化铜发生反应的化学方程式:_________ 。
(3)第一次过滤后的溶液中所含的阳离子有Cu2+、H+、_______ 、_______ 。通入高压H2时发生的反应中氧化剂和还原剂的物质的量之比为________ 。
(4)通入高压H2时,Cu2+先于M2+被还原出来的原因为________ 。
(5)若取10kg质量分数为84%的硫化铜精矿经过上述流程(铜元素在整个流程中损失率为5%,则可制得Cu粉的质量为________ kg。

(1)浸取前,通常将硫化铜精矿粉碎的目的是
(2)写出通入高压O2时硫化铜发生反应的化学方程式:
(3)第一次过滤后的溶液中所含的阳离子有Cu2+、H+、
(4)通入高压H2时,Cu2+先于M2+被还原出来的原因为
(5)若取10kg质量分数为84%的硫化铜精矿经过上述流程(铜元素在整个流程中损失率为5%,则可制得Cu粉的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从钨渣中提取钪过程中产出大量含有硫酸锰、硫酸亚铁和硫酸的废液。用菱锰矿(主要含MnO2及Fe2O3、CaO、Al2O3、SiO2,CuO等杂质)处理废液制备高纯MnSO4·H2O的实验如下:
①在2000 mL烧杯中加入提钪废液,加热升温,搅拌下按一定比例加入锰矿,反应80 min。
②搅拌下加入新制备的碳酸锰浆液调节pH在5.0~5.5,过滤。
③将滤液加热升温至90℃,搅拌下加入适量硫化锰浆液,继续煮沸60 min,静置过滤除去不溶物。在滤液中于室温下加入适量新制备的水合二氧化锰,吸附除硅继续搅拌 ,静置过滤除去不溶物。
,静置过滤除去不溶物。
④将除硅后的滤液加热煮沸,搅拌下滴加适量氟化锰饱和溶液,继续搅拌30 min,静置、过滤除去不溶物。
⑤将滤液在烧杯中加热,过程中用玻璃棒不断搅拌,至液体刚好完全蒸干时停止加热,冷却得高纯MnSO4·H2O。
回答下列问题:
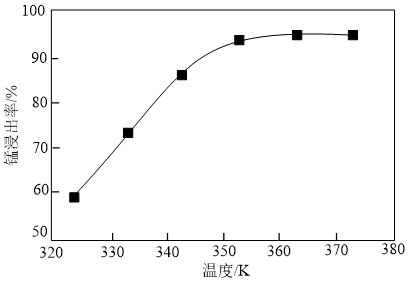
(1)步骤①中反应温度对锰浸出率的影响如图,反应温度应维持在_______ ℃,其中发生的氧化还原反应的离子方程式为_______ 。
(2)当溶液中可溶组分浓度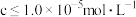 时,可认为已除尽。已知下列物质的
时,可认为已除尽。已知下列物质的
步骤②中滤渣主要成分是_______ ,步骤③不溶物主要成分是_______ 。
(3)步骤④反应的离子方程式为_______ 。
(4)已知MnSO4·H2O的溶解度随温度变化如图,实验中步骤①②③④是正确的,步骤⑤有错误,步骤⑤的正确操作为:_______ 。
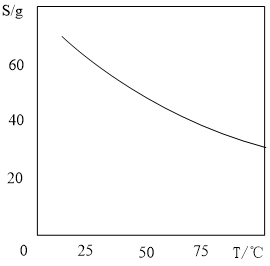
①在2000 mL烧杯中加入提钪废液,加热升温,搅拌下按一定比例加入锰矿,反应80 min。
②搅拌下加入新制备的碳酸锰浆液调节pH在5.0~5.5,过滤。
③将滤液加热升温至90℃,搅拌下加入适量硫化锰浆液,继续煮沸60 min,静置过滤除去不溶物。在滤液中于室温下加入适量新制备的水合二氧化锰,吸附除硅继续搅拌
 ,静置过滤除去不溶物。
,静置过滤除去不溶物。④将除硅后的滤液加热煮沸,搅拌下滴加适量氟化锰饱和溶液,继续搅拌30 min,静置、过滤除去不溶物。
⑤将滤液在烧杯中加热,过程中用玻璃棒不断搅拌,至液体刚好完全蒸干时停止加热,冷却得高纯MnSO4·H2O。
回答下列问题:
(1)步骤①中反应温度对锰浸出率的影响如图,反应温度应维持在

(2)当溶液中可溶组分浓度
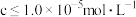 时,可认为已除尽。已知下列物质的
时,可认为已除尽。已知下列物质的
| 物质 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Mn(OH)2 | CaF2 |
| Ksp |  |  |  |  | 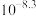 |
(3)步骤④反应的离子方程式为
(4)已知MnSO4·H2O的溶解度随温度变化如图,实验中步骤①②③④是正确的,步骤⑤有错误,步骤⑤的正确操作为:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组研究含铁元素的盐类物质的制备、保存和性质。
实验I.配制 溶液:向
溶液:向 溶液中加入足量铁粉,充分振荡,备用。
溶液中加入足量铁粉,充分振荡,备用。
(1) 溶液与铁粉反应的离子方程式为
溶液与铁粉反应的离子方程式为_______ 。
(2)在老师的指导下,配制的 溶液底部仍保留一层铁粉,请说明该操作的必要性
溶液底部仍保留一层铁粉,请说明该操作的必要性_______ 。
实验II.通过 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
(3)实验i中滴加 溶液后出现的一系列现象是
溶液后出现的一系列现象是_______ ;请用化学或离子方程式说明 溶液中滴加碱溶液后出现此系列现象的原因:
溶液中滴加碱溶液后出现此系列现象的原因: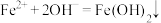 、
、_______ 。
(4)探究实验ⅱ中先滴加 溶液时
溶液时 溶液中是否发生了反应?
溶液中是否发生了反应?
①向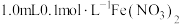 溶液中
溶液中_______ (填写具体实验方法),溶液立即变红,说明加酸时溶液中发生了反应,生成了 。
。
②推测溶液中产生 ,的可能原因有两种:
,的可能原因有两种:
a.酸性条件下,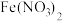 溶液中的
溶液中的 被
被 氧化。
氧化。
b.酸性条件下, 可能被空气中的
可能被空气中的 氧化,写出相应的离子反应方程式
氧化,写出相应的离子反应方程式_______ 。
实验I.配制
 溶液:向
溶液:向 溶液中加入足量铁粉,充分振荡,备用。
溶液中加入足量铁粉,充分振荡,备用。(1)
 溶液与铁粉反应的离子方程式为
溶液与铁粉反应的离子方程式为(2)在老师的指导下,配制的
 溶液底部仍保留一层铁粉,请说明该操作的必要性
溶液底部仍保留一层铁粉,请说明该操作的必要性实验II.通过
 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
 | 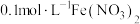 溶液 溶液 | 实验i:先滴加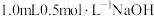 溶液;再滴加 溶液;再滴加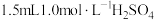 溶液 溶液 | i.滴加 溶液后 ;加酸后溶液变为黄色 溶液后 ;加酸后溶液变为黄色 |
实验ⅱ:先滴加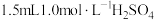 溶液;再滴加 溶液;再滴加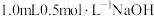 溶液 溶液 | ii.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 | ||
 溶液后出现的一系列现象是
溶液后出现的一系列现象是 溶液中滴加碱溶液后出现此系列现象的原因:
溶液中滴加碱溶液后出现此系列现象的原因: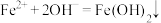 、
、(4)探究实验ⅱ中先滴加
 溶液时
溶液时 溶液中是否发生了反应?
溶液中是否发生了反应?①向
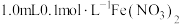 溶液中
溶液中 。
。②推测溶液中产生
 ,的可能原因有两种:
,的可能原因有两种:a.酸性条件下,
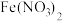 溶液中的
溶液中的 被
被 氧化。
氧化。b.酸性条件下,
 可能被空气中的
可能被空气中的 氧化,写出相应的离子反应方程式
氧化,写出相应的离子反应方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】乙醛是一种重要的脂肪族化合物,在工业、农业、医药、食品和饲料添加剂等领域具有非常广泛的应用。目前,常用乙醇脱氢来制备。
I(乙醇氧化脱氢):2CH3CH2OH(g)+O2(g) 2CH3CHO(g)+2H2O(g) ∆H1
2CH3CHO(g)+2H2O(g) ∆H1
II(乙醇直接脱氢):CH3CH2OH(g) CH3CHO(g)+H2(g) ∆H2
CH3CHO(g)+H2(g) ∆H2
(1)已知相关共价键的键能数据如表:
∆H1=___________ kJ·mol-1
(2)在恒温恒容下,如果从反应物出发建立平衡,不能说明反应I(乙醇氧化脱氢)达到平衡状态的是___________ 。(填选项字母)
A、体系压强不再变化 B、v正(CH3CH2OH)=2v逆(O2)
C、混合气体的密度保持不变 D、混合气体平均相对分子质量保持不变
(3)对于反应II(乙醇直接脱氢),T1℃,P1kPa条件下,向一容积可变的密闭容器中,充入2mol乙醇气体,达平衡后乙醇的转化率为50%,容器体积为2L。T1℃,P2 kPa条件下,充入2mol乙醇气体,平衡后乙醇的转化率为60%,此时容器的体积为___________ L。
(4)乙醇直接脱氢反应中Cu基催化剂是最常用的催化剂体系之一、研究者研究了用Cu35Zn25Al43作催化剂时不同温度对乙醇直接脱氢反应性能的影响,图象如图:
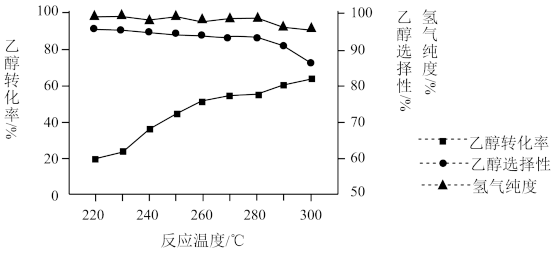
最适宜的温度为___________ ;结合图象说明选择该温度的理由___________ 。
(5)乙醇直接脱氢反应中铜基催化剂有失活的缺点。大连物化所的研究者设计了一种多级海胆状结构Cu-MFI-AE催化剂,在乙醇催化中展示了较高的乙醛选择性、稳定性。催化剂表面上反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。

写出该历程中最大能垒对应步骤的化学方程式___________ 。
I(乙醇氧化脱氢):2CH3CH2OH(g)+O2(g)
 2CH3CHO(g)+2H2O(g) ∆H1
2CH3CHO(g)+2H2O(g) ∆H1II(乙醇直接脱氢):CH3CH2OH(g)
 CH3CHO(g)+H2(g) ∆H2
CH3CHO(g)+H2(g) ∆H2(1)已知相关共价键的键能数据如表:
| 共价键 | C-H | O-H | C-O | C=O | O=O | C-C |
| 键能(kJ·mol-1) | 413 | 462 | 351 | 745 | 497 | 348 |
∆H1=
(2)在恒温恒容下,如果从反应物出发建立平衡,不能说明反应I(乙醇氧化脱氢)达到平衡状态的是
A、体系压强不再变化 B、v正(CH3CH2OH)=2v逆(O2)
C、混合气体的密度保持不变 D、混合气体平均相对分子质量保持不变
(3)对于反应II(乙醇直接脱氢),T1℃,P1kPa条件下,向一容积可变的密闭容器中,充入2mol乙醇气体,达平衡后乙醇的转化率为50%,容器体积为2L。T1℃,P2 kPa条件下,充入2mol乙醇气体,平衡后乙醇的转化率为60%,此时容器的体积为
(4)乙醇直接脱氢反应中Cu基催化剂是最常用的催化剂体系之一、研究者研究了用Cu35Zn25Al43作催化剂时不同温度对乙醇直接脱氢反应性能的影响,图象如图:

最适宜的温度为
(5)乙醇直接脱氢反应中铜基催化剂有失活的缺点。大连物化所的研究者设计了一种多级海胆状结构Cu-MFI-AE催化剂,在乙醇催化中展示了较高的乙醛选择性、稳定性。催化剂表面上反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。

写出该历程中最大能垒对应步骤的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】费托合成是以合成气(CO 和 H2 混合气体)为原料在催化剂和适当条件下合成烯烃(C2~C4)以及烷烃(CH4、C5~C11、C12~C18等,用Cn H2n+2表示)的工艺过程。
已知:① 2CO(g) +O2(g) =2CO2 (g) △H1 =a
②2H2(g) + O2(g)=2H2O(g) △H2 =b
③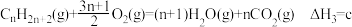
回答下列问题:
(1)反应(2n +1)H2 (g)+nCO(g)=CnH2n+2(g)+nH2O(g)的 △H_____ 。(用含有a、b、c、n 的式子表示)
(2)费托合成产物碳原子分布遵循 ASF 分布规律。碳链增长因子(α)是描述产物分布的重要参数,不同数值对应不同的产物分布。ASF 分布规律如图,若要控制 C2~C4的质量分数 0.48~0.57,则需控制碳链增长因子(α)的范围是________ 。
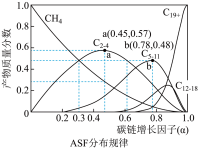
(3)近期,我国中科院上海高等研究院在费托合成烃的催化剂上取得重大进展。如图所示,Co2C作催化剂的规律是:选择球形催化剂时_____ ,选择平行六面体催化剂时_____ 。

(4)中科院大连化物所研究团队直接利用CO2与H2合成甲醇。一定条件下,向 2L 恒容密闭容器中充入1molCO2和 2mol H2发生反应“CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H”。CO2的平衡转化率(α)与温度(T)的关系如图所示。
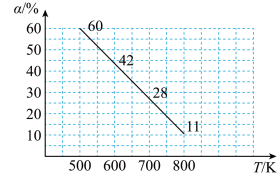
①判断△H_______ 0。(填“大于”“小于”或“等于”)
②500 K 时,反应 5 min 达到平衡。计算 0~5 min 用H2O 表示该反应的化学反应速率为_________ ,该反应的平衡常数为__________ 。
③500 K 时,测定各物质的物质的量浓度分别为 c(CO2)=0.4 mol/L、c(H2) = 0.2 mol/L、c(CH3OH) = 0.6 mol/L、c(H2O) = 0. 6 mol/L,此时反应____ (填“是”或“否”) 达到平衡,理由是_____ 。
④一定条件下,对于反应 CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g)。下列说法中不能表明反应达到平衡的是_____ 。
a.恒温恒容下,c(CH3OH)=c(H2O)
b.恒温恒容下,体系的压强保持不变
c.恒温恒容下,体系的平均摩尔质量不变
d.相同时间内,断裂 H-H 键和断裂 H-O 键之比 1:1
已知:① 2CO(g) +O2(g) =2CO2 (g) △H1 =a
②2H2(g) + O2(g)=2H2O(g) △H2 =b
③
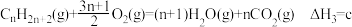
回答下列问题:
(1)反应(2n +1)H2 (g)+nCO(g)=CnH2n+2(g)+nH2O(g)的 △H
(2)费托合成产物碳原子分布遵循 ASF 分布规律。碳链增长因子(α)是描述产物分布的重要参数,不同数值对应不同的产物分布。ASF 分布规律如图,若要控制 C2~C4的质量分数 0.48~0.57,则需控制碳链增长因子(α)的范围是

(3)近期,我国中科院上海高等研究院在费托合成烃的催化剂上取得重大进展。如图所示,Co2C作催化剂的规律是:选择球形催化剂时

(4)中科院大连化物所研究团队直接利用CO2与H2合成甲醇。一定条件下,向 2L 恒容密闭容器中充入1molCO2和 2mol H2发生反应“CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H”。CO2的平衡转化率(α)与温度(T)的关系如图所示。

①判断△H
②500 K 时,反应 5 min 达到平衡。计算 0~5 min 用H2O 表示该反应的化学反应速率为
③500 K 时,测定各物质的物质的量浓度分别为 c(CO2)=0.4 mol/L、c(H2) = 0.2 mol/L、c(CH3OH) = 0.6 mol/L、c(H2O) = 0. 6 mol/L,此时反应
④一定条件下,对于反应 CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g)。下列说法中不能表明反应达到平衡的是
a.恒温恒容下,c(CH3OH)=c(H2O)
b.恒温恒容下,体系的压强保持不变
c.恒温恒容下,体系的平均摩尔质量不变
d.相同时间内,断裂 H-H 键和断裂 H-O 键之比 1:1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】(1)目前,我国采用“接触法治制硫酸。有关接触法制硫酸的下列说法中,正确的是__________ 。
E.转化器中采取高温是为了提高催化剂的活性和提高SO2的转化率
(2)硫酸工厂排放的尾气中含少量二氧化硫。为防止污染大气,在排放前必须进行尾气处理并设法进行综合利用。硫酸工厂排放尾气中的SO2可用足量石灰乳吸收,然后再用稀硫酸处理。
①写出上述过程发生反应的化学方程式:__________ ;
②若某硫酸厂每天排放的1万立方米(标准状况)尾气中含0.2%(体积分数)的SO2,通过上述方法处理,理论上需生石灰__________ kg。

(3)某研究小组用NaOH溶液吸收硫酸厂尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图所示,a、b离子交换膜将电解槽分为三个区域,电极材料为石墨。
①图中b表示__________ (填“阴”或“阳”)离子交换膜。A~E分别代表生产中的原料或产品,其中C为硫酸,则E表示__________ ;
②阳极的电极反应式为__________ 。
| A.二氧化硫的接触氧化在接触室中发生 |
| B.吸收塔中得到的硫酸质量分数为98% |
| C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4% |
| D.转化器中适宜条件是V2O5,催化剂、高温、常压 |
E.转化器中采取高温是为了提高催化剂的活性和提高SO2的转化率
(2)硫酸工厂排放的尾气中含少量二氧化硫。为防止污染大气,在排放前必须进行尾气处理并设法进行综合利用。硫酸工厂排放尾气中的SO2可用足量石灰乳吸收,然后再用稀硫酸处理。
①写出上述过程发生反应的化学方程式:
②若某硫酸厂每天排放的1万立方米(标准状况)尾气中含0.2%(体积分数)的SO2,通过上述方法处理,理论上需生石灰

(3)某研究小组用NaOH溶液吸收硫酸厂尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图所示,a、b离子交换膜将电解槽分为三个区域,电极材料为石墨。
①图中b表示
②阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】三氯化六氨合钴{[Co(NH3)6]Cl3}是合成其他含钴配合物的重要原料。工业上以水钴矿(主要成分为Co2O3,还含有少量的Fe2O3、Al2O3、MgO、CaO、SiO2)为原料制备三氯化六氨合钴晶体。

已知:①Co2O3具有很强的氧化性,其还原产物为Co2+;碱性条件下,Co2+能被O2氧化;
②25℃时相关物质的Ksp如表:
请回答下列问题:
(1)“浸取”时,Co2O3发生反应的离子方程式为_______ 。
(2)滤渣II的成分是Al(OH)3和Fe(OH)3,“氧化”时,NaClO3溶液的作用是_______ 。
(3)“除杂”时,CoF2可将Ca2+、Mg2+转化为沉淀除去,若所得滤液中Mg2+刚好沉淀完全,则此时滤液中c(Ca2+)=_______ mol·L-1(溶液中离子浓度≤l0-5mol·L-1时沉淀完全)。
(4)“转化”时,Co2+转化为[Co(NH3)6]3+,而水浴控温在50~60℃,温度不能过高的原因是_______ ,其反应的离子方程式为_______ 。
(5)为测定产品中钴元素的含量,取ag样品于烧杯中,加水溶解,加入足量的NaOH溶液,加热至沸腾,将[Co(NH3)6]Cl3完全转化为Co(OH)3,冷却后加足量KI固体和HCl溶液,充分反应一段时间后,将烧瓶中的溶液全部传移至250.00mL容量瓶中,定容。取25.00mL试样加入到锥形瓶中,加入淀粉作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,滴定至终点消耗Na2S2O3溶液的体积为VmL(已知:2Co3++2I-=2Co2++I2,I2+2 =2I-+
=2I-+ )。
)。
①滴定终点的现象是_______ 。
②该产品中钴元素的质量分数为_______ (用含a、V的式子表示)。

已知:①Co2O3具有很强的氧化性,其还原产物为Co2+;碱性条件下,Co2+能被O2氧化;
②25℃时相关物质的Ksp如表:
| 物质 | Co(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | MgF2 | CaF2 |
| Ksp | 1×10-13.8 | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-10 | 5×10-11 |
(1)“浸取”时,Co2O3发生反应的离子方程式为
(2)滤渣II的成分是Al(OH)3和Fe(OH)3,“氧化”时,NaClO3溶液的作用是
(3)“除杂”时,CoF2可将Ca2+、Mg2+转化为沉淀除去,若所得滤液中Mg2+刚好沉淀完全,则此时滤液中c(Ca2+)=
(4)“转化”时,Co2+转化为[Co(NH3)6]3+,而水浴控温在50~60℃,温度不能过高的原因是
(5)为测定产品中钴元素的含量,取ag样品于烧杯中,加水溶解,加入足量的NaOH溶液,加热至沸腾,将[Co(NH3)6]Cl3完全转化为Co(OH)3,冷却后加足量KI固体和HCl溶液,充分反应一段时间后,将烧瓶中的溶液全部传移至250.00mL容量瓶中,定容。取25.00mL试样加入到锥形瓶中,加入淀粉作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,滴定至终点消耗Na2S2O3溶液的体积为VmL(已知:2Co3++2I-=2Co2++I2,I2+2
 =2I-+
=2I-+ )。
)。①滴定终点的现象是
②该产品中钴元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以软锰矿粉(主要含有MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制备高纯MnO2的流程如下图所示:

(1)“酸浸”实验中,锰的浸出率结果如下图所示。由图可知,软锰矿粉酸浸的适宜条件是硫酸浓度为___________ mol/L、温度为___________ ℃。

(2)酸浸后,锰主要以Mn2+的形式存在,写出相应的离子方程式___________ 。
(3)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,为了使Fe3+、Al3+沉淀完全,调节pH的最小值约为___________ (保留小数点后一位)。(已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=2.0×10-33,lg2=0.3)
(4)从滤渣中分离出Al(OH)3,可用如图所示方法,试剂X是___________ 。

(5)加入碳酸氢铵产生沉淀的过程称为“沉锰”,“过滤II”所得滤渣为MnCO3。
①“沉锰”过程中放出CO2,反应的离子方程式为___________ 。
②“沉锰”过程中沉锰速率与温度的关系如图所示。

当温度高于60℃时,沉锰速率随着温度升高而减慢的原因是___________ 。
(6)写出焙烧过程的化学方程式___________ 。

(1)“酸浸”实验中,锰的浸出率结果如下图所示。由图可知,软锰矿粉酸浸的适宜条件是硫酸浓度为

(2)酸浸后,锰主要以Mn2+的形式存在,写出相应的离子方程式
(3)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,为了使Fe3+、Al3+沉淀完全,调节pH的最小值约为
(4)从滤渣中分离出Al(OH)3,可用如图所示方法,试剂X是

(5)加入碳酸氢铵产生沉淀的过程称为“沉锰”,“过滤II”所得滤渣为MnCO3。
①“沉锰”过程中放出CO2,反应的离子方程式为
②“沉锰”过程中沉锰速率与温度的关系如图所示。

当温度高于60℃时,沉锰速率随着温度升高而减慢的原因是
(6)写出焙烧过程的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】硫酸铅(PbSO4),制造铅蓄电池的一种原料;以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,可实现铅的再生利用。
(1)铅蓄电池中需要配制5.3 mol∙L−1的H2SO4溶液,需要的仪器有玻璃棒、___________ (从下列图中选择,写出名称)。

(2)工业上以PbS为原料可以制取PbSO4,80℃时浸取,将PbS与盐酸、MnO2和饱和食盐水一起浸取,PbS反应后生成 和S。
和S。
①写出PbS反应的离子方程式:___________ 。
②浸取时应控制盐酸的浓度。其他条件一定,若盐酸浓度过大,铅元素的浸出率反而下降,原因是___________ 。
(3)用废旧铅酸电池中的含铅废料,制备高纯PbO,实现铅的再生利用的过程中,

过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++PbO2+4H++ =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2O
ii:2Fe3++Pb+ =2Fe2++PbSO4
=2Fe2++PbSO4
下列实验方案可证实上述催化过程。请将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.___________ 。
(4)已知:Ksp(PbCO3)=1.5×10−13,Ksp(PbSO4)=1.8×10−8.在某制备过程中,经检测,过滤出的PbCO3沉淀中混有PbSO4,则该滤液中 =
=___________ 。
(5)以铅蓄电池为电源,电解二氧化碳酸性溶液可制得丙烯(如图)。

①Y极与电源___________ (填“正极”或“负极”)相连。
②该离子交换膜为___________ 膜。
③X极的电极反应式为___________ 。
(1)铅蓄电池中需要配制5.3 mol∙L−1的H2SO4溶液,需要的仪器有玻璃棒、

(2)工业上以PbS为原料可以制取PbSO4,80℃时浸取,将PbS与盐酸、MnO2和饱和食盐水一起浸取,PbS反应后生成
 和S。
和S。①写出PbS反应的离子方程式:
②浸取时应控制盐酸的浓度。其他条件一定,若盐酸浓度过大,铅元素的浸出率反而下降,原因是
(3)用废旧铅酸电池中的含铅废料,制备高纯PbO,实现铅的再生利用的过程中,

过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++PbO2+4H++
 =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2Oii:2Fe3++Pb+
 =2Fe2++PbSO4
=2Fe2++PbSO4下列实验方案可证实上述催化过程。请将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.
(4)已知:Ksp(PbCO3)=1.5×10−13,Ksp(PbSO4)=1.8×10−8.在某制备过程中,经检测,过滤出的PbCO3沉淀中混有PbSO4,则该滤液中
 =
=(5)以铅蓄电池为电源,电解二氧化碳酸性溶液可制得丙烯(如图)。

①Y极与电源
②该离子交换膜为
③X极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】 是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
(1)已知:①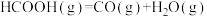
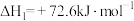
②
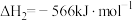
③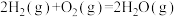
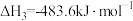
则 的
的
_______  。
。
(2)恒温恒容条件下,向密闭容器中充入1
 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。
(3)一定温度下,保持总压强为2.0 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性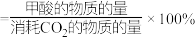 。该温度下,
。该温度下, 的平衡常数
的平衡常数
_______  。
。
(4)常温下,向 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
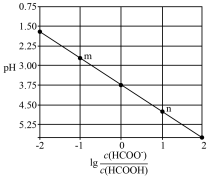
则
_______ ,n点溶液中离子浓度由大到小的排序为_______ 。
(5)常温下,已知 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中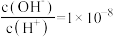 。
。
①
 的
的
_______ 。
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是_______ (填序号)
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的
C.稀释后甲酸的电离度会增大
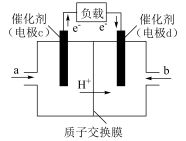
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是_______ (填“正极”或“负极”),c电极的电极反应式为_______ 。
 是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:(1)已知:①
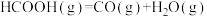
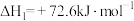
②

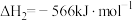
③
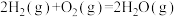
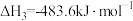
则
 的
的
 。
。(2)恒温恒容条件下,向密闭容器中充入1

 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。| A.气体压强不随时间变化时达到平衡状态 |
B.平衡时 的最大体积分数为50% 的最大体积分数为50% |
C.平衡后及时移走 ,平衡常数增大 ,平衡常数增大 |
D.平衡后再充入 , , 的平衡转化率增大 的平衡转化率增大 |
(3)一定温度下,保持总压强为2.0
 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性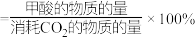 。该温度下,
。该温度下, 的平衡常数
的平衡常数
 。
。(4)常温下,向
 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
则

(5)常温下,已知
 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中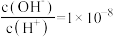 。
。①

 的
的
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的

C.稀释后甲酸的电离度会增大
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是

您最近一年使用:0次
【推荐2】甲醇是一种优质燃料,在工业上常用CO和H2合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g) CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4= 1 。
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g) CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是 2 (填选项字母)。
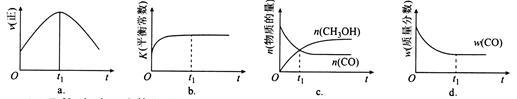
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)= 3 。T1℃时,在另一体积不变的密闭容器中也充入1 mol CO、2 mol H2,达到平衡时CO的转化率为0.7,则该容器的体积 4 5 L(填“>”“<”或“=”);T1℃时,CO(g)+2H2(g) CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K= 5 。
(4)在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当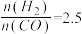 时,达到平衡状态,CH3OH的体积分数可能是图象中的
时,达到平衡状态,CH3OH的体积分数可能是图象中的 6 点。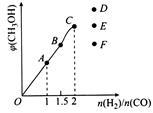
(5)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式: 7 。该电池负极与水库的铁闸相连时,可以保护铁闸不被腐蚀,这种电化学保护方法叫做 8 。
(6)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式: 9 。
 CH3OH(g)。
CH3OH(g)。已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g)
 CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4=(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g)
 CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)=
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=(4)在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当
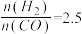 时,达到平衡状态,CH3OH的体积分数可能是图象中的
时,达到平衡状态,CH3OH的体积分数可能是图象中的
(5)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式:
(6)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】合理利用资源,加强环境保护,降低碳排放,实施低碳经济是今后经济生活的主流。回答下列问题:
(1)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4的物质的量之比混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:_____ CO2+4H2 ______+2H2O
______+2H2O
(2)用CO2合成燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下发生反应: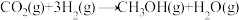 ,在体积为1 L的密闭容器中,充入2 mol CO2和6 molH2。
,在体积为1 L的密闭容器中,充入2 mol CO2和6 molH2。
①能判断该反应已达化学平衡状态的标志是___________ (填字母)。
a.CO2百分含量保持不变
b.容器中混合气体的质量保持不变
c.容器中H2浓度与CO2浓度之比为3∶1
d.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的平均反应速率v(H2)___________ 。

(3)以KOH为电解质的甲醇燃料电池总反应为 。通入甲醇的电极为燃料电池的
。通入甲醇的电极为燃料电池的___________ (填“正”或“负”)极,每消耗1 molCH3OH转移电子___________  。
。
(1)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4的物质的量之比混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:
 ______+2H2O
______+2H2O(2)用CO2合成燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下发生反应:
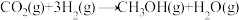 ,在体积为1 L的密闭容器中,充入2 mol CO2和6 molH2。
,在体积为1 L的密闭容器中,充入2 mol CO2和6 molH2。①能判断该反应已达化学平衡状态的标志是
a.CO2百分含量保持不变
b.容器中混合气体的质量保持不变
c.容器中H2浓度与CO2浓度之比为3∶1
d.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的平均反应速率v(H2)

(3)以KOH为电解质的甲醇燃料电池总反应为
 。通入甲醇的电极为燃料电池的
。通入甲醇的电极为燃料电池的 。
。
您最近一年使用:0次



