2020年12月17日,我国嫦娥五号返回器成功携带月壤返回。经专家分析月壤中含有铝、硅、钾、钛、铁、钴等多种元素。回答下列问题:
(1)Al基态原子的价电子排布式是_______ ,钾元素基态原子核外电子的空间运动状态有_______ 种。
(2)在硅酸盐中, 四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构。
四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构。

图甲为一种无限长单链结构的多硅酸根一部分,其中Si原子的杂化方式为_______ ,该多硅酸根的最简式为_______ 。
(3) 比
比 稳定,原因是
稳定,原因是_______ 。 (铁氰化钾)溶液是检验
(铁氰化钾)溶液是检验 常用的试剂,该物质中
常用的试剂,该物质中 键与
键与 键的个数比为
键的个数比为_______ 。与配体 互为等电子体的化学式为
互为等电子体的化学式为_______ (写一种即可)。
(4)钛、钴的一种化合物晶胞结构如下图所示:

①晶胞中离Ti最近的O有_______ 个;由Ti原子和O原子构成的四面体空隙与二者构成的八面体空隙之比为_______ 。
②已知该晶体的密度为 ,则晶胞中Ti与O的最近距离是
,则晶胞中Ti与O的最近距离是_______ nm(用含 、
、 的代数式表示)。
的代数式表示)。
(1)Al基态原子的价电子排布式是
(2)在硅酸盐中,
 四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构。
四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构。
图甲为一种无限长单链结构的多硅酸根一部分,其中Si原子的杂化方式为
(3)
 比
比 稳定,原因是
稳定,原因是 (铁氰化钾)溶液是检验
(铁氰化钾)溶液是检验 常用的试剂,该物质中
常用的试剂,该物质中 键与
键与 键的个数比为
键的个数比为 互为等电子体的化学式为
互为等电子体的化学式为(4)钛、钴的一种化合物晶胞结构如下图所示:

①晶胞中离Ti最近的O有
②已知该晶体的密度为
 ,则晶胞中Ti与O的最近距离是
,则晶胞中Ti与O的最近距离是 、
、 的代数式表示)。
的代数式表示)。
更新时间:2022-04-30 19:03:16
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】碳、氮、硫、硒等元素的单质及其化合物有重要的科学研究价值。回答下 列问题:
(1)氰[化学式(CN)2]、硫氰[化学式(SCN)2]等与卤素单质性质相似,又称类卤素。(CN)2中π键和σ键的数目之比为__________ 。沸点:(CN)2__________ (SCN)2(填“大于”、“等于”或“小于”),理由是__________ 。
(2)无机含氧酸的通式可写成(HO)mROn,如果成酸元素 R 相同,则 n 值越大,R 的正电性越高,在水中越容易电离出 H+。酸性强弱:HNO2____________ HNO3(填“大于”、“等于”或“小于”);NO2-中氮原子的杂化方式为___________ 。
(3)一种硒单质晶体的晶胞为六方晶胞,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶 体结构图和晶体结构俯视图如下所示。

已知正六棱柱的边长为 a cm,高为 b cm,NA 表示阿伏加 德罗常数,则该晶体的密度为__________ g·cm-3(用含 NA、a、b 的式子表示)。
(1)氰[化学式(CN)2]、硫氰[化学式(SCN)2]等与卤素单质性质相似,又称类卤素。(CN)2中π键和σ键的数目之比为
(2)无机含氧酸的通式可写成(HO)mROn,如果成酸元素 R 相同,则 n 值越大,R 的正电性越高,在水中越容易电离出 H+。酸性强弱:HNO2
(3)一种硒单质晶体的晶胞为六方晶胞,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶 体结构图和晶体结构俯视图如下所示。

已知正六棱柱的边长为 a cm,高为 b cm,NA 表示阿伏加 德罗常数,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
(1)铝热反应可以冶炼金属铬,Cr3+基态核外电子排布式为____________________ 。
(2)AlCl3可作反应的催化剂。

①1 mol对甲基苯乙酮分子中含有的σ键数目为__________ 。
②CH3COOH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为_______________ 。
(3)用价层电子对互斥理论解释SO 的键角大于SO
的键角大于SO 的原因是
的原因是_______________ 。
(4)某遮光剂的晶胞如图所示,由晶胞可知n=________ 。

(5)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体 的中心原子的杂化形式为
的中心原子的杂化形式为______ , 空间构型为_____ 。
大π键可用符号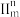 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为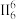 ,则
,则 中大π键应表示为
中大π键应表示为__________ 。
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为______ cm。(阿伏加 德罗常数用NA表示)

(1)铝热反应可以冶炼金属铬,Cr3+基态核外电子排布式为
(2)AlCl3可作反应的催化剂。

①1 mol对甲基苯乙酮分子中含有的σ键数目为
②CH3COOH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为
(3)用价层电子对互斥理论解释SO
 的键角大于SO
的键角大于SO 的原因是
的原因是(4)某遮光剂的晶胞如图所示,由晶胞可知n=

(5)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体
 的中心原子的杂化形式为
的中心原子的杂化形式为大π键可用符号
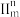 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为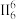 ,则
,则 中大π键应表示为
中大π键应表示为(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】2019年是国际纯粹与应用化学联合会(IUPAC)成立一百周年,也是元素周期表诞生150周年,IUPAC等从世界范围征集优秀青年化学家提名,形成一张“青年化学家元素周期表”,向世界介绍118位优秀青年化学家,有8位中国青年化学家成为“N、Hg、U”等元素的代言人。回答下列问题:
(1)Fe3+基态核外电子排布式为____________________ 。
(2)加碘食盐中含有KIO3,其立体结构如图,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置。K与O间的最短距离为____ nm,与K紧邻的I个数为______ 。
(3)下列有关性质的比较,能用元素周期律解释的是______ 。
a 酸性: b 非金属性:O>S
b 非金属性:O>S
c 碱性: d 热稳定性:
d 热稳定性:
(4)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是________ ,1 mol 乙醇分子中含有σ键的数目为_________ 。
(5)原子坐标参数表示晶胞内各原子的相对位置。如图(晶胞中,原子坐标参数A为(0,0,0);B为( ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为________ 。

(1)Fe3+基态核外电子排布式为
(2)加碘食盐中含有KIO3,其立体结构如图,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置。K与O间的最短距离为

(3)下列有关性质的比较,能用元素周期律解释的是
a 酸性:
 b 非金属性:O>S
b 非金属性:O>S c 碱性:
 d 热稳定性:
d 热稳定性:
(4)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(5)原子坐标参数表示晶胞内各原子的相对位置。如图(晶胞中,原子坐标参数A为(0,0,0);B为(
 ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF- 3IA洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了Fe、Cr、 Ni、 Co.、Cu等多种元素。回答下列问题:
(1)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的_______ 区;
(2)实验室常用KSCN溶液、苯酚(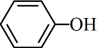 )检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为
)检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为_______ (用元素符号表示),KSCN和苯酚中碳原子的杂化轨道类型为_______ ;
(3)在周期表中Ir位于第六周期并和Co处于同一纵行,则基态Ir原子价电子轨道表示式为_______ 。
(4)羰基铁[Fe(CO) 5]可溶于汽油等有机物,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_______ ;在lmolFe (CO) 5分子中含_______ molσ键,与CO互为等电子体的一种离子的化学式为_______ ;
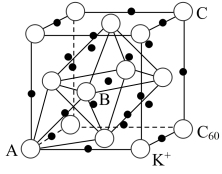
(5)碳的一种同素异形体的晶体,在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的_______ 空隙和_______ 空隙(填几何空间构型) ;若C60分子的坐标参数分别为A (0, 0, 0),B( ,0,
,0, ),C(1,1,1),则距离A位置最近的阳离子的坐标参数为
),C(1,1,1),则距离A位置最近的阳离子的坐标参数为 _______ ;
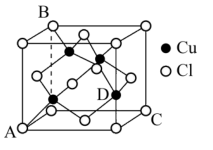
(6)CuCl的晶胞结构如图所示,该结构在实验室可经_______ 方法测得:晶胞中C、D两原子核间距为anm,阿伏加德罗常数的值为NA,CuCl 的相对分子质量为M,则该晶体密度为_______ g·cm-3(列出计算式即可)。
(1)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的
(2)实验室常用KSCN溶液、苯酚(
 )检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为
)检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为(3)在周期表中Ir位于第六周期并和Co处于同一纵行,则基态Ir原子价电子轨道表示式为
(4)羰基铁[Fe(CO) 5]可溶于汽油等有机物,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(5)碳的一种同素异形体的晶体,在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的
 ,0,
,0, ),C(1,1,1),则距离A位置最近的阳离子的坐标参数为
),C(1,1,1),则距离A位置最近的阳离子的坐标参数为 
(6)CuCl的晶胞结构如图所示,该结构在实验室可经

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】Ⅰ.Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。请回答下列问题:
(1)基态Fe3+的电子排布式可表示为__________________ 。
(2)与CN-互为等电子体的分子有___________ (写出2种)。
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=_____ 。
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:
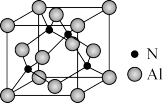
(4)下列说法正确的是__________ (填序号)。
(5)NH3空间构型为______ ;已知(CH3)3Al为非极性分子,则其中铝原子的杂化方式为__________ 。
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为_________ 。
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为____ g/cm。(阿伏加德罗常数用NA表示)
(1)基态Fe3+的电子排布式可表示为
(2)与CN-互为等电子体的分子有
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:

(4)下列说法正确的是
| A.氮化铝晶胞结构与NaCl相同 | B.第一电离能 N>Al |
| C.电负性N>Al | D.原子半径 N>Al |
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铁系元素是人体必需的微量元素,Fe3+可以与KSCN溶液、苯酚等发生显色作用。镁元素也是人体所必需的阳离子元素之一,它能够维持核酸结构的稳定性,调节机体免疫功能,对人体抵抗新冠病毒等病毒侵袭起着重要作用。
(1)与SCN−互为等电子体且为非极性分子的化学式为__________ (任写一种)。
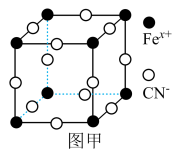

(2)普鲁士蓝俗称铁蓝,晶胞如图甲所示(K+未画出),平均每两个晶胞立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为___________ 。
(3)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)_____________
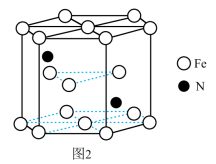
(4)某种磁性氮化铁的结构如图2所示,Fe为____________ 堆积,N随机排列在Fe构成的正四面体空隙中,空隙的占有率为 ,则该化合物的化学式为
,则该化合物的化学式为___________ 。其中铁原子最近的铁原子的个数为________ ;氮化铁晶胞底边长为anm,高为cnm,则这种磁性氮化铁的晶体密度为______ g·cm-3(用含a、c和NA的计算式表示)。
(1)与SCN−互为等电子体且为非极性分子的化学式为


(2)普鲁士蓝俗称铁蓝,晶胞如图甲所示(K+未画出),平均每两个晶胞立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为
(3)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)
(4)某种磁性氮化铁的结构如图2所示,Fe为
 ,则该化合物的化学式为
,则该化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在我国已实现了产业化。该合金的晶胞结构如图所示。

(1)该晶体的化学式为________________ 。
(2)已知该合金的摩尔质量为M g·mol-1,密度为d g·cm-3,设NA为阿伏加德罗常数的值,则该晶胞的体积是______________ cm3(用含M、d、NA的代数式表示)。
(3)该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=511 pm,c=397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=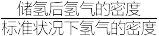 。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为________ 。

(1)该晶体的化学式为
(2)已知该合金的摩尔质量为M g·mol-1,密度为d g·cm-3,设NA为阿伏加德罗常数的值,则该晶胞的体积是
(3)该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=511 pm,c=397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=
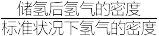 。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】下图是元素周期表的一部分:
 阴影部分元素的外围电子排布式的通式为
阴影部分元素的外围电子排布式的通式为____ 。Sb的元素名称为____ 。基态P原子中,电子占据的最高能级符号为____ ,该能层具有的原子轨道数为____ 。
 氮族元素氢化物
氮族元素氢化物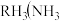 、
、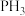 、
、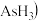 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物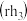 性质可能有
性质可能有____ 。

A.稳定性
B.沸点
C. 键能
键能
D.分子间作用力
 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____ 种。

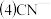 和
和 、
、 及
及 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元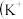 未标出
未标出 ,该图是普鲁士蓝的晶胞吗?
,该图是普鲁士蓝的晶胞吗?____  填“是”或“不是”
填“是”或“不是” ,平均每个结构单元中含有
,平均每个结构单元中含有____ 个 。
。

 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是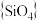 四面体,多磷酸盐中是
四面体,多磷酸盐中是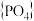 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____ 。

| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
| Pb | Bi | Po | At | ||
 阴影部分元素的外围电子排布式的通式为
阴影部分元素的外围电子排布式的通式为 氮族元素氢化物
氮族元素氢化物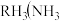 、
、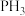 、
、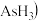 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物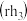 性质可能有
性质可能有
A.稳定性
B.沸点
C.
 键能
键能D.分子间作用力
 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
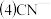 和
和 、
、 及
及 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元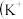 未标出
未标出 ,该图是普鲁士蓝的晶胞吗?
,该图是普鲁士蓝的晶胞吗? 填“是”或“不是”
填“是”或“不是” ,平均每个结构单元中含有
,平均每个结构单元中含有 。
。 
 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是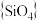 四面体,多磷酸盐中是
四面体,多磷酸盐中是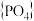 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】“天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙奥秘离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。元素铼( )的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含
)的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含 )中提取铼,其工艺流程如图所示:
)中提取铼,其工艺流程如图所示:
(1)矿样粒度与浸出率关系如下图所示,则“浸出”时应将富铼渣粉碎至___________目(填字母)。
(2)已知“浸出”时反应中 转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:
转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:__________________ 。
(3)实验室中,操作Ⅲ所用装置应选用___________(填字母)。
(4)“一系列操作”包括①________ (填操作名称,下同)、冷却结晶、过滤、洗涤和②____________ ;从下列仪器中选出①②中需使用的仪器,依次为______ (填字母)。___________ 法提纯;“热还原”反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)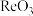 晶胞结构如下图所示,其中氧原子配位数为
晶胞结构如下图所示,其中氧原子配位数为___________ ,铼原子填在了氧原子围成的___________ (填“四面体”“立方体”或“八面体”)空隙中。
 )的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含
)的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含 )中提取铼,其工艺流程如图所示:
)中提取铼,其工艺流程如图所示: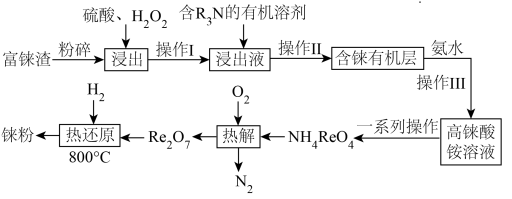
(1)矿样粒度与浸出率关系如下图所示,则“浸出”时应将富铼渣粉碎至___________目(填字母)。
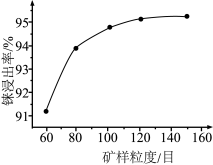
| A.60 | B.80 | C.100 | D.120 |
(2)已知“浸出”时反应中
 转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:
转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:(3)实验室中,操作Ⅲ所用装置应选用___________(填字母)。
A. | B.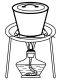 | C.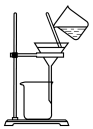 | D.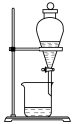 |
(4)“一系列操作”包括①
A.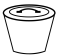 B.
B. C.
C. D.
D.
(6)
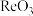 晶胞结构如下图所示,其中氧原子配位数为
晶胞结构如下图所示,其中氧原子配位数为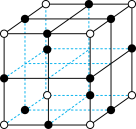
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O
(1)X基态原子的电子排布式为______ .
(2)C、H、O三种原子的电负性由大到小的顺序为______ .
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:
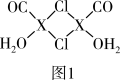
①与CO为互为等电子体的分子是______ .
②该配合物中氯原子的杂化方式为______ .
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键______ .
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为______ .XCl的化学式__________

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=_____________ (无需化简,列式即可)。
(1)X基态原子的电子排布式为
(2)C、H、O三种原子的电负性由大到小的顺序为
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:

①与CO为互为等电子体的分子是
②该配合物中氯原子的杂化方式为
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硼、硅、硒等元素及其化合物用途广泛。请回答下列问题:
(1)基态硒原子的价电子排布式为_______ ;SeO2常温下为白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体为________ 晶体。
(2)在硼、硅、硒的气态氢化物中,其立体构型为正四面体的是_______ (填化学式),在硅的氢化物中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性大小为Se_____ Si(填“>”或“<”)。
(3)在周期表的第二周期中,第一电离能介于硼元素和氮元素之间的元素有_____ 种。
(4)硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,BF3·NH3中B与N之间形成______ 键;NH3中N原子的杂化轨道类型为______ ,写出与NH3等电子体的一种离子符号________ 。
(5)金刚砂(SiC)的摩氏硬度为9.5,其晶胞结构如图所示。在SiC中,每个Si原子周围距离最近的Si原子数目为________ ;若金刚砂的密度为ρg·cm-3,NA表示阿伏加 德罗常数的值,则晶胞中碳原子与硅原子的最近距离为________ pm。(用含ρ和NA的式子表示)
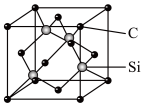
(1)基态硒原子的价电子排布式为
(2)在硼、硅、硒的气态氢化物中,其立体构型为正四面体的是
(3)在周期表的第二周期中,第一电离能介于硼元素和氮元素之间的元素有
(4)硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,BF3·NH3中B与N之间形成
(5)金刚砂(SiC)的摩氏硬度为9.5,其晶胞结构如图所示。在SiC中,每个Si原子周围距离最近的Si原子数目为

您最近一年使用:0次
【推荐3】Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________ 族。基态Co原子的简化电子排布式为_________ 。
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________ 杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______ ,配合物晶体中可能存在的作用力有___________ 。
A离子键B极性共价键C非极性共价键D配位键E氢键

(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NixO晶体中x值为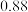 ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______ 。

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____ g(用a、NA表示)。

(1)Co元素在周期表中的位置是4周期
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为
A离子键B极性共价键C非极性共价键D配位键E氢键

(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NixO晶体中x值为
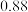 ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为

您最近一年使用:0次



