元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O
(1)X基态原子的电子排布式为______ .
(2)C、H、O三种原子的电负性由大到小的顺序为______ .
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:
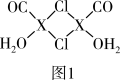
①与CO为互为等电子体的分子是______ .
②该配合物中氯原子的杂化方式为______ .
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键______ .
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为______ .XCl的化学式__________

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=_____________ (无需化简,列式即可)。
(1)X基态原子的电子排布式为
(2)C、H、O三种原子的电负性由大到小的顺序为
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:

①与CO为互为等电子体的分子是
②该配合物中氯原子的杂化方式为
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=
更新时间:2020-06-15 17:14:25
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知X、Y、Z、W、Q是前四周期的核电荷数依次增大的元素,X的价电子层中有3个未成对电子,X与Z同主族;Y与W同主族,W元素原子M层有两对成对电子;Q的最外层只有1个电子,但次外层有18个电子。
(1)X、Y、W的第一电离能由大到小的顺序是__ (填字母对应的元素符号)。
(2)已知元素Z的某钾盐(KH2ZO4)是其酸(H3ZO2)的正盐,则酸H3ZO2的结构式为__ (元素Z用对应的元素符号书写)。
(3)已知元素X、Z相关键的键能(kJ•mol-1)如表:从能量角度看,X元素形成的单质以X2、而Z元素形成的单质Z4(结构式可表示为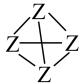 )形式存在的原因是
)形式存在的原因是__ 。
(4)元素W的含氧酸根离子(WO )的空间构型为
)的空间构型为__ ,与之互为等电子体的阴离子有__ (写出一种离子符号;等电子体指化学通式相同且价电子总数相等的分子或离子)。
(5)对于基态Q原子,下列叙述正确的是__ (填标号)。
(6)向盛有QSO4水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。分离出所得溶质化合物[Q(NH3)4(H2O)2]SO4,然后加热该化合物固体,首先失去的组分是__ ,理由是__ 。
(1)X、Y、W的第一电离能由大到小的顺序是
(2)已知元素Z的某钾盐(KH2ZO4)是其酸(H3ZO2)的正盐,则酸H3ZO2的结构式为
(3)已知元素X、Z相关键的键能(kJ•mol-1)如表:从能量角度看,X元素形成的单质以X2、而Z元素形成的单质Z4(结构式可表示为
 )形式存在的原因是
)形式存在的原因是| X—X | X≡X | Z—Z | Z≡Z |
| 193 | 946 | 197 | 489 |
 )的空间构型为
)的空间构型为(5)对于基态Q原子,下列叙述正确的是
| A.遵循能量最低原理,核外电子排布应为[Ar]3d94s2 |
| B.排布在外层的电子总是比排布在内层的电子离核更远 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
| D.电子先排入4s轨道,再排进3d轨道,故3d轨道的电子能量比4s高 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图

(1)基态Zn2+的价电子排布式为___________ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是___________ 。
(2)甘氨酸(H2N-CH2-COOH)中N的杂化轨道类型为___________ ;甘氨酸易溶于水,试从结构角度解释___________ 。
(3)一水合甘氨酸锌中Zn2+的配位数为___________ 。
(4)[Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为 ,则1molIMI中含有
,则1molIMI中含有___________ 个σ键。
(5)常温下IMI的某种衍生物与甘氨酸形成的离子化合物 为液态而非固态,原因是
为液态而非固态,原因是___________ 。
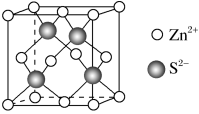
(6)Zn与S形成某种化合物的晶胞如图I所示。

①Zn2+填入S2-组成的___________ 空隙中;
②由①能否判断出S2-、Zn2+相切?___________ (填“能”或“否”);已知晶体密度为dg/cm3,S2-半径为apm,若要使S2-、Zn2+相切,则Zn2+半径为___________ pm(写计算表达式)。

(1)基态Zn2+的价电子排布式为
(2)甘氨酸(H2N-CH2-COOH)中N的杂化轨道类型为
(3)一水合甘氨酸锌中Zn2+的配位数为
(4)[Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为
 ,则1molIMI中含有
,则1molIMI中含有(5)常温下IMI的某种衍生物与甘氨酸形成的离子化合物
 为液态而非固态,原因是
为液态而非固态,原因是(6)Zn与S形成某种化合物的晶胞如图I所示。

①Zn2+填入S2-组成的
②由①能否判断出S2-、Zn2+相切?
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
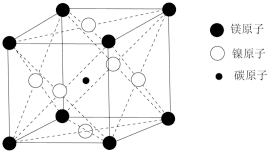
【推荐3】最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。
(1)该新型超导晶体的一个晶胞如图所示,则该晶体的化学式是__________ 。镍在元素周期表中的位置是______ ,Ni2+的价电子有_________ 种不同运动状态。
(2)500-600℃时,BeCl2以双聚分子存在的BeCl2的结构式为________________________ 。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于______ 晶体,配体是______ 该配合物中存在的作用力类型有___________ (填标号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
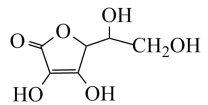
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_______ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(5)副族元素Zn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中为( 为Se,
为Se, 为Zn),Zn的配位数为
为Zn),Zn的配位数为______ ,该晶体的密度为 g/cm3,则Zn—Se键的键长为
g/cm3,则Zn—Se键的键长为______ nm。
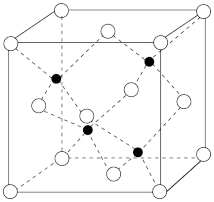
(1)该新型超导晶体的一个晶胞如图所示,则该晶体的化学式是

(2)500-600℃时,BeCl2以双聚分子存在的BeCl2的结构式为
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

(5)副族元素Zn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中为(
 为Se,
为Se, 为Zn),Zn的配位数为
为Zn),Zn的配位数为 g/cm3,则Zn—Se键的键长为
g/cm3,则Zn—Se键的键长为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】物质结构决定物质性质。回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________ (填元素符号),其中C原子的核外电子排布式为__________ 。
(2)单质A有两种同素异形体,其中沸点高的是__________ (填分子式);B的氢化物所属的晶体类型为_________ 。

(3)化合物D2A的立体构型为________ 中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ :列式计算晶体F的密度(g.cm-3)___________ 。
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是

(3)化合物D2A的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】我国科学家研究发现,在KOH催化下,CO(NH2)2和LiTPSI还原形成稳定的LiF/高分子双层SEI,使LiMn2O4//Li4T15O12电池稳定工作。请回答下列问题:
(1)基态Mn2+的电子排布式为[Ar]____ 。基态K原子核外电子云轮廓图呈球形的能级上占据的电子总数为____ 。
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是____ 。
(3)CO(NH2)2中元素电负性由大到小的顺序为____ (用元素符号表示)。CO(NH2)2分子中碳原子的杂化方式为____ 。
(4)几种钛的卤化物的熔点如表所示:
钛的卤化物熔点呈上述变化的主要原因是____ 。
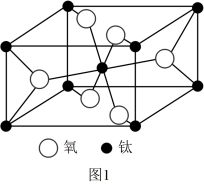
(5)一种钛的氧化物晶胞如图1所示,其化学式为____ 。
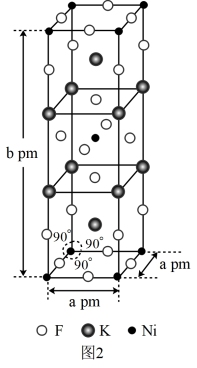
(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为____ g·cm-3(只列计算式即可)。
(1)基态Mn2+的电子排布式为[Ar]
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是
(3)CO(NH2)2中元素电负性由大到小的顺序为
(4)几种钛的卤化物的熔点如表所示:
| 卤化物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -25 | 39 | 150 |
(5)一种钛的氧化物晶胞如图1所示,其化学式为

(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为__ ;第一电离能I1(Si)__ I1(Ge)(填>或<)。
(2)基态Ge原子核外电子排布式为__ ;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是__ 。
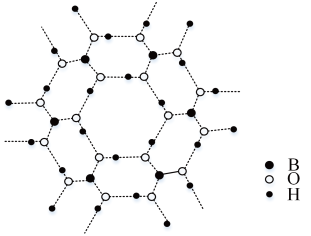
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为__ ;硼酸在热水中比在冷水中溶解度显著增大的主要原因是__ 。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为__ ;CsSiB3O7的摩尔质量为Mg.mol-1,设NA为阿伏加 德罗常数的值,则CsSiB3O7晶体的密度为__ g·cm-3(用代数式表示)。
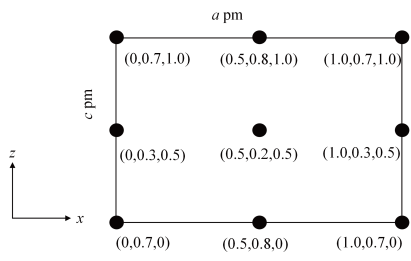
(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子核外电子排布式为
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】我国科学家发明了高选择性的二氧化碳加氢合成甲醇( )的催化剂,其组成为
)的催化剂,其组成为 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
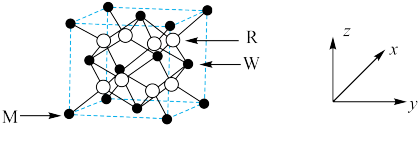
(1)图示晶胞中R代表___________ (填“O”或“ ”)原子,判断的理由为
”)原子,判断的理由为___________ 。
(2)关于 分子:
分子:
①该分子中氧原子采取的杂化类型为___________ 。
②该分子中的碳原子的价层电子对数为___________ 。
③有机物大多难溶于水,而甲醇可以与水互溶,其原因为___________ 。
(3)原子坐标参数表示晶胞内部各原子的相对位置,在如上图所示的晶胞中:
①若M原子的坐标参数为 ,W原子的坐标参数为
,W原子的坐标参数为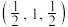 ,则R原子的坐标参数为
,则R原子的坐标参数为___________ 。
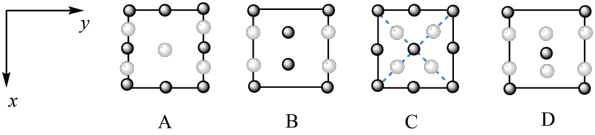
② 晶胞在z轴方向的投影图为
晶胞在z轴方向的投影图为___________ (填标号)。
(4)查阅资料可知: 的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
① 属于
属于___________ (填“分子”、“原子”或“离子”)晶体。
②假设 的密度为
的密度为
 ,摩尔质量为M
,摩尔质量为M ,
, 表示阿伏加德罗常数的值,则晶胞中
表示阿伏加德罗常数的值,则晶胞中 原子和O原子的最短距离为
原子和O原子的最短距离为___________  (列式表示即可)。
(列式表示即可)。
 )的催化剂,其组成为
)的催化剂,其组成为 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
(1)图示晶胞中R代表
 ”)原子,判断的理由为
”)原子,判断的理由为(2)关于
 分子:
分子:①该分子中氧原子采取的杂化类型为
②该分子中的碳原子的价层电子对数为
③有机物大多难溶于水,而甲醇可以与水互溶,其原因为
(3)原子坐标参数表示晶胞内部各原子的相对位置,在如上图所示的晶胞中:
①若M原子的坐标参数为
 ,W原子的坐标参数为
,W原子的坐标参数为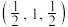 ,则R原子的坐标参数为
,则R原子的坐标参数为②
 晶胞在z轴方向的投影图为
晶胞在z轴方向的投影图为
(4)查阅资料可知:
 的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
的熔点为2700℃,沸点为4300℃且熔融状态下可导电。①
 属于
属于②假设
 的密度为
的密度为
 ,摩尔质量为M
,摩尔质量为M ,
, 表示阿伏加德罗常数的值,则晶胞中
表示阿伏加德罗常数的值,则晶胞中 原子和O原子的最短距离为
原子和O原子的最短距离为 (列式表示即可)。
(列式表示即可)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
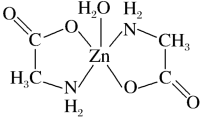
【推荐2】一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图。 的价电子排布式为
的价电子排布式为_______ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是_______ 。
(2)甘氨酸(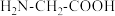 )中N的杂化轨道类型为
)中N的杂化轨道类型为_______ ;甘氨酸易溶于水,试从结构角度解释_______ 。
(3)一水合甘氨酸锌中 的配位数为
的配位数为_______ 。 填入
填入 组成
组成_______ 空隙中;
②由①能否判断出 、
、 相切?
相切?_______ (填“能”或“否”);
③已知晶体密度为 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为_______ pm(写计算表达式)。
 的价电子排布式为
的价电子排布式为(2)甘氨酸(
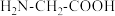 )中N的杂化轨道类型为
)中N的杂化轨道类型为(3)一水合甘氨酸锌中
 的配位数为
的配位数为(4) 是
是 的另一种配合物,IMI的结构为
的另一种配合物,IMI的结构为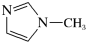 ,常温下IMI的某种衍生物与甘氨酸形成的离子化合物
,常温下IMI的某种衍生物与甘氨酸形成的离子化合物 为液态而非固态。原因是
为液态而非固态。原因是
 填入
填入 组成
组成②由①能否判断出
 、
、 相切?
相切?③已知晶体密度为
 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】如图,铜离子与有机物HA可形成一种螯合物CuA2,从而萃取水中的铜离子。

回答下列问题:
(1)基态铜原子价电子排布式为_______ 。
(2)有机物HA中,C、N、O三种元素的电负性由大到小的顺序是_______ 。
(3)螯合物CuA2中的氮原子、氧原子的杂化方式分别为_______ 。
(4)下列关于螯合物CuA2的说法中,正确的是_______ (填序号)。
①CuA2中O的配位能力比N强 ②与Cu2+配位的4个原子可能呈平面构型
③CuA2既溶于水又溶于有机溶剂 ④每个CuA2中含2个氢键、2个π键
(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是_______ 。
(6)金属铜与铝可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示,晶胞参数α=β=γ=90°,a=b=0.41 nm,c=0.58 nm,按图甲中阴影面进行投影得到图乙。

①已知晶胞中A点的原子坐标为 ,则B点的原子坐标为
,则B点的原子坐标为_______ 。
②该晶体的化学式为_______ ,密度为_______  (结果保留两位有效数字)。
(结果保留两位有效数字)。

回答下列问题:
(1)基态铜原子价电子排布式为
(2)有机物HA中,C、N、O三种元素的电负性由大到小的顺序是
(3)螯合物CuA2中的氮原子、氧原子的杂化方式分别为
(4)下列关于螯合物CuA2的说法中,正确的是
①CuA2中O的配位能力比N强 ②与Cu2+配位的4个原子可能呈平面构型
③CuA2既溶于水又溶于有机溶剂 ④每个CuA2中含2个氢键、2个π键
(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是
(6)金属铜与铝可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示,晶胞参数α=β=γ=90°,a=b=0.41 nm,c=0.58 nm,按图甲中阴影面进行投影得到图乙。

①已知晶胞中A点的原子坐标为
 ,则B点的原子坐标为
,则B点的原子坐标为②该晶体的化学式为
 (结果保留两位有效数字)。
(结果保留两位有效数字)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】超导材料和超导技术是2世纪最伟大的发现之一,有着广阔的应用前景。我国科学家发现了一种新型的超导体材料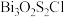 ,由
,由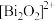 和
和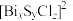 交替堆叠构成。其中A层是由
交替堆叠构成。其中A层是由 无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。
无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。

(1)画出基态S的价电子排布图_______ 。
(2)写出A层离子的化学式_______ 。A层各元素的第一电离能由大到小的顺序为_______ 。
(3)“依布硒”( )具有良好的抗炎活性。下列说法正确的是
)具有良好的抗炎活性。下列说法正确的是_______ 。
a.Se采用sp3的方式杂化
b.分子中各个C原子的杂化方式不同
c.分子中既含有极性共价键,又含有非极性共价键
d.分子中 和
和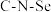 的键角相同
的键角相同
(4)H2O和H2S都是分子晶体,熔沸点较高的是_______ ,原因是_______ 。
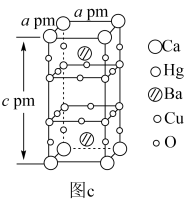
(5)83Bi是第_______ 周期VA族元素, 是一种极少数不溶性的钠盐,其阴离子的立体构型为
是一种极少数不溶性的钠盐,其阴离子的立体构型为_______ 。
(6)汞钡铜氧晶体通过掺杂Ca2+可以获得具有更高临界温度的超导材料,如图c所示。其密度为_______  (列式表示、设NA为阿伏加德罗常数的值)。
(列式表示、设NA为阿伏加德罗常数的值)。
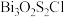 ,由
,由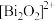 和
和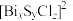 交替堆叠构成。其中A层是由
交替堆叠构成。其中A层是由 无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。
无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。
(1)画出基态S的价电子排布图
(2)写出A层离子的化学式
(3)“依布硒”(
 )具有良好的抗炎活性。下列说法正确的是
)具有良好的抗炎活性。下列说法正确的是a.Se采用sp3的方式杂化
b.分子中各个C原子的杂化方式不同
c.分子中既含有极性共价键,又含有非极性共价键
d.分子中
 和
和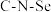 的键角相同
的键角相同(4)H2O和H2S都是分子晶体,熔沸点较高的是
(5)83Bi是第
 是一种极少数不溶性的钠盐,其阴离子的立体构型为
是一种极少数不溶性的钠盐,其阴离子的立体构型为(6)汞钡铜氧晶体通过掺杂Ca2+可以获得具有更高临界温度的超导材料,如图c所示。其密度为
 (列式表示、设NA为阿伏加德罗常数的值)。
(列式表示、设NA为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】【化学——选修3:物质的结构与性质】
钛有“生物金属”和“未来金属”之称,钛及其化合物的应用正越来越受到人们的关注。
(1)基态钛原子外围电子的轨道表达式为___________ 。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___ 种。
(2)金属钛的熔点、硬度均比铝大,可能的原因是____ 。
(3)TiCl4是氯化法制取钛的中间产物。TiCl4和SiCl4在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是__________ (填化学式)。
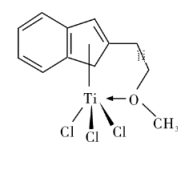
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图所示。
①组成该物质的元素中,电负性最大的是__________ (填元素名称)。
②M中碳原子的杂化形式有___________ 种。
③M中不含__________ (填字母代号)。
a.π键 b.σ键 c.配位键
d.氢键 e.离子键

(5)①金属钛晶体中原子采用面心立方最密堆积,则晶胞中钛原子的配位数为_____ 。
②设钛原子的直径为d cm,用NA表示阿伏伽德罗常数的值,钛原子的摩尔质量为M g·mol-1,则晶体钛的密度为________ g·cm-3。
③金属钛晶胞中有若干个正四面体空隙,如图中a、b、c、d四个钛原子形成一个正四面体,其内部为正四面体空隙,可以填充其他原子。若晶胞中所有的正四面体空隙中都填充氢原子,那么形成的氢化钛的化学式为__________ 。
钛有“生物金属”和“未来金属”之称,钛及其化合物的应用正越来越受到人们的关注。
(1)基态钛原子外围电子的轨道表达式为
(2)金属钛的熔点、硬度均比铝大,可能的原因是
(3)TiCl4是氯化法制取钛的中间产物。TiCl4和SiCl4在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是

(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图所示。
①组成该物质的元素中,电负性最大的是
②M中碳原子的杂化形式有
③M中不含
a.π键 b.σ键 c.配位键
d.氢键 e.离子键

(5)①金属钛晶体中原子采用面心立方最密堆积,则晶胞中钛原子的配位数为
②设钛原子的直径为d cm,用NA表示阿伏伽德罗常数的值,钛原子的摩尔质量为M g·mol-1,则晶体钛的密度为
③金属钛晶胞中有若干个正四面体空隙,如图中a、b、c、d四个钛原子形成一个正四面体,其内部为正四面体空隙,可以填充其他原子。若晶胞中所有的正四面体空隙中都填充氢原子,那么形成的氢化钛的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期且相邻的元素,B基态原子2p轨道中有三个自旋方向完全相同的电子;C基态原子核外电子占有9个轨道,且只有1个未成对电子;D、E、F是位于同一周期的金属元素, D、E基态原子的价电子层中未成对电子数分别为4、2,且原子序数相差2;F是ds区元素,F基态原子的价电子层中只有1个未成对电子。
回答下列问题:
(1)E元素在周期表中的位置是____________ ,E的价层电子排布图为________________ 。E单质能导电的原因是_______________ 。
(2)A、B、D三种元素形成配合物D3[D(AB)6]2,该配合物的中心离子是___ ,1 个AB-离子中含有_____ 个 π键。
(3)A元素最高价氧化物分子中A原子的杂化轨道类型是______ ,BC3分子的立体构型是_____________ 。
(4)新制的F(OH)2能够溶解于浓NaOH溶液中形成一种配离子,反应的离子方程式是__ 。
(5)E、F元素的第二电离能分别是:IE=1753kJ/mol、IF=1958kJ/mol, IF>IE的原因是___ 。
(6)C、F元素形成的一种化合物晶胞如下图,F位于面心和顶点,其晶胞参数为a pm。
①已知M点的坐标为 ,则N点的坐标为
,则N点的坐标为______ ,P点的坐标为_______ 。
若阿伏伽德罗常数用NA表示,则该晶体的密度是_____________ g/cm3(只要求列算式)。

回答下列问题:
(1)E元素在周期表中的位置是
(2)A、B、D三种元素形成配合物D3[D(AB)6]2,该配合物的中心离子是
(3)A元素最高价氧化物分子中A原子的杂化轨道类型是
(4)新制的F(OH)2能够溶解于浓NaOH溶液中形成一种配离子,反应的离子方程式是
(5)E、F元素的第二电离能分别是:IE=1753kJ/mol、IF=1958kJ/mol, IF>IE的原因是
(6)C、F元素形成的一种化合物晶胞如下图,F位于面心和顶点,其晶胞参数为a pm。
①已知M点的坐标为
 ,则N点的坐标为
,则N点的坐标为若阿伏伽德罗常数用NA表示,则该晶体的密度是

您最近一年使用:0次



