 和
和 存在平衡:
存在平衡: 。下列分析正确的是
。下列分析正确的是A. 平衡混合气体中含N原子大于 平衡混合气体中含N原子大于 |
| B.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
C.恒容时,充入少量 ,平衡正向移动导致气体颜色变浅 ,平衡正向移动导致气体颜色变浅 |
D.断裂 中的共价键所需能量大于断裂 中的共价键所需能量大于断裂 中的共价键所需能量 中的共价键所需能量 |
更新时间:2022-05-05 21:42:13
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法错误的是
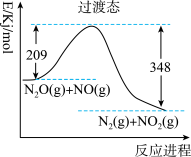

| A.使用催化剂可以降低过渡态的能量 |
| B.反应物能量之和大于生成物能量之和 |
| C.N2O(g)+NO(g)→N2(g)+NO2(g)+139kJ |
| D.反应物的键能总和大于生成物的键能总和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1所示,相对能量变化关系如图2所示,吸附在催化剂表面的物质用“*”标注。下列说法错误的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1所示,相对能量变化关系如图2所示,吸附在催化剂表面的物质用“*”标注。下列说法错误的是
 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1所示,相对能量变化关系如图2所示,吸附在催化剂表面的物质用“*”标注。下列说法错误的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1所示,相对能量变化关系如图2所示,吸附在催化剂表面的物质用“*”标注。下列说法错误的是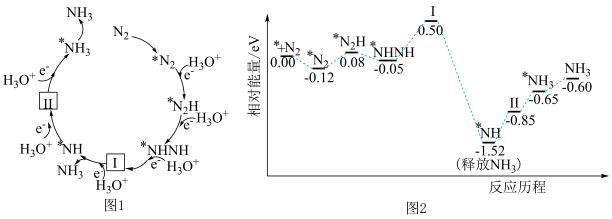
| A.反应过程中存在极性键的断裂与形成及非极性键的断裂 |
B.由图1反应历程可以看出,生成1mol 需要消耗6mol 需要消耗6mol |
C.Ⅱ表示的微粒符号是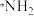 |
D.反应历程中化学反应速率最慢的反应是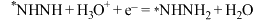 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
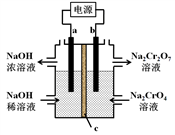
【推荐1】根据反应2CrO42-+2H+ Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
 Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
| A.a连接电源负极 |
| B.b极反应式:2H2O-4e-=O2↑+4H+ |
| C.c为阳离子交换膜 |
| D.通过2 mol电子时生成1 mol Cr2O72- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,向VL恒容密闭容器中通入4molX(g),发生反应:① ,②
,② 。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下列说法错误的是
。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下列说法错误的是
 ,②
,② 。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下列说法错误的是
。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下列说法错误的是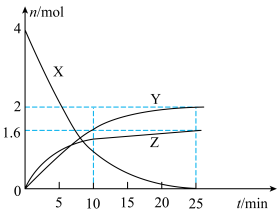
| A.25min时,生成了3.2molM |
B.0~10min内,气体X的平均反应速率为 |
C.该温度下,反应②的平衡常数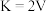 |
| D.25min时保持其他条件不变,再向体系中通入1molY(g)后,反应②的平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是温度和压强对X+Y 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
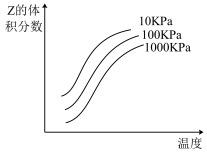
 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
| A.上述可逆反应的正反应为放热反应 |
| B.X和Y中最多只有一种为气态,Z为气态 |
| C.X、Y、Z均为气体 |
| D.上述反应的逆反应ΔH>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0,下列对图像的分析中正确的是


| A.图I研究的是t0时增大压强对反应速率的影响 |
| B.图II研究的一定是t0时使用了催化剂对反应速率的影响 |
| C.图III研究的是温度对化学平衡的影响,且甲的温度较高 |
| D.图IV研究的可能是压强对化学平衡的影响,且a的压强较高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】若反应:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法
N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法不正确 的是
 N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法
N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法| A.分离出CO2,使Q减小,Q<K,因此平衡正向移动 |
| B.分离出N2,使Q减小,Q<K,因此平衡正向移动 |
| C.降低温度,使Q减小,Q<K,因此平衡正向移动 |
| D.加入催化剂可以同等程度增大正、逆反应速率,平衡不移动 |
您最近一年使用:0次




