已知25℃时有关弱酸的电离平衡常数如表所示。
下列说法错误的是
| 弱酸 | HClO | HF |  |  |
| 电离常数 |  | 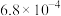 |  |  |
A.向 溶液中加入少量 溶液中加入少量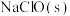 ,溶液的pH会增大 ,溶液的pH会增大 |
B.反应 可以发生 可以发生 |
C.相同物质的量浓度的四种溶液中由水电离出的 : : 溶液 溶液 溶液> 溶液> 溶液 溶液 溶液 溶液 |
D.酸性: |
更新时间:2022-05-20 18:00:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,将NH3 通入50 mL NH4Cl 溶液中至pH=10,再向其中滴加1 mol/L盐酸。溶液的pH随加入盐酸体积的变化如图所示,下列说法不正确的是


| A.a 点溶液中,c(OH-) = 1×10-4mol/L | B.b 点溶液中,c( ) > c(Cl-) ) > c(Cl-) |
| C.a→b,水的电离程度减小 | D.c 点时,加入的 n(HCl)小于通入的 n(NH3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离的 的溶液:Na+、Cu2+、 的溶液:Na+、Cu2+、 、 、 |
B.0.2mol/L的NH4Cl溶液:Na+、K+、 、 、 |
C.使甲基橙变红色的溶液:Fe3+、K+、 、 、 |
D.0.1mol/L NaClO溶液:H+、Na+、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐1】草酸( )是二元弱酸。某小组做如下两组实验:
)是二元弱酸。某小组做如下两组实验:
实验I:往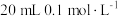
 溶液中滴加
溶液中滴加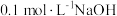 溶液。
溶液。
实验Ⅱ:往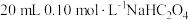 溶液中滴加
溶液中滴加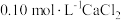 溶液。
溶液。
[已知: 的电离常数
的电离常数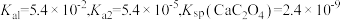 ,溶液混合后体积变化忽略不计],下列说法正确的是
,溶液混合后体积变化忽略不计],下列说法正确的是
 )是二元弱酸。某小组做如下两组实验:
)是二元弱酸。某小组做如下两组实验:实验I:往
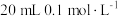
 溶液中滴加
溶液中滴加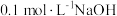 溶液。
溶液。实验Ⅱ:往
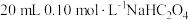 溶液中滴加
溶液中滴加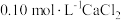 溶液。
溶液。[已知:
 的电离常数
的电离常数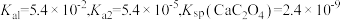 ,溶液混合后体积变化忽略不计],下列说法正确的是
,溶液混合后体积变化忽略不计],下列说法正确的是| A.实验I可选用甲基橙作指示剂,指示反应终点 |
B.实验I中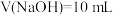 时,存在 时,存在 |
C.实验Ⅱ中发生反应 |
D.实验Ⅱ中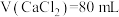 时,溶液中 时,溶液中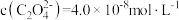 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,在体积均为10.0mL、浓度均为0.10mol·L-1的HX、HY溶液中分别滴加某浓度的NaOH溶液,pOH水[pOH水=-lgc( ),c(
),c( )表示溶液中水电离出的OH-的浓度]与滴加NaOH溶液的体积的关系如图所示,下列说法正确的是
)表示溶液中水电离出的OH-的浓度]与滴加NaOH溶液的体积的关系如图所示,下列说法正确的是

 ),c(
),c( )表示溶液中水电离出的OH-的浓度]与滴加NaOH溶液的体积的关系如图所示,下列说法正确的是
)表示溶液中水电离出的OH-的浓度]与滴加NaOH溶液的体积的关系如图所示,下列说法正确的是
| A.HX、HY均为弱酸,HY的酸性更强 |
| B.NaOH溶液浓度c(NaOH)=0.1mol·L-1 |
| C.M、N两点的溶液中:c(X-)与c(Y-)不相等 |
| D.常温下HY的电离常数Ka≈5.4×10-6 |
您最近一年使用:0次



 与
与 可结合生成多种络合物,在水溶液中存在如下平衡:
可结合生成多种络合物,在水溶液中存在如下平衡: ,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中
,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中 关系如图。下列说法正确的是
关系如图。下列说法正确的是
 分布系数的变化情况
分布系数的变化情况 时,
时,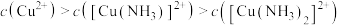
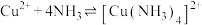 的平衡常数K=1012.6
的平衡常数K=1012.6


