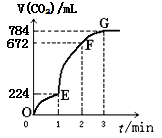
某同学将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是
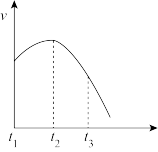

| A.从t1→t2的原因是溶液中H+的浓度较大 |
| B.从t1→t2的原因水蒸发,致使H+的浓度升高 |
| C.从t2→t3的原因是随着反应的进行镁条的质量下降 |
| D.从t2→t3的原因是随着反应的进行,H+的浓度逐渐下降 |
更新时间:2022-05-15 09:53:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作、现象和解释或结论完全正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 分别向浓度为2 mol·L-1的盐酸和1 mol·L-1的硫酸中加入形状、质量相同的锌粒 | 盐酸中的锌粒表面产生气体的速率明显快 | 盐酸中的H+浓度大 |
| B | 除去氯化钠固体中的少量硝酸钾时,将固体溶于水,加热浓缩,降温结晶 | 析出大量固体 | 利用了硝酸钾的溶解度随温度变化大,而氯化钠变化小的特点 |
| C | 将甲烷,乙烯和氯化氢混合气体通入酸性高锰酸钾溶液中 | 紫色褪去 | 从高锰酸钾洗气瓶出来的气体含有甲烷、二氧化碳和少量未反应的氯化氢 |
| D | 量取10.00mL待测氢氧化钠溶液于锥形瓶中,加入2滴甲基橙,用0.10 mol·L-1盐酸滴定 | 滴加盐酸至10.00 mL时,锥形瓶内溶液颜色由黄色变为橙色,且半分钟内不变色 | 氢氧化钠溶液的浓度为0.10mol·L-1 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】关于图中各装置的叙述不正确的是


A.装置①模拟铁制品镀铜可用 溶液作电镀液 溶液作电镀液 |
| B.装置②能探究浓度对锌与稀硫酸化学反应速率的影响 |
| C.装置③可通过球内气体颜色的深浅判断温度对平衡的影响 |
| D.装置④在充电时,应将电源的负极连接在Pb电极上 |
您最近半年使用:0次
【推荐3】下列实验操作能达到实验目的的是
| 选项 | 目的 | 操作 |
| A | 制备无水AlCl3 | 蒸发Al与稀盐酸反应后的溶液 |
| B | 比较Ca和Mg的金属性强弱 | 用pH计测同温同浓度的MgCl2溶液的和CaCl2溶液的pH |
| C | 提纯混有NH4Cl的粗碘 | 将粗碘放入烧杯中,烧杯口放一盛满冷水的烧瓶,隔石棉网对烧杯加热然后收集烧瓶外壁的固体 |
| D | 探究浓度对反应速率的影响 | 分别向盛有2 mL 0.1 mol/L和2 mL0.2 mol/LKMnO4溶液两支试管中加入5 mL0.1 mol/LH2C2O4,第一支试管中溶液先褪色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业合成三氧化硫的反应为2SO2(g)+O2(g) 2SO3(g) △H=-198kJ/mol,反应过程可用如图模拟(
2SO3(g) △H=-198kJ/mol,反应过程可用如图模拟( 表示O2,
表示O2, 表示SO2,
表示SO2, 表示催化剂)。下列说法不正确的是
表示催化剂)。下列说法不正确的是

 2SO3(g) △H=-198kJ/mol,反应过程可用如图模拟(
2SO3(g) △H=-198kJ/mol,反应过程可用如图模拟( 表示O2,
表示O2, 表示SO2,
表示SO2, 表示催化剂)。下列说法不正确的是
表示催化剂)。下列说法不正确的是
| A.过程Ⅱ和过程Ⅲ决定了全部反应进行的程度 |
| B.催化剂可降低反应的活化能,从而使单位体积中活化分子百分数增大,化学反应速率加快 |
| C.过程Ⅱ为吸热过程,过程Ⅲ为放热过程;所以升高温度,过程Ⅱ速率加快,过程Ⅲ速率减慢 |
| D.1molSO2和0.5molO2反应,放出的热量小于99kJ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据下列实验操作和现象所得到的结论正确的是
A.碳酸钙与过量盐酸反应,某时间段内生成 的速率先快后慢,速率加快的主要因素是温度升高 的速率先快后慢,速率加快的主要因素是温度升高 |
B.取 溶液,向其中滴加 溶液,向其中滴加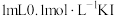 溶液,取上层清液滴加KSCN溶液,溶液变成血红色,该反应是可逆反应 溶液,取上层清液滴加KSCN溶液,溶液变成血红色,该反应是可逆反应 |
| C.将红热的铂丝插入到盛有氨气和氧气的集气瓶,铂丝一直保持红热,集气瓶出现红棕色气体,氨气与氧气反应放热,无一氧化氮生成 |
D.分别向蛋白质溶液中加入饱和 和 和 溶液,均析出固体,蛋白质都发生变性 溶液,均析出固体,蛋白质都发生变性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验能达到预期目的是
| 选项 | 实验内容 | 实验目的 |
| A | 将 的 的 溶液和 溶液和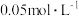 的 的 溶液等体积混合,充分反应后,取少许混合液滴加 溶液等体积混合,充分反应后,取少许混合液滴加 溶液 溶液 | 验证 与 与 的反应有一定限度 的反应有一定限度 |
| B | 相同温度下,分别向两支试管中加入 浓度均为 浓度均为 的草酸溶液,再分别加入 的草酸溶液,再分别加入 和 和 酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色时间不同 酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色时间不同 | 比较反应物浓度对反应速率的影响 |
| C | 相同条件下,向一支试管中加入 和 和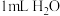 ,向另一支试管中加入 ,向另一支试管中加入 和 和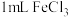 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究 对 对 分解速率的影响 分解速率的影响 |
| D | 向2支盛有 不同浓度 不同浓度 溶液的试管中,同时加入 溶液的试管中,同时加入 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】某同学为探究浓度对化学反应速率的影响,设计以下实验。
下列说法错误的是
| ① | ② | ③ | ④ | |
| 试剂a | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 |
| 试剂b | 2mL0.1mol/LH2C2O4水溶液 | 2mL0.2mol/LH2C2O4水溶液 | 1mL0.2mol/LH2C2O4水溶液 | 1mL以浓盐酸为溶剂配制的0.2mol/LH2C2O4水溶液 |
| 褪色时间 | 690s | 677s | 600s |
| A.对比实验①、②可知,H2C2O4水溶液浓度增大,反应速率加快 |
| B.对比实验②、③可知,酸性高锰酸钾水溶液浓度增大,反应速率加快 |
| C.为验证H+浓度对反应速率的影响,设计实验④并与③对照 |
D.实验③的离子方程式为2 +6H++5H2C2O4=2Mn2++10CO2↑+8H2O +6H++5H2C2O4=2Mn2++10CO2↑+8H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列情况下,反应速率相同的是
| A.等体积0.1 mol/L HCl和0.1 mol/L CH3COOH分别与0.2 mol/L NaOH溶液反应 |
| B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应 |
| C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应 |
| D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应 |
您最近半年使用:0次