如图是元素周期表的一部分。回答下列问题:
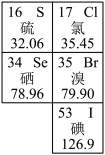
硒是人体必需的微量元素。
(1)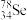 与
与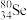 互称为
互称为___________ 。
(2)硒元素的气态氢化物的化学式为___________ 。
(3) 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成硒单质和
气体发生反应,生成硒单质和 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:___________
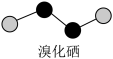
(4)溴化硒是一种重要的电子元件材料,其分子的球棍模型如下图所示。下列说法正确的是___________(填字母)。

硒是人体必需的微量元素。
(1)
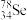 与
与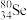 互称为
互称为(2)硒元素的气态氢化物的化学式为
(3)
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成硒单质和
气体发生反应,生成硒单质和 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:(4)溴化硒是一种重要的电子元件材料,其分子的球棍模型如下图所示。下列说法正确的是___________(填字母)。

| A.溴化硒属于离子化合物 | B.原子半径: |
C. 元素的非金属性比 元素的非金属性比 的强 的强 | D.溴化硒的相对分子质量为317.72 |
更新时间:2022-05-26 12:37:25
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________________ 。当1 mol O2发生反应时,还原剂所失电子的物质的量为_________ mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是_____________ 。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________ 。
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_________________ ;该操作将I2还原为I-的目的是________________________ 。
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是________________ 。

(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为________________ ,反应消耗1 mol NaBH4时转移的电子数目为_____________ 。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是

(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2020年11月24日,搭载“嫦娥五号”探测器的“长征五号”大型运载火箭成功发射升空,12月17日“嫦娥五号”返回器顺利返回。
(1)“长征五号”的第一、二子级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4) 做推进剂,该反应的能量转化形式是___________ ,化学方程式为C2H8N2+2N2O4=3N2+4H2O+2X, 则X的化学式是___________ 。
(2)“长征五号”的第三子级火箭采用液氢、液氧做推进剂。制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制氢气。如图所示,制氢过程中,ZnFe2O4的作用是____________ , 该循环制氢中不断消耗的物质是___________ (填化学式)。
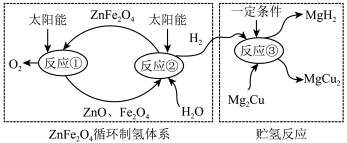
II.贮氢:请写出反应③的化学方程式___________ 。氢化物MgH2与水反应生成一种碱,并释放出H2,其化学方程式为___________ 。
III.如图是氢气和氧气在密闭容器中燃烧的微观示意图,请回答:
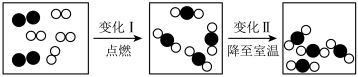
变化I和变化II的本质区别是___________ 。
(3)本次探月的重要任务是寻找月球矿物成分,以探索未来新能源。月壤中含有丰富的氦-3,氦-3是世界公认的高效、清洁、安全的核聚变发电燃料。下列关于氦- 3的叙述正确的是___________(填字母序号)。
(1)“长征五号”的第一、二子级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4) 做推进剂,该反应的能量转化形式是
(2)“长征五号”的第三子级火箭采用液氢、液氧做推进剂。制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制氢气。如图所示,制氢过程中,ZnFe2O4的作用是

II.贮氢:请写出反应③的化学方程式
III.如图是氢气和氧气在密闭容器中燃烧的微观示意图,请回答:

变化I和变化II的本质区别是
(3)本次探月的重要任务是寻找月球矿物成分,以探索未来新能源。月壤中含有丰富的氦-3,氦-3是世界公认的高效、清洁、安全的核聚变发电燃料。下列关于氦- 3的叙述正确的是___________(填字母序号)。
| A.其原子核内质子数为3 | B.其原子核外电子数为2 |
| C.其相对原子质量约为2 | D.其化学性质肯定比较活泼 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2 溶液反应的化学方程式:_____________________________________________________________________________ 。
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______________________________________ 。
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为_______________________________________________________________ 。
(3) Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为___________________________________________________ 。
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
(3) Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的X值。
(1)通过分析X值的变化规律,确定N、Mg的X值范围:___ <X(Mg)<___ ;___ <X(N)<___ 。
(2)推测X值与原子半径的关系是___ 。
(3)某有机物结构简式为 ,在S∼N中,你认为共用电子对偏向谁?
,在S∼N中,你认为共用电子对偏向谁?___ (写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是_______ 。
(5)预测元素周期表中,X值最小的元素位置_______ (放射性元素除外)。
| 元素 | Li | Be | B | C | O | F |
| X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
| 元素 | Na | Al | Si | P | S | Cl |
| X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析X值的变化规律,确定N、Mg的X值范围:
(2)推测X值与原子半径的关系是
(3)某有机物结构简式为
 ,在S∼N中,你认为共用电子对偏向谁?
,在S∼N中,你认为共用电子对偏向谁?(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是
(5)预测元素周期表中,X值最小的元素位置
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分元素,用元素符号或化学式回答下列问题:
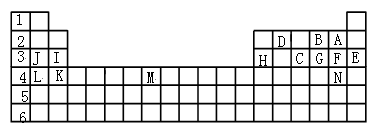
① 表中用字母标出的14种元素中,化学性质最不活泼的是________ ,主族元素中金属性最强的是_______ ,常温下单质为液态的非金属元素是_______ ;属于过渡元素的是_________ 。
②C、G、F气态氢化物的稳定性顺序是______________________ 。
③第三周期中原子半径最小的元素是_______ 。

① 表中用字母标出的14种元素中,化学性质最不活泼的是
②C、G、F气态氢化物的稳定性顺序是
③第三周期中原子半径最小的元素是
您最近一年使用:0次
【推荐3】黑火药的爆炸反应原理为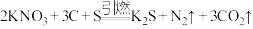 。请回答下列问题:
。请回答下列问题:
(1)基态 原子核外有
原子核外有___________ 种空间运动状态的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为___________ 。
(3)K位于周期表的___________ 区;基态钾离子的电子占据的最高能层符号是___________ 。
(4) 与
与 具有相同的电子构型,
具有相同的电子构型,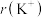 小于
小于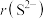 ,原因是
,原因是___________ 。
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是___________ 。
a.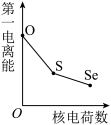 b.
b.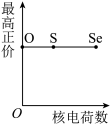 c.
c.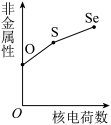 d.
d.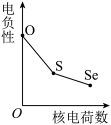
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能 。
。 的Born-Haber循环如图所示。
的Born-Haber循环如图所示。

由图可知, 原子的第二电离能为
原子的第二电离能为___________  ;
; 键的键能为
键的键能为___________  ;氧原子的第一电子亲和能为
;氧原子的第一电子亲和能为___________  ;
; 的晶格能为
的晶格能为___________  。
。
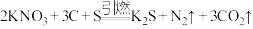 。请回答下列问题:
。请回答下列问题:(1)基态
 原子核外有
原子核外有(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(3)K位于周期表的
(4)
 与
与 具有相同的电子构型,
具有相同的电子构型,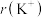 小于
小于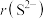 ,原因是
,原因是(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是
a.
 b.
b. c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能
 。
。 的Born-Haber循环如图所示。
的Born-Haber循环如图所示。
由图可知,
 原子的第二电离能为
原子的第二电离能为 ;
; 键的键能为
键的键能为 ;氧原子的第一电子亲和能为
;氧原子的第一电子亲和能为 ;
; 的晶格能为
的晶格能为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①〜⑩种元素,填写下列空白(涉及具体元素对应化学符号表示):
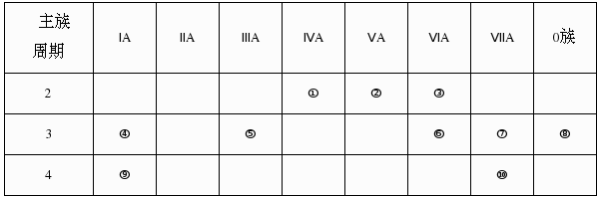
(1)在这些元素中,化学性质最不活泼的是_______ (填元素符号)元素⑩在周期表中的位置______ 。形成化合物最多的元素______ (填序号)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:______ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:_________________ .
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是________ 。
(5)元素③的氢化物的结构式为_____ ;该氢化物在一定条件下可以生成另一种③的氢化物和③的单质。

(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(5)元素③的氢化物的结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第_____ ,周期第_____ 族;
(2)元素②⑤⑥⑧的简单离子半径由大到小的顺序是________ ;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的离子方程式为____ ;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的化学方程式_______ 。
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(pm) | 74 | 102 | 152 | 110 | 99 | 186 | 75 | 143 |
| 最高价态 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低价态 | -2 | -2 | -3 | -1 | -3 |
试回答下列问题:
(1)元素③在周期表中的位置是第
(2)元素②⑤⑥⑧的简单离子半径由大到小的顺序是
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的离子方程式为
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,表中所列的每个序号分别代表某一元素。
(1)元素②在周期表的位置是_______ 。元素③④组成原子个数比为1:1的化合物的电子式_______ 。
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是_______ (填离子符号)。
(3)元素⑩原子最外层电子数是L层电子数的1/4,其二价阳离子的电子数为24,请画出该元素的原子结构示意图_______ 。
(4)写出工业制取元素⑥的单质的化学方程式_______ 。
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于_______ (填“离子化合物”或“共价化合物”);元素⑤与Ga性质相似,下列关于Ga说法错误的是_______ (填写序号)。
A.一定条件下,Ga可溶于强酸与强碱
B.常温下,Ga可与水剧烈反应
C.Ga(OH)3受热能分解
D.一定条件下,Ga2O3可与NaOH溶液反应
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | ⑩ |
(1)元素②在周期表的位置是
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是
(3)元素⑩原子最外层电子数是L层电子数的1/4,其二价阳离子的电子数为24,请画出该元素的原子结构示意图
(4)写出工业制取元素⑥的单质的化学方程式
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于
A.一定条件下,Ga可溶于强酸与强碱
B.常温下,Ga可与水剧烈反应
C.Ga(OH)3受热能分解
D.一定条件下,Ga2O3可与NaOH溶液反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)下列物质中属于同位素的是__________ ;属于同素异形体的是__________ 。
A.O2、O3 B. Cl和
Cl和 Cl
Cl
C.Fe2+、Fe3+ D.H2O、D2O、T2O
(2)据报道,某些花岗岩会产生放射性的稀有气体氡,从而对人体产生伤害,请将以下Rn的原子结构示意图补全。_______

(3)下列四种物质中①Ar,②CO2,③K2S,④NaOH,只有存在共价键的物质是___ ;(填编号)用电子式表示③的形成过程:__________ 。
(4)硅酸盐的组成比较复杂,常用氧化物的形式表示。石棉Mg3Ca(SiO3)4表示为氧化物形式为:__________ 。
(5)若K37ClO3+6H35C1===KCl+3Cl2↑+3H2O,则此反应中生成氯气的相对分子质量约为_________ (计算结果保留三位有效数字)。
(6)将NaHSO4溶于水,破坏了NaHSO4中的______ (填化学键类型),NaHSO4在熔融状态下电离,破坏了______ (填化学键类型),写出其在熔融状态下的电离方程式_____________ 。
(1)下列物质中属于同位素的是
A.O2、O3 B.
 Cl和
Cl和 Cl
Cl C.Fe2+、Fe3+ D.H2O、D2O、T2O
(2)据报道,某些花岗岩会产生放射性的稀有气体氡,从而对人体产生伤害,请将以下Rn的原子结构示意图补全。

(3)下列四种物质中①Ar,②CO2,③K2S,④NaOH,只有存在共价键的物质是
(4)硅酸盐的组成比较复杂,常用氧化物的形式表示。石棉Mg3Ca(SiO3)4表示为氧化物形式为:
(5)若K37ClO3+6H35C1===KCl+3Cl2↑+3H2O,则此反应中生成氯气的相对分子质量约为
(6)将NaHSO4溶于水,破坏了NaHSO4中的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.(1)写出表示含有8个质子、10个中子的原子的化学符号_______ 。
(2)元素周期表中,所含元素超过18种的周期是_______ 。
Ⅱ.有:① 168O、178O、188O ②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是_______ ;
(2)互为同素异形体的是_______ ;
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合物中分子量最大的是_______ (填化学式)。
(2)元素周期表中,所含元素超过18种的周期是
Ⅱ.有:① 168O、178O、188O ②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是
(2)互为同素异形体的是
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合物中分子量最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对于数以千万计的化学物质及各种微量,分类法的作用几乎是无可替代的。
(1)下列7种微粒 、
、 、
、 、
、 、
、 、
、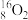 、
、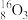 中有
中有____ 种核素,含有____ 种元素,其中  与
与 ;
;____ 与____ 互称为____ , 、
、 具有相同的
具有相同的____ 。
(2)现有以下8种物质:① Cu ② BaSO4晶体 ③熔融的NaCl ④Fe(OH)3胶体 ⑤纯硫酸 ⑥CO2 ⑦氯气 ⑧石灰水
①属于混合物的是(填序号,下同)____ ;
②能导电的单质是____ ;
③属于电解质的是____ ;
④属于非电解质的是____ 。
(1)下列7种微粒
 、
、 、
、 、
、 、
、 、
、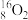 、
、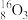 中有
中有 与
与 ;
; 、
、 具有相同的
具有相同的(2)现有以下8种物质:① Cu ② BaSO4晶体 ③熔融的NaCl ④Fe(OH)3胶体 ⑤纯硫酸 ⑥CO2 ⑦氯气 ⑧石灰水
①属于混合物的是(填序号,下同)
②能导电的单质是
③属于电解质的是
④属于非电解质的是
您最近一年使用:0次



