元素周期表中7种元素分别用X、Y、Z、M、Q、R、W表示。X原子是最外层电子排布为nsn的非金属元素,Y原子核外的L层电子数是K层的2倍,Z是地壳内含量最高的元素,M原子的3p能级有一个空轨道,q元素为短周期元素中金属性最强的元素,请回答下列问题:
(1)Y、Z、M、Q四种元素的第一电离能由大到小的顺序为_______ (用元素符号和“>”表示)。
(2)R、W形成的合金其晶胞结构如图1所示:
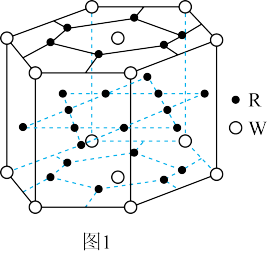
则它的化学式为_______ 。
(3)Z和Q形成的化合物可能含有的化学键有_______ ,Y、Z和Q三种元素共同形成的常见6原子化合物中,阴离子的中心原子杂化类型为 _______ ,立体空间构型为 _______ 。
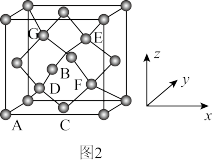
(4)如图2为M单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则E原子的坐标参数为
,0)。则E原子的坐标参数为 _______ ;已知M单晶的晶胞参数apm,其密度为 _______  。
。
(1)Y、Z、M、Q四种元素的第一电离能由大到小的顺序为
(2)R、W形成的合金其晶胞结构如图1所示:

则它的化学式为
(3)Z和Q形成的化合物可能含有的化学键有
(4)如图2为M单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则E原子的坐标参数为
,0)。则E原子的坐标参数为  。
。
更新时间:2022-05-29 10:47:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B、A与X均可形成10个电子化合物;B的最高价含氧酸可与其气态氢化物反应生成盐,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液先变红后褪色。
用元素符号或化学式回答下列问题。
(1)X在周期表中的位置是______________ ;
(2)化合物Y2X2的电子式为__________ ,它含有的化学键类型有_________ (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)X、Z的简单氢化物中沸点较高的是_______ (填化学式),原因是__________________ 。
(4)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:___________________ ;
(5)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为:___________
用元素符号或化学式回答下列问题。
(1)X在周期表中的位置是
(2)化合物Y2X2的电子式为
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)X、Z的简单氢化物中沸点较高的是
(4)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:
(5)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有A、B、C、D、E五种元素,它们可能是原子或离子,且为短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素。金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍。D的气态氢化物水溶液显碱性,而其最高价氧化物水化物为强酸。E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个。
(1)写出A元素名称:______ ,C2粒子的符号:______ 。
(2)画出E离子的结构示意图:______ ,E的氢化物的分子式______ 。
(3)写出B与E化合的化学方程式:______ 。
(4)写出A的单质、B的单质分别与水反应的溶液混合后发生的反应的离子方程式:______ 。
(5)A与C形成的化合物中含化学键类型是:______ ,用电子式表示该化合物:______ 。
(1)写出A元素名称:
(2)画出E离子的结构示意图:
(3)写出B与E化合的化学方程式:
(4)写出A的单质、B的单质分别与水反应的溶液混合后发生的反应的离子方程式:
(5)A与C形成的化合物中含化学键类型是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z是原子序数依次递减的四种常见元素。X元素是地壳中含量最多的元素,Y、Z组成的气态化合物M可做制冷剂,其水溶液呈碱性,W的单质在X2中燃烧产物可使品红溶液褪色,请回答:
(1)W元素原子结构示意图是___________ ;该元素最高正化合价与最低负化合价分别是__________ 和__________ 。
(2)Y元素的最高价氧化物的水化物与其氢化物反应的化学方程式是____________ 。
(3)由以上四种元素的其中三种元素所形成的氧化物中,有一种物质能与水反应生成气体,且该反应属于氧化还原反应,请写出该反应的化学方程式__________________________ ,其中氧化剂和还原剂的物质的量之比是:__________________ 。
(1)W元素原子结构示意图是
(2)Y元素的最高价氧化物的水化物与其氢化物反应的化学方程式是
(3)由以上四种元素的其中三种元素所形成的氧化物中,有一种物质能与水反应生成气体,且该反应属于氧化还原反应,请写出该反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】2020年,智能材料已大量涌现,为生物医疗、国防军事以及航空航天等领域发展提供支撑。
(1)快离子导体是具有优良离子导电能力的固体电解质。反应 的产物分子中形成配位键提供孤电子对的配位原子名称是
的产物分子中形成配位键提供孤电子对的配位原子名称是______ 。
(2)第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。基态Ga原子价电子排布图为______ ,第一电离能介于硼和氮之间的第二周期元素有______ 种。
(3)金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。钛(Ti)在元素周期表中位于______ (周期,族,区),钛(Ti)的基态原子M能层中有______ 种空间运动状态的电子。
(4)镍能形成多种配合物,如正四面体形的 和正方形的
和正方形的 、正八面体形的
、正八面体形的 等。下列说法正确的有
等。下列说法正确的有______ (填标号)。
A.CO与 互为等电子体,其中CO分子内
互为等电子体,其中CO分子内 键和
键和 键个数之比为1∶2
键个数之比为1∶2
B. 在形成配合物时,其配位数只能为4
在形成配合物时,其配位数只能为4
C.沸点: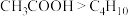 ,因为
,因为 分子间范德华力更强
分子间范德华力更强
D.键角: ,因为
,因为 的成键电子对间的排斥力更大
的成键电子对间的排斥力更大
E.极性:F―C>Cl―C,因此酸性
(5)一种四方结构( )的超导化合物汞钡铜氧晶体的晶胞如图所示。
)的超导化合物汞钡铜氧晶体的晶胞如图所示。______  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)快离子导体是具有优良离子导电能力的固体电解质。反应
 的产物分子中形成配位键提供孤电子对的配位原子名称是
的产物分子中形成配位键提供孤电子对的配位原子名称是(2)第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。基态Ga原子价电子排布图为
(3)金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。钛(Ti)在元素周期表中位于
(4)镍能形成多种配合物,如正四面体形的
 和正方形的
和正方形的 、正八面体形的
、正八面体形的 等。下列说法正确的有
等。下列说法正确的有A.CO与
 互为等电子体,其中CO分子内
互为等电子体,其中CO分子内 键和
键和 键个数之比为1∶2
键个数之比为1∶2B.
 在形成配合物时,其配位数只能为4
在形成配合物时,其配位数只能为4C.沸点:
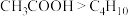 ,因为
,因为 分子间范德华力更强
分子间范德华力更强D.键角:
 ,因为
,因为 的成键电子对间的排斥力更大
的成键电子对间的排斥力更大E.极性:F―C>Cl―C,因此酸性

(5)一种四方结构(
 )的超导化合物汞钡铜氧晶体的晶胞如图所示。
)的超导化合物汞钡铜氧晶体的晶胞如图所示。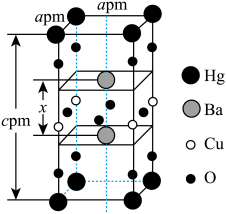
 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】有五种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填空:
(1)A原子的核外电子排布式为___________ 。
(2)B元素在周期表中的位置:__________________ ;离子半径:B___ A(填“大于”或“小于”)
(3)C原子的价电子排布图是___________ ,其原子核外有__________ 个未成对电子,能量最高的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(4)D原子的电子排布式为___________ 。D-的结构示意图是________________
(5)C、E元素的第一电离能的大小关系是___________ (用元素符号表示)。
(6)已知CD3分子中D元素为+1价,则C、D的电负性大小关系是________________ (用元素符号表示),CD3与水反应后的产物是__________ 和__________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
| E | L层上有2对成对电子 |
请根据表中信息填空:
(1)A原子的核外电子排布式为
(2)B元素在周期表中的位置:
(3)C原子的价电子排布图是
(4)D原子的电子排布式为
(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素为+1价,则C、D的电负性大小关系是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
(1)C基态原子中能量最高的电子,其电子云在空间有___ 个方向,原子轨道呈___ 形,C简单离子核外有__ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:__ 。
(3)G位于__ 族__ 区,它的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为___ 。
(4)ED3分子的VSEPR模型名称为__ ,其中E原子的杂化轨道类型为__ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数与s电子数相等 |
| C基态原子的价电子排布为nsn-1npn+1 |
| D的能层数与C相同,且电负性比C大 |
| E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第五列 |
(2)A2B2难溶于CS2,简要说明理由:
(3)G位于
(4)ED3分子的VSEPR模型名称为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、R、I、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,I的原子序数是W的两倍,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________ ,Y的电子排布图为_________________________
(2)化合物ZX3中Z原子的杂化方式为___________ ,ZW2- 离子的立体构型是___________ ;
(3)①Y、R的最高价氧化物的沸点较高的是___________ (填化学式),原因是___________ ;
②W与I的简单氢化物中W的熔沸点更高,原因是______________________
(4)向Q元素的硫酸盐溶液中通入足量ZX3,充分反应后溶液呈深蓝色,该反应的离子方程式为__________________________________________________ ;
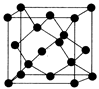
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________ ,Y原子的配位数为___________ ,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏伽德罗常数的数值为___________ (用含a和ρ的代数式表示)。
(1)Q+核外电子排布式为
(2)化合物ZX3中Z原子的杂化方式为
(3)①Y、R的最高价氧化物的沸点较高的是
②W与I的简单氢化物中W的熔沸点更高,原因是
(4)向Q元素的硫酸盐溶液中通入足量ZX3,充分反应后溶液呈深蓝色,该反应的离子方程式为
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号______ 。
(2)最外层电子排布为4s24p1的原子的核电荷数为______ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4该元素的名称是______ 。
(4)根据VSEPR模型,H3O+的分子立体结构为:______ ,SO2的立体结构为:______ 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为______ 。
(6)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为______ 。
(7)某元素核外有三个电子层,最外层电子数是核外电子总数的 ,写出该元素原子的电子排布式是
,写出该元素原子的电子排布式是______ 。
(8)写出铬元素在周期表中的位置______ ,它位于______ 区。
(1)含有8个质子,10个中子的原子的化学符号
(2)最外层电子排布为4s24p1的原子的核电荷数为
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4该元素的名称是
(4)根据VSEPR模型,H3O+的分子立体结构为:
(5)周期表中最活泼的非金属元素原子的轨道表示式为
(6)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为
(7)某元素核外有三个电子层,最外层电子数是核外电子总数的
 ,写出该元素原子的电子排布式是
,写出该元素原子的电子排布式是(8)写出铬元素在周期表中的位置
您最近一年使用:0次
【推荐3】北京冬奥会上采用二氧化碳跨临界制冰,使人们再次看到了二氧化碳综合化利用的巨大前景,转化 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。
(1) 电催化制
电催化制 。在电解过程中向电解质中加入离子导体M(
。在电解过程中向电解质中加入离子导体M(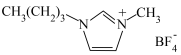 )可以提高
)可以提高 的选择性(
的选择性( 的选择性是指
的选择性是指 转化生成
转化生成 的百分比,下同)。
的百分比,下同)。
①离子导体M中采取 杂化类型的原子有
杂化类型的原子有___________ 。
②电催化还原 制
制 的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图___________ 。

(2) 热还原制
热还原制 和
和 。在
。在 、
、 催化下,
催化下, 和
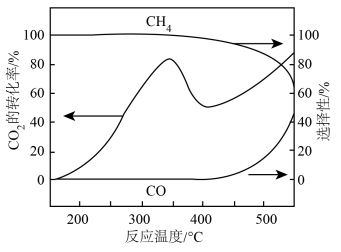
和 混和气体(体积比1:4)进行反应,测得
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和
和 的选择性随温度变化如图所示。
的选择性随温度变化如图所示。
反应Ⅰ: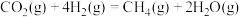

反应Ⅱ:

①400℃后,随温度升高 转化率不断上升的原因是
转化率不断上升的原因是___________ 。
②525℃下,向恒容密闭容器中充入上述混合气体进行反应,体系达到平衡时 的体积分数为
的体积分数为___________ ,反应Ⅱ平衡常数K为___________ 。
③反应Ⅱ中 和
和 在
在 (存O空位)催化剂的作用下,可以提高
(存O空位)催化剂的作用下,可以提高 的选择性,反应过程如图所示。从电负性的角度分析,过程①和②能发生的反应机理
的选择性,反应过程如图所示。从电负性的角度分析,过程①和②能发生的反应机理___________ 。

 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。(1)
 电催化制
电催化制 。在电解过程中向电解质中加入离子导体M(
。在电解过程中向电解质中加入离子导体M( )可以提高
)可以提高 的选择性(
的选择性( 的选择性是指
的选择性是指 转化生成
转化生成 的百分比,下同)。
的百分比,下同)。①离子导体M中采取
 杂化类型的原子有
杂化类型的原子有②电催化还原
 制
制 的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
(2)
 热还原制
热还原制 和
和 。在
。在 、
、 催化下,
催化下, 和
和 混和气体(体积比1:4)进行反应,测得
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和
和 的选择性随温度变化如图所示。
的选择性随温度变化如图所示。
反应Ⅰ:
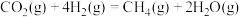

反应Ⅱ:


①400℃后,随温度升高
 转化率不断上升的原因是
转化率不断上升的原因是②525℃下,向恒容密闭容器中充入上述混合气体进行反应,体系达到平衡时
 的体积分数为
的体积分数为③反应Ⅱ中
 和
和 在
在 (存O空位)催化剂的作用下,可以提高
(存O空位)催化剂的作用下,可以提高 的选择性,反应过程如图所示。从电负性的角度分析,过程①和②能发生的反应机理
的选择性,反应过程如图所示。从电负性的角度分析,过程①和②能发生的反应机理
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁、钴、镍的性质非常相似,称为铁系元素。回答下列问题:
(1)Fe在元素周期表中的位置为_______ (填周期和族),基态Ni原子的价电子排布式为_______ 。
(2)Fe3+的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是_______ ,第一电离能最小的是_______ ;SCN-中碳原子的杂化轨道类型为_______ 。
(3)Co2+在水溶液中以[Co(H2O)6]2+的形式存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,试分析[Co(NH3)6]2+更稳定的原因是_______ 。
(4)NiSO4常用于电镀工业,其中SO 的空间构型为
的空间构型为_______ 。
(5)Ni和La的合金是良好的储氢材料。该合金的晶胞结构如图所示(Ni原子中只有1个在晶胞体心,其余都在晶胞面上):
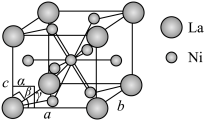
该合金的化学式为_______ ;已知阿伏加德罗常数的值为NA,晶胞参数为a=b=511pm,c=397 pm;α=β=90°,r=60°。计算该合金的密度ρ=_______ g·cm-3(列出计算式即可)
(1)Fe在元素周期表中的位置为
(2)Fe3+的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是
(3)Co2+在水溶液中以[Co(H2O)6]2+的形式存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,试分析[Co(NH3)6]2+更稳定的原因是
(4)NiSO4常用于电镀工业,其中SO
 的空间构型为
的空间构型为(5)Ni和La的合金是良好的储氢材料。该合金的晶胞结构如图所示(Ni原子中只有1个在晶胞体心,其余都在晶胞面上):

该合金的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1.其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。
(1)写出元素D在周期表中的位置是____ ,B原子的外围电子排布图____ 。E原子的核外有____ 种不同运动状态的电子,B和C的第一电离能大小关系____ 。(用元素符号表示)
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,画出原子个数比为1:1的化合物的电子式_______ ,两种化合物可任意比互溶,解释其主要原因为_______ 。
(3)该配位化合物的化学式为_______ 。
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为_______ 。
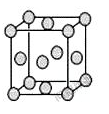
(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为pg∙cm-3,则阿伏伽德罗常数为_______ (用a、p表示)。该晶胞配位数为_______ ,EDC4常作电镀液,其中DC 的空间构型是
的空间构型是_______ ,其中D原子的杂化轨道类型是_______ 。若电解EDC4的水溶液,则电解总反应的化学方程式为_______ 。
(1)写出元素D在周期表中的位置是
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,画出原子个数比为1:1的化合物的电子式
(3)该配位化合物的化学式为
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为

(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为pg∙cm-3,则阿伏伽德罗常数为
 的空间构型是
的空间构型是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某废旧锂电池正极材料中含有LiCoO2、LiMnO2以及有机物、碳粉等,以该正极材料为原料可制备CoCO3和Li2CO3。
已知:Ksp[Co(OH)2]=1.6×10-15,Ksp[CoCO3]=1.4×10-13。
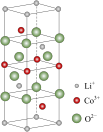
(1)热解。将正极材料加热。LiCoO2的晶胞如图所示,各离子位于晶胞的顶点、棱和体内。晶胞中Co3+的数目是___________ 。
(2)浸出。热解所得产物含Li+、Co3+、Mn3+等,向其中加入H2O2和稀H2SO4,充分反应,过滤,得到含Li+、Co2+、Mn2+的浸出液。H2O2在该过程中的作用为___________ 。
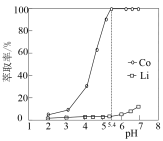
(3)分离。向浸出液中加入有机萃取剂HA,发生反应:Co2++2HA CoA2+2H+,将CoA2萃取入有机相中,HA对金属离子的萃取率与pH的关系如图所示。分液后,再从有机相中反萃取得到CoSO4溶液的操作是
CoA2+2H+,将CoA2萃取入有机相中,HA对金属离子的萃取率与pH的关系如图所示。分液后,再从有机相中反萃取得到CoSO4溶液的操作是___________ 。
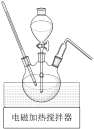
(4)制备CoCO3.用CoSO4溶液与NH4HCO3−氨水混合溶液反应制备CoCO3,装置如图所示。分液漏斗中盛装的溶液为___________ ,该反应的离子方程式为___________ 。
(5)制备Li2CO3.已知:常温下,LiOH易溶于水,Li2CO3的溶解度为1.3 g;pH约为10时,Mn(OH)2完全沉淀。请补充完整制取纯度较高的Li2CO3的实验方案:取(3)中萃取、分液后的水层溶液(含少量Mn2+),___________ ,得到纯度较高的Li2CO3。(实验中可使用的试剂:1.0 mol·L−1NaOH溶液、1.0 mol·L−1 H2SO4溶液、稀盐酸、BaCl2溶液、1.0 mol·L−1 Na2CO3溶液)
已知:Ksp[Co(OH)2]=1.6×10-15,Ksp[CoCO3]=1.4×10-13。
(1)热解。将正极材料加热。LiCoO2的晶胞如图所示,各离子位于晶胞的顶点、棱和体内。晶胞中Co3+的数目是

(2)浸出。热解所得产物含Li+、Co3+、Mn3+等,向其中加入H2O2和稀H2SO4,充分反应,过滤,得到含Li+、Co2+、Mn2+的浸出液。H2O2在该过程中的作用为
(3)分离。向浸出液中加入有机萃取剂HA,发生反应:Co2++2HA
 CoA2+2H+,将CoA2萃取入有机相中,HA对金属离子的萃取率与pH的关系如图所示。分液后,再从有机相中反萃取得到CoSO4溶液的操作是
CoA2+2H+,将CoA2萃取入有机相中,HA对金属离子的萃取率与pH的关系如图所示。分液后,再从有机相中反萃取得到CoSO4溶液的操作是
(4)制备CoCO3.用CoSO4溶液与NH4HCO3−氨水混合溶液反应制备CoCO3,装置如图所示。分液漏斗中盛装的溶液为

(5)制备Li2CO3.已知:常温下,LiOH易溶于水,Li2CO3的溶解度为1.3 g;pH约为10时,Mn(OH)2完全沉淀。请补充完整制取纯度较高的Li2CO3的实验方案:取(3)中萃取、分液后的水层溶液(含少量Mn2+),
您最近一年使用:0次



