部分弱酸的电离平衡常数如下表:
下列选项错误的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
A.2CN-+H2O+CO2=2HCN+CO |
B.2HCOOH+CO =2HCOO-+H2O+CO2↑ =2HCOO-+H2O+CO2↑ |
C.由数据可知酸性:HCOOH>H2CO3>HCN>HCO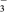 |
| D.25 ℃时,在等浓度的CH3COOH溶液和HCN溶液中,水的电离程度后者大 |
2022高三·全国·专题练习 查看更多[6]
(已下线)选择题1-5作业(十四) 水的电离 溶液的酸碱性与 pH广东省广州市第八十六中学2022-2023学年高二上学期期中考试化学试题河南省新乡市第一中学2022-2023学年高二上学期第一次月考化学试题(已下线)第23讲 弱电解质的电离平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第31练 水的电离和溶液的pH-2023年高考化学一轮复习小题多维练(全国通用)
更新时间:2022-07-26 21:20:56
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列各反应对应的离子方程式正确的是
A.向100 mL 0.12 mol·L−1的Ba(OH)2溶液中通入0.02 mol CO2: Ba2++3OH−+2CO2=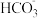 +BaCO3↓+H2O +BaCO3↓+H2O |
B.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2OH−+2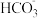 = = CaCO3↓+ CaCO3↓+ +2H2O +2H2O |
C.硫酸氢钠与氢氧化钡两种溶液反应后溶液恰好呈中性:H++ +Ba2++OH−=BaSO4↓+H2O +Ba2++OH−=BaSO4↓+H2O |
D.向含0.1 mol NaOH和0.2molNa2CO3的溶液中加入1L0.4 mol·L−1稀盐酸:OH−+ +3H+=CO2↑+2H2O +3H+=CO2↑+2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列离子方程式书写正确的是
| A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓ |
| B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑ |
| C.利用腐蚀法制作印刷线路板:2Fe3+ + Cu ="=" 2Fe2+ + Cu2+ |
D.AgNO3溶液中加入过量氨水: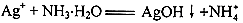 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列离子方程式中正确的是
A.用Pt电极电解少量的CuC12溶液:2H2O+Cu2++2Cl- H2↑+C12↑+Cu(OH)2↓ H2↑+C12↑+Cu(OH)2↓ |
B.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:NH +Al3++2SO +Al3++2SO +2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O +2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O |
C.酸性高锰酸钾溶液中滴加H2O2溶液4MnO +4H2O2+12H+=4Mn2++7O2↑+10H2O +4H2O2+12H+=4Mn2++7O2↑+10H2O |
| D.向磁性氧化铁中加入氢碘酸:Fe3O4+8H+=Fe2++2Fe3++4H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,NH3•H2O的Kb约为10-5。在下列装置中存在不同pH的两种溶液,溶液中离子不能穿过隔膜,分子可以自由穿过隔膜(如图所示)。已知c起始(NH3•H2O)=c平衡(NH3•H2O)+c(NH )。当达到平衡时,下列叙述正确的是
)。当达到平衡时,下列叙述正确的是

 )。当达到平衡时,下列叙述正确的是
)。当达到平衡时,下列叙述正确的是
A.溶液I中c(OH-)=c(H+)+c(NH ) ) |
| B.溶液I和II中的c平衡(NH3•H2O)不相等 |
C.溶液II中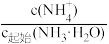 为0.1 为0.1 |
| D.溶液I和II中c起始I(NH3•H2O):c起始II(NH3•H2O)=101:11 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知25℃时有关弱酸的电离平衡常数如下:
则下列有关说法正确的是
| 弱酸化学式 |  | HCN |  |
| 电离平衡常数 |  |  |  |
A.浓度均为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 |
B.等体积等浓度的上述三种酸溶液中, 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b |
C.NaCN溶液中通入少量 发生的化学反应为 发生的化学反应为 |
D.稀释HCN溶液过程中, 减小 减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】设阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.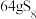 (分子结构: (分子结构: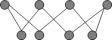 )中的共价键数目为 )中的共价键数目为 |
B.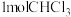 ,含有 ,含有 键的数目为 键的数目为 |
C. 溶液中含有的 溶液中含有的 离子数为 离子数为 |
D.标准状况下, 甲烷和乙烯混合物中含有的氢原子数为 甲烷和乙烯混合物中含有的氢原子数为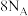 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
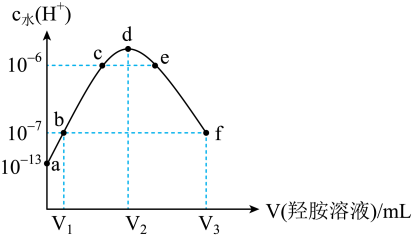
【推荐1】常温下,向20 mL的某稀盐酸中滴入0.1 mol·L-1的羟胺溶液, 羟胺的电离方程式为:NH2OH+H2O  NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
 NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
| A.0.1 mol·L-1羟胺溶液的 pH=8.5 | B.b点溶液中:c(H+) =c(OH-) |
| C.d点对应溶液中存在:c(H+)=c (OH-)+c (NH2OH) | D.该稀盐酸的浓度为0.2 mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,用 溶液滴定二元弱酸
溶液滴定二元弱酸 溶液,图中直线①表示溶液中
溶液,图中直线①表示溶液中 和
和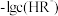 的关系,直线②表示
的关系,直线②表示 和
和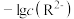 的关系。下列说法错误的是
的关系。下列说法错误的是

 溶液滴定二元弱酸
溶液滴定二元弱酸 溶液,图中直线①表示溶液中
溶液,图中直线①表示溶液中 和
和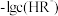 的关系,直线②表示
的关系,直线②表示 和
和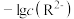 的关系。下列说法错误的是
的关系。下列说法错误的是
A.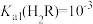 |
B.滴定过程中,当pH=6时,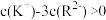 |
C.若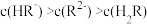 ,则pH范围为 ,则pH范围为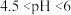 |
D.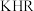 的溶液中: 的溶液中: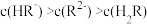 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
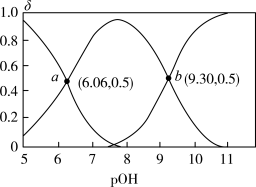
【推荐3】联氨(又称肼,N2H4是无色液体)为二元弱碱,在水中的电离方式与氨相似。常温下,向10mL0.1mol/L的联氨溶液中,滴加0.1mol/L的HCl溶液xmL溶液中N2H4、 、
、 的物质的量分数δ随溶液pOH[pOH=-lgc(OH-)]变化的曲线如图所示,下列说法错误的是
的物质的量分数δ随溶液pOH[pOH=-lgc(OH-)]变化的曲线如图所示,下列说法错误的是
 、
、 的物质的量分数δ随溶液pOH[pOH=-lgc(OH-)]变化的曲线如图所示,下列说法错误的是
的物质的量分数δ随溶液pOH[pOH=-lgc(OH-)]变化的曲线如图所示,下列说法错误的是
| A.联氨与硫酸形成的酸式盐的化学式为N2H6(HSO4)2 |
| B.pOH=6.06时,加入HCl溶液的体积为5mL |
C.加入HCl溶液体积为10mL时溶液中:2c( )+c( )+c( )<c(Cl-) )<c(Cl-) |
D.反应N2H4+H+  的K=107.94 的K=107.94 |
您最近一年使用:0次



