根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是
①Cl2+2KI=I2+2KCl ②2FeCl3+2HI=I2+2FeCl2+2HCl ③2FeCl2+Cl2=2FeCl3
①Cl2+2KI=I2+2KCl ②2FeCl3+2HI=I2+2FeCl2+2HCl ③2FeCl2+Cl2=2FeCl3
| A.Cl2>I2>Fe3+ | B.Fe3+>Cl2>I2 |
| C.Cl2>Fe3+>I2 | D.I2>Fe3+>Cl2 |
21-22高一上·上海静安·期中 查看更多[2]
更新时间:2022-08-25 18:45:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】溴酸盐在国际上被定位为2B级潜在致癌物。从2009年10月1日起,我国实行矿泉水新标准,首次规定矿泉水中溴酸盐的含量最高不得超过0.01 mg·L-1。已知KBrO3可发生下列反应:2KBrO3 + I2 = 2KIO3 + Br2,下列有关溴酸钾的说法不 正确的是 ( )
| A.溴酸钾既有氧化性又有还原性 | B.该反应说明I2也可以置换出Br2 |
| C.该反应说明I2的还原性强于Br2 | D.该反应与2KI+Br2=2KBr+I2相矛盾 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知如下三个实验均能发生化学反应,下列判断正确的是
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向FeSO4溶液中滴入几滴氯水 | 将铜丝放入氯化铁溶液中 |
| A.上述实验证明氧化性:Fe3+>Cu2+>Fe2+ |
| B.实验②中Fe2+既显氧化性又显还原性 |
| C.实验③中发生的是置换反应 |
| D.实验①中铁作氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验操作、现象、结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 过量铁粉加入稀硝酸中,充分反应后,滴加KSCN溶液 | 有无色气泡产生,溶液呈血红色 | 稀硝酸能将Fe氧化成Fe3+ |
| B | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性: |
| C | 向某溶液中滴加几滴新制氯水,再滴加少量KSCN 溶液 | 溶液呈血红色 | 溶液中含有Fe2+ |
| D | 铁放置于浓硝酸中 | 无明显变化 | 铁与浓硝酸常温下会发生钝化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应属于氧化还原反应,且水既不作氧化剂又不作还原剂的是
| A.2F2+2H2O=4HF+O2 |
| B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.2H2O+2Na=2NaOH+H2↑ |
D.2H2O O2↑+2H2↑ O2↑+2H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】硝酸盐污染已成为一个日益严重的环境问题。甲酸( HCOOH)在纳米级Pd表面分解为活性H2和CO2,再经下列历程实现NO 的催化还原,进而减少污染。已知Fe( II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法错误的是
的催化还原,进而减少污染。已知Fe( II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法错误的是
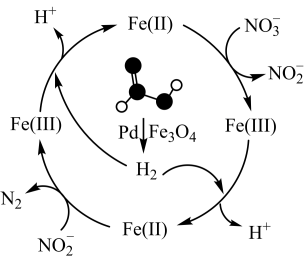
 的催化还原,进而减少污染。已知Fe( II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法错误的是
的催化还原,进而减少污染。已知Fe( II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法错误的是
| A.Fe3O4参与了该循环历程 |
| B.HCOOH分解时,碳氢键和氧氢键发生了断裂 |
| C.H2在反应历程中生成的H+起到调节体系pH的作用 |
D.在整个历程中,1 mol H2可还原1 mol NO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol·L-1NaOH溶液,整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是


| A.向a点所示溶液中通入SO2,溶液的酸性和漂白性均增强 |
| B.b点所示的溶液中:c(H+)>c(Cl-)>c(HClO)>c(ClO-)>c(OH-) |
| C.a点和c点溶液中水的电离程度相同 |
| D.d点所示溶液中:c(Na+)=c(ClO-)+2c(HClO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式正确的是
A.向含2 mol  的溶液中通入1 mol 的溶液中通入1 mol  : : |
B.氯气溶于水中: |
C.向 溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: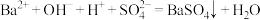 |
D.钠与水反应: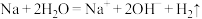 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列各组物质的转化关系中,不能全部通过一步反应完成的是
A. | B.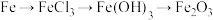 |
C.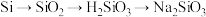 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成一种无限长链离子,其片段为 ;CN-结合H+能力弱于C
;CN-结合H+能力弱于C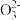 。氰化物浓度较低时,可在碱性条件下用H2O2或Cl2将其转化为N2;浓度较高时,可加入HCN、Fe和K2CO3溶液反应生成K4[Fe(CN)6]溶液。下列物质性质与用途具有对应关系的是
。氰化物浓度较低时,可在碱性条件下用H2O2或Cl2将其转化为N2;浓度较高时,可加入HCN、Fe和K2CO3溶液反应生成K4[Fe(CN)6]溶液。下列物质性质与用途具有对应关系的是
 ;CN-结合H+能力弱于C
;CN-结合H+能力弱于C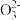 。氰化物浓度较低时,可在碱性条件下用H2O2或Cl2将其转化为N2;浓度较高时,可加入HCN、Fe和K2CO3溶液反应生成K4[Fe(CN)6]溶液。下列物质性质与用途具有对应关系的是
。氰化物浓度较低时,可在碱性条件下用H2O2或Cl2将其转化为N2;浓度较高时,可加入HCN、Fe和K2CO3溶液反应生成K4[Fe(CN)6]溶液。下列物质性质与用途具有对应关系的是| A.H2O2具有还原性,可用于处理含氰废水 |
| B.维生素C具有还原性,可用作食品抗氧化剂 |
| C.FeCl3溶液显酸性,可用于刻蚀铜板 |
| D.NaHCO3受热易分解,可用于治疗胃酸过多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】(2018·北京市西城区4月一模)下列解释事实的方程式书写正确的是
| A.Na2CO3溶液处理水垢中的CaSO4:Ca2+ + CO32− == CaCO3↓ |
| B.Na2O2作呼吸面具的供氧剂:2Na2O2 + 2CO2 == 2 Na2CO3 + O2 |
| C.稀HNO3洗涤做过银镜反应的试管:Ag + 2H+ + NO3− == Ag+ + NO2↑ + H2O |
| D.FeCl3溶液腐蚀线路板:Fe3+ + Cu == Fe2+ + Cu2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】由下列实验操作和现象得出的结论错误的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下,分别用浓HNO3和稀HNO3与铁反应 | 稀HNO3与铁反应快 | 其它条件相同,反应物浓度越小,反应速率越快 |
| B | 往盛有FeCl3溶液的试管中滴加几滴淀粉-碘化钾溶液 | 溶液变蓝 | 氧化性:Fe2+>I2 |
| C | 常温下,向三支试管中分别加入1mL0.1mol/L、0.2mol/L、0.3mol/LNa2S2O3溶液,再同时分别加入2mL0.5mol/L稀硫酸 | 加入0.3mol/LNa2S2O3溶液的试管最先沉淀 | 其它条件相同,c(Na2S2O3)越大,反应生成S的速率越快 |
| D | 向盛有稀盐酸的试管中加入铁粉 | 刚开始时一段时间内产生气泡的速率加快 | 铁与稀盐酸反应放出热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

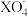 =2X2++5Z2+8H2O,②2M2++R2=2M3++2R-,③2R-+Z2=R2+2Z-。由此判断,下列说法中正确的是
=2X2++5Z2+8H2O,②2M2++R2=2M3++2R-,③2R-+Z2=R2+2Z-。由此判断,下列说法中正确的是

