有效氯的含量是漂白粉的主要指标,有效氯含量的实质是指单位质量的含氯化合物中所含氧化态氯的氧化能力相当于多少纯净氯气的氧化能力,有效氯含量越高,漂白粉的效力就越大。有效氯的测定方法是将漂白粉与盐酸反应,生成氯气通入KI溶液,置换出碘,进而通过碘与淀粉的显色反应确定碘的量,便可确定漂白粉中有效氯的含量。反应的化学方程式是:
Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O……①
Cl2+2KI=2KCl+I2……②
(1)请用单线桥标出反应①的电子转移方向和数目_______ 。
(2)Cl2在反应①中是_______ ,在反应②中是_______ 。
a.氧化剂 b.还原剂 c.氧化产物 d.还原产物
(3)在反应①中,氧化剂与还原剂的物质的量之比为_______ ,当电子转移1mol,则还原产物的质量是_______ g。
(4)反应①中需要采用浓度较大的盐酸,如盐酸浓度不够,会发生反应③,化学反应方程式如下:
Ca(ClO)2+2HCl=CaCl2+2HClO……③
为何①和③反应物的类别相同,发生的反应却不同,请从氧化还原的角度解释原因_______ 。
Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O……①
Cl2+2KI=2KCl+I2……②
(1)请用单线桥标出反应①的电子转移方向和数目
(2)Cl2在反应①中是
a.氧化剂 b.还原剂 c.氧化产物 d.还原产物
(3)在反应①中,氧化剂与还原剂的物质的量之比为
(4)反应①中需要采用浓度较大的盐酸,如盐酸浓度不够,会发生反应③,化学反应方程式如下:
Ca(ClO)2+2HCl=CaCl2+2HClO……③
为何①和③反应物的类别相同,发生的反应却不同,请从氧化还原的角度解释原因
更新时间:2022-08-29 20:02:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】铁是一种比较活泼的金属,在日常生活和工业上都有重要的用途。
(1)铁与稀硫酸反应的离子方程式是___________ 。
(2)在常温下,铁与水不发生反应,在高温下,红热的铁与水蒸气发生反应,生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g) Fe3O4+4H2。
Fe3O4+4H2。
①作为氧化剂的物质是________ ,铁元素被________ 。(填“氧化”或“还原”)
②若消耗3molFe,则生成氢气的体积为_____ L(标准状况),转移电子的物质的量是_____ mol。
(1)铁与稀硫酸反应的离子方程式是
(2)在常温下,铁与水不发生反应,在高温下,红热的铁与水蒸气发生反应,生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g)
 Fe3O4+4H2。
Fe3O4+4H2。①作为氧化剂的物质是
②若消耗3molFe,则生成氢气的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)离子方程式的书写:
①氢氧化铜与硫酸_______ ;
②碳酸氢钠与盐酸______ ;
③除去铜粉中混有的镁粉_____ 。
(2) 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,___ 是氧化剂; ___ 元素被氧化;___ 是氧化产物;该反应的离子方程式为____ 。
(3)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中的还原剂是__ ,还原产物是__ ,离子方程式为__ 。
①氢氧化铜与硫酸
②碳酸氢钠与盐酸
③除去铜粉中混有的镁粉
(2) 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,
(3)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中的还原剂是
您最近一年使用:0次
【推荐1】已知:(1)实验室制取Cl2的方程式为:MnO2+4HCl(浓) 2MnCl2+Cl2↑+2H2O,其中MnO2发生了
2MnCl2+Cl2↑+2H2O,其中MnO2发生了___________ 反应,具有___________ 性,在该反应中HCl体现___________ (填“氧化性”或“还原性”或“酸性”或“还原性和酸性”或“氧化性和酸性”或“氧化性和还原性”)
(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑,用单线桥法表示该反应过程中电子转移的方向和数目___________
(3)用CuCl2作催化剂,在450℃下,用空气中的O2跟HCl反应也能制得氯气,其方程式为4HCl+O2 2H2O+2Cl2上述三种制氯气方法中,从氯元素化合价的变化看,三者的共同点是
2H2O+2Cl2上述三种制氯气方法中,从氯元素化合价的变化看,三者的共同点是___________ 比较以上三个反应,三个反应中氧化剂的氧化能力从强到弱的顺序为___________
 2MnCl2+Cl2↑+2H2O,其中MnO2发生了
2MnCl2+Cl2↑+2H2O,其中MnO2发生了(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑,用单线桥法表示该反应过程中电子转移的方向和数目
(3)用CuCl2作催化剂,在450℃下,用空气中的O2跟HCl反应也能制得氯气,其方程式为4HCl+O2
 2H2O+2Cl2上述三种制氯气方法中,从氯元素化合价的变化看,三者的共同点是
2H2O+2Cl2上述三种制氯气方法中,从氯元素化合价的变化看,三者的共同点是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知反应KClO3+6HCl=KCl+3Cl2↑+3H2O,请回答下列问题
(1)用双线桥法表示出电子转移的方向和数目___________ 。
(2)反应中氧化产物和还原产物物质的量之比为___________ ,盐酸表现出___________ 性和___________ 性。
(1)用双线桥法表示出电子转移的方向和数目
(2)反应中氧化产物和还原产物物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是____________________________
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是__________ 。
②在下面的化学式上标出电子转移的方向和数目_____________________________
KMnO4+ KI + H2SO4→
(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是______________________________________ 。
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是
②在下面的化学式上标出电子转移的方向和数目
KMnO4+ KI + H2SO4→
(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】我国四大发明之一的黑火药是硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: 。
。
(1) 属于
属于_______ 化合物(填“共价”或“离子”), 的电子式为
的电子式为_______ 。
(2)该反应的氧化剂是_______ 。
(3)若反应中转移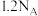 个电子,则被
个电子,则被 氧化的C的质量是
氧化的C的质量是_______ g。
 。
。(1)
 属于
属于 的电子式为
的电子式为(2)该反应的氧化剂是
(3)若反应中转移
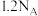 个电子,则被
个电子,则被 氧化的C的质量是
氧化的C的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氯及其化合物在生产生活中应用广泛。
(1)在元素周期表中,元素Ts跟氯元素位于同一主族。它的一种核素可由核反应 →
→ 得到,Ts的原子结构示意图可表示为:
得到,Ts的原子结构示意图可表示为: ,则m=
,则m=___________ , 的中子数为
的中子数为___________ 。
(2)海水制得的粗盐中含有MgCl2、CaCl2、Na2SO4等杂质。某同学设计了以下除杂流程,请将下表补充完整:
(3)高氯酸(HClO4)是一元强酸,在工业上有重要用途。写出高氯酸与小苏打溶液反应的离子方程式___________ 。
(4)ClO2是一种安全高效的消毒剂。以单位质量得到的电子数表示消毒效率,ClO2的消毒效率是Cl2的___________ 倍。
(1)在元素周期表中,元素Ts跟氯元素位于同一主族。它的一种核素可由核反应
 →
→ 得到,Ts的原子结构示意图可表示为:
得到,Ts的原子结构示意图可表示为: ,则m=
,则m= 的中子数为
的中子数为(2)海水制得的粗盐中含有MgCl2、CaCl2、Na2SO4等杂质。某同学设计了以下除杂流程,请将下表补充完整:
| 实验步骤 | 添加的试剂 | 预期沉淀的离子 |
| 1 | ||
| 2 | BaCl2溶液 |  |
| 3 | ||
| 4 | 适量稀盐酸 |
(3)高氯酸(HClO4)是一元强酸,在工业上有重要用途。写出高氯酸与小苏打溶液反应的离子方程式
(4)ClO2是一种安全高效的消毒剂。以单位质量得到的电子数表示消毒效率,ClO2的消毒效率是Cl2的
您最近一年使用:0次

 和
和 ,即可得到
,即可得到 ,该反应的还原产物是
,该反应的还原产物是 ____
____ ____
____ ____
____ ____
____ ____
____
 ,则该元素氧化物的化学式为
,则该元素氧化物的化学式为

